Manejo de la Toxicidad Asociada a Medicamentos
Regresar al Procesos de Soporte Asistencial, Enfermería y Aplicación de Medicamentos
AMBULANCIAS PROMOVER
Teléfono: (60 8 2739402 Extensión:123
Celular: 3153198987
Correos: coordinacionambulancias@promoversas.com.coradioperacionambulancias@promoversas.com.co
Identificación
|
Nombre |
Código |
|||
|
Manual Manejo de la Toxicidad Asociada a Medicamentos |
MPA3 | |||
|
Fecha de Emisión |
Fecha de Actualización |
Versión | ||
|
2003-01-10 |
2024/03/27 |
10 | ||
Elaboró: Servicio de Enfermería
Reviso y Aprobó Ultima versión: Comité de farmacia y terapéutica
Introducción
Los medicamentos disponibles hoy en día en el manejo de las enfermedades oncológicas y otras patologías crónicas generan efectos secundarios al ejercer su acción sobre células cancerígenas y células sanas que comparten procesos metabólicos y funcionales. Las células más afectadas por el efecto citotóxico de la quimioterapia son las de mayor tasa de replicación celular como folículos pilosos, médula ósea, tubo digestivo y el sistema reproductor.
De otro lado reacciones de hipersensibilidad, cardiotoxicidad, neurotoxicidad requieren un cuidadoso manejo pues ejercen una influencia negativa sobre la calidad de vida de los pacientes, así como un riesgo vital.
Este manual presenta un abordaje de estas posibles complicaciones desde el punto de vista del manejo en Oncomedic ltda en sus dos sedes.
Objetivo
Establecer los lineamientos procedimentales para abordar la toxicidad generada por los medicamentos que se prescriben y/o administran en oncomedic ltda.
Alcance
El manejo de la toxicidad en oncomedic ltda inicia desde el momento mismo de la planeación de la actividad asistencial, donde se identifican los riesgos dadas las condiciones de la prestación del servicio, lo que permite abordar estrategias para su posterior manejo, continua con la atención del usuario durante la consulta medica donde se identifican los riesgos inherentes al individuo, incluye las terapéuticas instauradas y las medidas de control ante los riesgos identificados donde se realiza un trabajo conjunto con el paciente y el equipo asistencial y termina con el seguimiento del paciente.
Descripción
Tomando en cuenta el riesgo de sufrir toxicidad por la administración de los medicamentos en oncomedic ltda se realizan diversos procedimientos para reducir el riesgo
- Gestión de medicamentos
- Consulta Especializada
- Soporte Asistencial y Enfermería y Aplicación de Medicamentos
- Programa de Seguridad del Paciente
- Farmacovigilancia
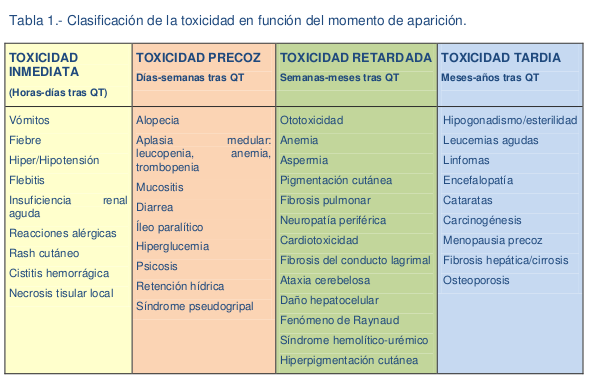
Los medicamentos pueden generar grados diversos de toxicidad en los diferentes momentos, en función del tiempo se clasificaran así:
Tomado de Toxicidad de los tratamiento antineoplasicos, Ana Blasco Cordellat, Cristina Caballero, Carlos Campo Herrero.
Servicio de Oncología Médica Hospital General Universitario de Valencia
Toxicidad inmediata
Emesis
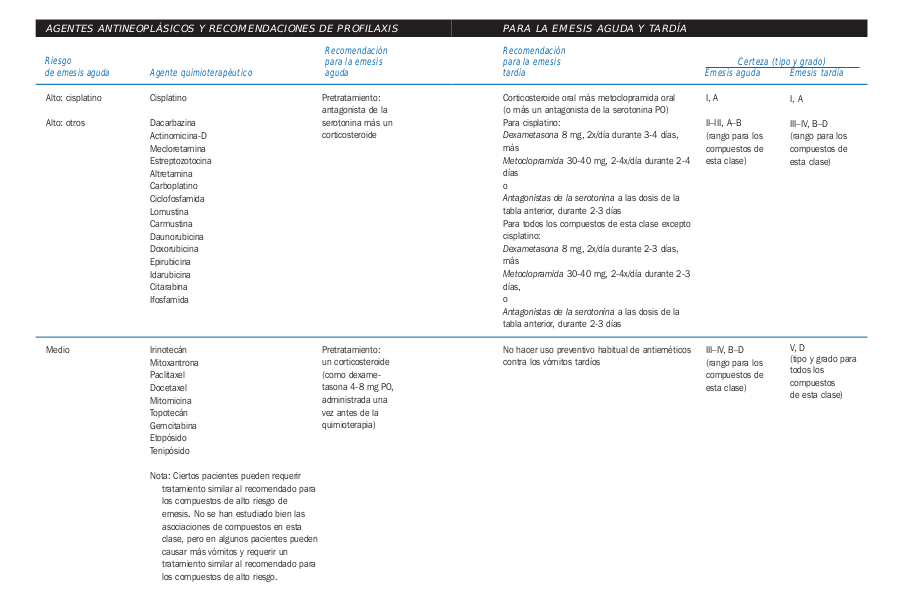
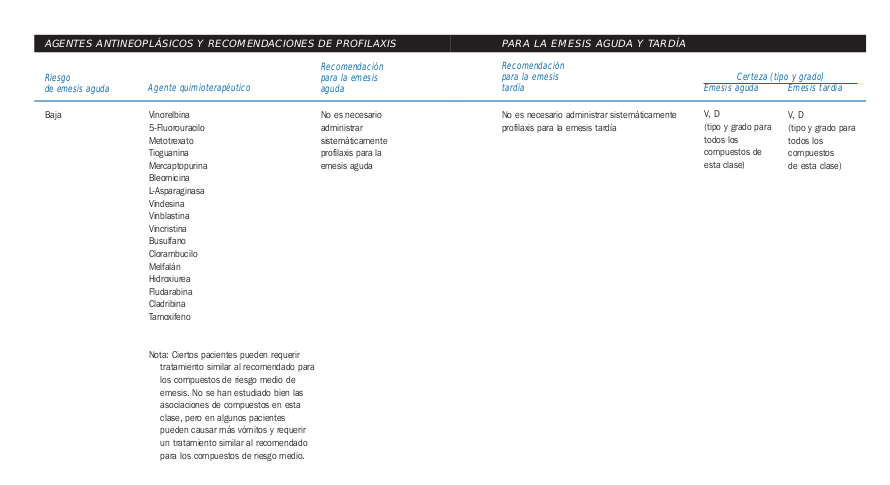
- Factores de riesgo de emesis aguda
- Características del paciente
- Agentes quimioterapéuticos
Tomado de la Guía de Quimioterapia AMGEN
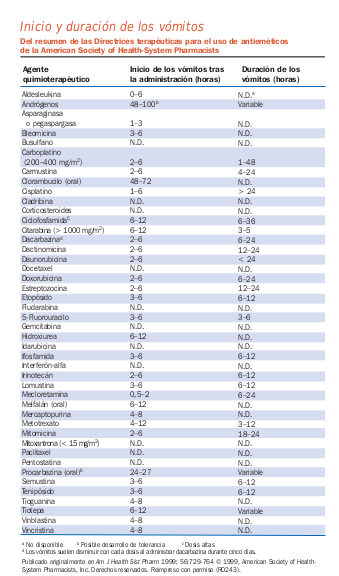
- Tipos de emesis
- Emesis aguda (vómitos que tienen lugar entre 0 y 24 horas después de la quimioterapia)
- Vómitos tardíos (vómitos que ocurren > 24 horas después de la quimioterapia)
- Emesis anticipatoria
- Antieméticos:
- Mayor índice terapéutico antagonistas de los receptores 5-HT3 como ondansetron y los corticoides
- Menor índice terapéutico como antagonistas de la dopamina, butirofenonas, fenotiazinas y cannabinoides
- En casos de quimioterapia con riesgo alto de emesis, se recomiendan los antagonistas selectivos de la serotonina (con dexametasona)
- También pueden ser de uso fármacos adyuvantes como benzodiazepinas y antihistamínicos, pero no se recomiendan como monoterapia
- Puede ser recomendable el uso de asociaciones
- En caso de emesis anticipatoria se aconseja el uso de los regímenes antieméticos apropiados más activos que se administre para prevenir los vómitos agudos o
tardíos. Éstos deben administrarse junto con la quimioterapia inicial, así mismo es recomendable el tratamiento conductual con desensibilización sistemática. - Nuevos antieméticos:
- Palonosetrón es un nuevo antagonista de los receptores de la serotonina con mayor afinidad por los receptores 5-HT3. Se han publicado dos estudios clínicos en los
que ha resultado más eficaz que ondansetrón1 y dolasetrón2 frente a la quimioterapia moderadamente emetógena. - Aprepitant es el primero de una nueva clase de antieméticos, los antagonistas de los receptores de la neurocinina. La adición de este fármaco al tratamiento
estándar con un antagonista de la serotonina y un corticosteroide mejora el control tanto de la fase aguda como de la tardía frente a la quimioterapia altamente
emetógena.
Reacción Alérgicas y de Hipersensibilidad
- La fiebre o hipertermia inmediata puede estar asociada directamente al uso fármacos como Interleukinas, Interferon, Bleomicina. Temsirolimus, Cetuximab, Rituximab, trastuzumab, aabitualmente este tipo de fiebre secundaria a fármacos ocurre en las primeras horas tras la administración y desaparece rápidamente. En otras ocasiones, sin embargo, la fiebre ocurre a partir de las 48 horas tras la administración del fármaco y dura varios días, lo que dificulta la distinción de otras causas farmacológicas e infecciosas, y conlleva la administración empírica de antibióticos, las manifestaciones clínicas pueden ser similares a las de las reacciones alérgicas, con aparición posterior de manifestaciones cutáneas (exantema generalizado o exantema fijo). La fiebre secundaria a fármacos, no responde al tratamiento con antibióticos, desapareciendo con la suspensión del tratamiento y con corticoides (lo que sugiere su origen inmunológico/alérgico).
- Reacción Alérgicas y de Hipersensibilidad aparecen durante la infusión del tratamiento frecuentemente asociadas a Anticuerpos monoclonales como Rituximab Trastuzumab y Cetuximab, entre los 30 y los 120 minutos del inicio de la infusión y se resuelven disminuyendo la velocidad de la perfusión o interrumpiéndola, precisando en casos excepcionales (reacciones anafilácticas) medidas de soporte farmacológico.
- La cardiotoxicidad puede ocurrir durante el tratamiento o pocas horas después de su administración y consiste principalmente en taquicardias supraventriculares. Estos efectos son, por lo general, transitorios y ocurren en hasta un 40% de los pacientes; no son dependientes de la dosis ni están relacionados con el desarrollo de miocardiopatía posterior. En algunos casos pueden evolucionar desarrollando un derrame pericárdico, pudiendo llegar al fallo cardíaco. Desaparecen al interrumpir el tratamiento, para su prevención y control debe haber una adecuada valoración del paciente, valoración de los signos vitales del paciente y su estado generala antes y durante la administración del medicamento, Infusión lenta de medicamentos cardiotoxicos
- Hipotensión se puede generar como consecuencia de algún régimen de quimioterapia, debido principalmente a la depleción de volumen como consecuencia del vómito secundario a la toxicidad gastrointestinal, sin embargo, otras causas pueden ser origen vascular, como la pérdida del tono vascular y el incremento de la permeabilidad capilar en vasos y capilares, en la mayoría de los pacientes es un fenómeno transitorio que requiere incrementar la administración de fluidos y, en ocasiones, tratamiento farmacológico con agentes depresores, El uso de interleucinas ha evidenciado hipotensión severa, fenómenos isquémicos y disritmias; aunque la causa no está bien determinada, quizá estos fenómenos tengan una causa común y algunos datos apuntan hacia la alteración en la síntesis del óxido nítrico.
- Prodromo: ansiedad, angioedema, broncoespasmo.
- Fiebre y escalofríos,
- Nauseas, vómitos
- Cefalea, dolor en la zona tumoral
- Rigidez
- Disnea, sensación de opresión
- Rash, exantema: Aparición de pequeñas pápulas que van confluyendo hasta formar placas generalizadas
- Hipotensión moderada a severa
- Anafilaxia: Aparición de disnea (sensación de ahogo), flushing (enrojecimiento facial) y dolor torácico. asociadas a Paclitaxel, Carboplatino, Oxaliplatino, Docetaxel, Etopósido, Ciclofosfamida, Ifosfamida Temsirolimus.Cetuximab, Rituximab Trastuzumab
- Paro cardio respiratorio
Tratamiento y medidas de control generales
- Premedicación con dexametasona, difenhidramina y antagonista del receptor 2 de la histamina, acetaminofen.
- Retirar del fármaco responsable, lo que produce mejoría del proceso.
- Monitorear los signos vitales, en caso de disnea asegurar que la vía aérea esté libre (dentadura postiza, vómito, otros), retirar las prendas que opriman (faja, corbata).
- Administración intravenosa (IV) rápida de difenhidramina 50mg o 10mg de clorfeniramina.
- Administración IV de hidrocortisona 10 mg.
- Si hay hipotensión, se deben elevar las extremidades inferiores o piernas hasta que los fluidos retornen la presión sanguínea.
- En brocoespasmo leve se pueden utilizar beta estimulantes administrando ß2 estimulantes (salbutamol) vía inhalatoria, 2 inhalaciones cada 10 ó 20 minutos hasta 1 hora.
- Reinicio de la infusión aproximadamente 30 minutos después de la resolución completa del cuadro clínico, aumentando el tiempo de infusión.
- Los casos graves, pueden requerir medidas de soporte vital, hospitalización y tratamiento con corticoides intravenosos.
Código Azul:
Es un sistema de alarma para el manejo de pacientes en paro Cardio-respiratorio por un grupo entrenado y coordinado con previas funciones establecidas.
Equipo de Código Azul: Es el grupo de personas debidamente capacitadas y entrenadas para atender el llamado de un eventual CÓDIGO AZUL
.OBJETIVO
Describir el sistema de alerta para una respuesta rápida, coordinada y eficiente en el manejo de pacientes en paro Cardio-respiratorio de modo que se brinde una atención y reanimación en el menor tiempo disminuyendo la morbi-mortalidad en la atención.
ALCANCE
Este procedimiento aplica a todos los usuarios internos/externos, que se encuentren dentro de Oncomedic/saludarte y que presenten situaciones de emergencia con riesgo vital, inminencia de paro o que requieran reanimación cerebro-cardiopulmonar.
AUTORIDAD Y RESPONSABILIDAD:
La autoridad está a cargo del médico, la responsabilidad estará a cargo de médico, la enfermera jefe y auxiliares de enfermería. Todo el personal médico, asistencial y administrativo de la institución.
Asignación de funciones:
Líder: Coordina las acciones del equipo en el momento en que se presenta el Código Azul. Verifica pulsos carotideos, femoral, índica el momento de iniciar RCP, estimula a los demás asistente a realizar sus actividades con calidad y seguridad.
Ordena medicamentos, asesora y constata las funciones del equipo. Se asegura del manejo de la vía aérea. Verifica que el masaje se haga de una manera efectiva. Revisa el acceso venoso. Puede cambiar las funciones de cualquier miembro del equipo. Vigila e interpreta el registro de los monitores. Coordina las funciones del equipo.
Asistente de compresiones torácicas: Se encarga de realizar Verifica signos de paro cardíaco, ausculta ruidos cardíacos y pulmonares, evalúa el paciente, realiza 5 ciclos de compresiones torácicas, firmes, continuas, de buena calidad de 5 cm de profundidad, dejando regresar el tórax a su posición normal, con el mínimo de interrupciones, se comunica con el asistente de vía aérea para realizar el ciclo de compresión/ventilación 30/2 en la fase de soporte vital básico. En el avanzado deben ser compresiones continuas, se intercambia con el circulante cada 5 ciclos o dos minutos (o antes si presenta signos de fatiga), indicados por el líder para garantizar la RCP de calidad
Asistente de Vía Aérea:
Se encarga de revisar y libera la vía aérea para posteriormente asegurarla, con los dispositivos indicados para el caso según protocolo, evalúa expansibilidad torácica, proporciona ventilación, introduce los dispositivos para la vía aérea necesarios dependiente la situación actual del paciente y controla pulso carotideo.
Asistente Circulante DEA/MONITOR:
Se encarga de Traer y utilizar el DEA/monitor
Retira inmediatamente las ropas del paciente
Monitoriza al paciente conectando los electrodos al paciente,
Se intercambia con el compresor cada 5 ciclos o dos minutos (o antes si presenta signos de fatiga)
Coloca el monitor en un lugar donde el líder del equipo (y la mayoría del equipo) lo pueda ver.
Asistente de Medicamentos: Se encarga de canalizar 2 vías venosas de grueso calibre (18-16), fija la venoclisis y revisa su permeabilidad. Administra medicamentos ordenados por el líder, administra volumen para arrastrar el medicamento y eleva la extremidad según protocolos, verifica tiempos de aplicación y dosis, Informa inconvenientes de paso de medicamentos y sirve de relevo para dar compresiones de calidad.
Asistente del Registro: Lleva el tiempo desde el inicio del código azul, informa cada 3 minutos al líder el tiempo transcurrido, Se mantiene en comunicación con el Líder, registra la hora de las intervenciones y de la medicación (y avisa cuando se deben llevar a cabo las Próximas), describe ordenadamente las acciones, registra la frecuencia y duración de las interrupciones de las compresiones, realiza informe de la reanimación, trasmite estos datos al líder del equipo (y al resto del equipo) Este equipo en caso necesario puede estar apoyado por:
Proceso de activación
La reanimación con éxito tras un paro cardíaco requiere un conjunto integrado de acciones coordinadas que se representan con los eslabones de la cadena de supervivencia. La reanimación eficaz requiere una respuesta integrada conocida como un sistema de atención. La apreciación colectiva de las dificultades y oportunidades presentes en la cadena de supervivencia pasa a ser un elemento fundamental en un sistema de atención en el que las reanimaciones se concluyen con éxito.
Por tanto, los individuos y grupos deben trabajar juntos, compartir ideas e información, para evaluar y mejorar sus sistemas de reanimación. La capacidad de liderazgo y de responsabilidad son componentes importantes de este abordaje del equipo.
Los pacientes que sufren un paro cardíaco dependen de un sistema de vigilancia y prevención del paro cardíaco apropiado. Cuando sobreviene el paro cardíaco, los pacientes dependen de una interacción fluida entre los respondientes de la situación y la red de atención.
Quien detecte una persona (paciente, visitante, trabajador) con pérdida súbita del estado de conciencia y no responde al llamado ni al estímulo táctil o ante la sospecha de un paro, activara la alerta para el código azul de la siguiente forma:
- Llamado Código Azul
- Respuesta al llamado: Cada miembro del equipo debe acudir al lugar del evento en un tiempo menor a 3 minutos a partir del momento en que se ha recibido la alerta, cumpliendo con los algoritmos de reanimación definidos en la guía Reanimación Cardio-Cerebro-Pulmonar, hasta el resultado final de la evolución del paciente.
Precauciones:
Todo paciente que requiera la intervención del equipo de Código azul debe ser considerado como potencialmente infectado, por esta razón es importante tener en cuenta:
▪ Uso obligatorio de guantes, tapabocas y gafas y en general los elementos de protección personal para todos los miembros del equipo que participen en la Reanimación.
▪ Manejo cuidadoso de los elementos corto-punzantes, agujas, hojas de bisturí, catéteres, etc. Para evitar accidentes de riesgo biológico
▪ Manipulación adecuada de secreciones y fluidos corporales, así como de las lesiones cutáneas y heridas quirúrgicas.
▪ Lavado de manos antes y después del contacto con el paciente, siempre que sea posible.
Prácticas Generales
Tienen como objetivo que los errores no causen efectos adversos a los pacientes y deben estar basadas en los siguientes principios básicos de seguridad:
1) Reducir la posibilidad de que los errores ocurran:
a) Estandarizar las dosis, concentraciones y/o volumen de los medicamentos a utilizar
b) Limitar el número de presentaciones de los medicamentos
c) Verificar que el medicamento administrado sea el ordenado.
2) Hacer visibles los errores:
a) Una vez ocurran, para actuar antes de que alcancen al paciente.
b) Implementar sistemas de “doble chequeo”, ya que es menos probable que dos personas distintas se equivoquen al controlar el mismo proceso cuando se utilizan bombas de infusión para administrar medicamentos.
3) Minimizar las consecuencias de los errores
a) Realizar cambios en los productos o en los procedimientos de trabajo que reduzcan la gravedad de los posibles efectos adversos causados por los errores de medicación.
b) Uso adecuado de medicamentos
Atención de la Emergencia
Paro cardio respiratorio
- Conservar la calma, Pedir ayuda,
- Llamar al servicio de emergencia y al médico tratante
- Colocar al paciente en posición de seguridad decúbito supino.
- Permeabilizar la vía aérea, extraer cuerpos extraños, prótesis dentales de la cavidad oral extensión de la cabeza hacia atrás y elevación de la mandíbula.
- Retirar las prendas que opriman (faja, corbata).
Uso del ambu: Luego de permeabilizar la vía aérea colocar la mascarilla del ambú encima de la nariz y la boca, con el extremo estrecho encima del puente de su nariz y el extremo ancho encima de la boca, para mantener un sello hermético, coloque los dedos 3, 4 y 2
Suministro de Oxigeno:Permite incrementar la cantidad de oxigeno en el aire inspirado, manteniendo una saturación de O2 en sangre arterial superior al 90%, corrigiendo o previniendo la hipoxemia y reduciendo el trabajo respiratorio y el gasto cardiaco.
- Indicaciones:
- Hipotensión
- Bradicardia
- Angina de Pecho
- Respiración superficial, Hipoventilación, Disnea, Cianosis.
- Reducción de la saturación de Oxigeno.
- Disminución de la cantidad de oxígeno o de la presión parcial del oxígeno en el gas inspirado.
- Disminución de la ventilación alveolar.
- Alteración de la relación ventilación/perfusión.
- Alteración de la transferencia gaseosa.
- Aumento del shunt intrapulmonar.
- Descenso del gasto cardíaco.
- Hipovolemia.
- Disminución de la hemoglobina o alteración química de la molécula.
- Recomendaciones
- Permear vía aérea
- Realizar las conexiones
- Llenar con agua destilada el humidificador (si aplica)
- Abrir el suministro
- Verificar el apropiado funcionamiento
- Colocar la mascarilla asegurándola con el elástico evitando presiones exageradas
- Determinar el flujo de administración.
- Monotorizar al paciente y actuar según situación clínica
- Realizar el registro
Fuente: Murrant T; Bihari D. 2000.Anaphylaxis and anaphylactoid reactions. Int J Clin Pract 54 (5): 322-328. Hernández M, Catena ,Pérez García M, Martín Bragado M, González Martínez A, Mestre Rodríguez M 1998.
Paro Cardiopulmonar: se manifiesta con:
- Abolición de los pulsos femoral y carotideo
- Perdida de conciencia
- Paro respiratorio (apnea)
- Dilatación de pupilas que aparecen 40” después del paro.
Tratamiento: busca asegurar la correcta oxigenación mediante la permeabilidad de las vía aérea y la adecuada ventilación del paciente, restablecer la circulación de sangre oxigenada y prevenir las lesiones celulares irreversibles, traslado a un centro asistencial.
- Conservar la calma y pedir Ayuda
- Llamar al servicio de emergencia y al medico tratante
- Colocar al paciente en posición de seguridad decúbito supino.
- Permeabilizar la vía aérea, extraer cuerpos extraños, prótesis dentales de la cavidad oral extensión de la cabeza hacia atrás y elevación de la mandíbula.
- Retirar las prendas que opriman (faja, corbata).
- Iniciar RCP básica:
Comprobar la hora de inicio de la RCP.
Utilizar ambú para ventilar al paciente
Monitorizar signos vitales
Uso del DEA
Epinefrina: Solución acuosa concentración 1:1000, Ampolla de 1 mg en 1 cc (1:1000) 0.3 ml a 0.5 ml subcutánea o IM, la dosis se repite c/ 5 a 10 min si no hay mejoría clínica 0.1ml/kg La dosis se repite c/ 5 a 10 min si no hay mejoría clínica
Puede ser necesario expandir la volemia con líquidos IV.
Se administra un bolo inicial de 500-1000 mL de solución fisiológica seguida por una infusión ajustada Corticoides Dexametasona: 4mg/ml
Lidocaina 0,5 - 1 mgr / kg / iv, hasta dosis total de 3mgr/ kg.
Administración de atropina 1mg en bolo IV repetir cada 5 minutos hasta un máximo de 3mg.)
Continuar con la maniobra hasta estabilizar al paciente o recibir ayuda
Control y destino del paciente.
Una vez terminada la reanimación con resultado positivo, se remite el paciente a un centro hospitalario para su evaluación y manejo posterior.
Si el paciente fallece deberá realizarse los respectivos tramites con medicina legal previa información a los familiares.
Realizar los trámites administrativos, como descripción detallada de las actividades realizadas, de los insumos y medicamentos utilizados, cada uno de los integrantes del equipo de código azul regresará a su respectivo servicio
Solicitud en el sistema para que sean repuestos por el personal de farmacia los materiales y medicamentos del carro de paro, con el fin que esté todo completo en caso de volver a requerirse.
Reporte del evento adverso y evaluación: El líder del grupo informa inmediatamente terminada la reanimación sobre la actividad, lo positivo y negativo con el fin de seguir mejorando y perfeccionando cada vez más el sistema, el caso se analiza en el comité de seguridad del paciente y/o de farmacia según corresponda.
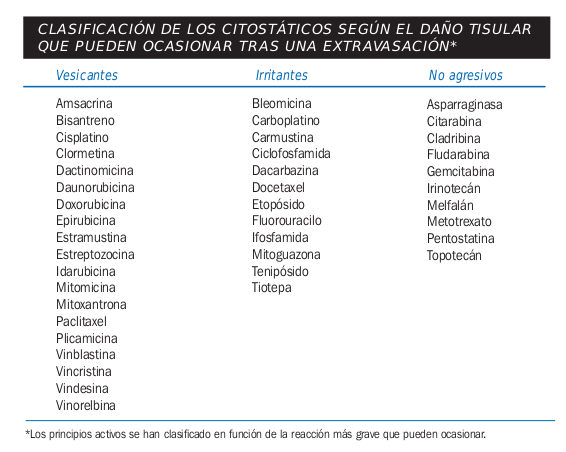
Extravasación de Agentes Citostáticos
Una de las principales complicaciones en la administración de medicamentos, es la posibilidad de que se produzca una extravasación, lo que podría ocasionar grave daño al tejido adyacente, dependiendo del tipo de medicamento que se esté utilizando.
Factores de riesgo:
- Pacientes que no puedan comunicarse.
- Pacientes con historia de enfermedades vasculares periféricas, diabetes.
- Pacientes que han recibido previamente radioterapia en la zona de punción.
- Pacientes sometidos a terapia intravenosa previa de larga duración.
- Elección inapropiada de la cánula intravenosa utilizada.
- Realización de la administración por personal con escasa experiencia.
- Localización inapropiada de la punción.
- Uso de medicamentos citostáticos que pueden causar irritación al extravasarse como:
Tomado de la guía de quimioterapia Amgen
Prevención:Las principales medidas a tomar en cuenta para evitar las extravasaciones son:
- Ejecución de los procedimientos por personal con experiencia.
- Conocer los medicamentos a administrar.
- Dilución correcta.
- Velocidad de administración adecuada
- Mantener una vigilancia cuidadosa.
- Elección correcta del lugar de la punción, Se debe elegir un vaso con gran flujo que permita una dilución rápida.
- Elección correcta de la cánula.
- Correcto método de administración.
Identificación de la extravasación:La identificación de la extravasación debe ser lo más precoz posible, la sintomatología que puede inducir sospecha es la aparición de dolor súbito en el área de aplicación, aspecto erítematoso o pálido y sensación local de calor, frío o quemazón.
Manejo De Extravasaciones:El mejor tratamiento de la extravasación es evitarla, en caso que no sea posible su diagnostico precoz también constituye un aspecto fundamental y su apropiado manejo, ante los síntomas antes mencionados:
- Suspenda inmediatamente el goteo, aún cuando no sea evidente una zona de infiltración o el retorno venoso esté aún presente.
- Retire la infusión y la venoclisis, pero no el catéter.
- Aspire con una jeringa de baja presión (1 o 2 c.c.) una o dos veces o tantas como sea necesario, hasta extraer el liquido extravasado.
- Si se aprecia alguna ampolla subcutánea, extraer su contenido con aguja fina
- Administrar el antídoto si existe (consultar al médico).
- Usualmente se recomienda el uso por vía subcutánea hidrocortisona en forma consecutiva y en forma de corona
- Retirar el catéter.
- Elevar la extremidad, colocar compresas tibias sobre el sitio de la extravasación esta aumenta la circulación local favoreciendo la absorción del medicamento extravasado (menos frente a los alcaloides de la vinca). o aplicar hielo que permite reducir el dolor
- Documentar el incidente.
- Llevar a cabo un seguimiento.
Toxicidad Precoz o Aguda
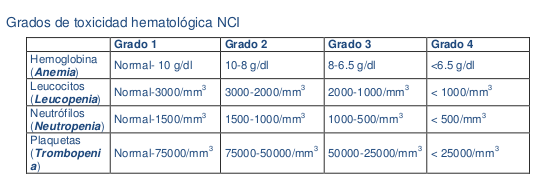
Toxicidad Hematológica
Como los agentes quimioterápicos actúan sobre los distintos mecanismos de la división celular, afectan también a las células sanas, especialmente a las que tiene una gran capacidad de replicación o renovación dentro de las que se encuentran las celulas hematopoyéticas causando mielosupresión, el tiempo y duración de la mielosupresión depende no sólo del esquema quimioterápico (fármacos, dosis, duración, vía de administración) sino que también del paciente (edad, estado nutricional, funcionamiento de la médula, tratamientos previos; los fármacos antidiana, producen poca toxicidad hematológica, destacando entre ellos el Rituximab, con un 48% de citopenias grado 3-4, siendo principalmente linfopenias, el Imatinib, con neutropenia y Bortezomib, con plaquetopenias prolongadas
- Anemia: La incidencia de anemia en el paciente en tratamiento antineoplasico depende del tipo y dosis de quimioterápico, tipo de tumor (más frecuente en linfomas, pulmón, ovario, genitourinario), las manifestaciones clínicas asociadas son astenia, taquicardia, disnea y están relacionadas con la severidad y la velocidad de instauración. En el tratamiento se pueden utilizar transfusiones de concentrados de hematíes y la eritropoyetina (EPO).
- Neutropenia: reducción por debajo de 2000 cels/mm 3 de neutrófilos en sangre periférica que conlleva una importante alteración de los mecanismos de defensa contra infecciones, que puede llegar a ser mortal. Se denomina neutropenia febril a la existencia de temperatura axilar mayor de 38,5o C durante más de una hora y con un recuento absoluto de neutrófilos menor de 500 mm3, en un 48-60% de los pacientes que presentan neutropenia febril existe una infección, se trata de una situación amenazante para la vida del paciente, por el alto riesgo de infecciones agresivas y la inapropiada respuesta defensiva que puede desarrollar el paciente.
Manifestaciones clínicas de alarma: que pueden indicar infección cuando hay un descenso de los neutrófilos:
*Escozor al orinar.
*Fiebre.
*Enrojecimiento, hinchazón o dolor en lesiones, heridas quirúrgicas o catéteres
*Cansancio.
*Cefalea.
*Dolores musculares.
*Dificultad para tragar.
*Sensación de calor o frío.
*Dolor en abdomen.
*Escalofríos o tiritona.
*Diarrea.
*Dolor de garganta.
*Molestias en recto o ano al defecar.
*Tos o dificultad para respirar.
*Congestión nasal.
Para prevenir la incidencia y disminuir la duración de la neutropenia post- quimioterapia se utilizan factores estimulantes de colonias de granulocitos (G-CSF), que están indicados en los siguientes casos:
* Profilaxis Primaria en pacientes con alto riesgo de desarrollar neutropenia febril
La Profilaxis secundarios a se realiza en pacientes que desarrollaron neutropenia febril en ciclos previos.
En la neutropenia febril se usan junto con el tratamiento antibiótico en pacientes en los que se prevea una alto riesgo de complicaciones asociadas a la infección y tengan factores de mal pronóstico (<110 neutrófilos/ mm3, enfermedad primaria no controlada, hipotensión, bacteriemia, comorbilidad).
Los factores estimulantes de granulocitos (G-CSF) se utilizan a dosis de 5 m/ Kg/ día por vía subcutánea, 24-72 horas después de finalizar el ciclo de quimioterapia. Se suele mantener el tratamiento hasta que se alcanza un recuento de neutrófilos de 10.000/ mm3.
Riesgo de Infecciones:
Resumen de las Directrices para el uso de antimicrobianos en pacientes neutropénicos con cáncer de la Infectious Diseases Society of America
- Fiebre: una única toma de la temperatura oral ≥ 38,3°C o una temperatura ≥ 38,0°C durante una hora o más.
- Neutropenia: recuento de neutrófilos < 500 células/mm3 o < 1000 células/mm3 previéndose una disminución a < 500 células/mm3.
Tratamiento antibiótico inicial
- Sólo para adultos de bajo riesgo usar ciprofloxacino más amoxicilina/ácido clavulánico. No está indicada la monoterapia con vancomicina
- Elegir tratamiento con uno de los siguientes compuestos: cefepima, ceftazidima, imipenem o meropenem.
- Elegir un aminoglucósido junto con una penicilina activa contra Pseudomonas, cefalosporina (cefepima o ceftazidima) o carbapenem.
- Elegir cefepima o ceftazidima más vancomicina, con o sin un aminoglucósido; carbapenem más vancomicina, con o sin un aminoglucósido; o una penicilina activa
contra Pseudomonas más un aminoglucósido y vancomicina. - Modificación de la terapia durante la primera semana de tratamiento
*Si se identifica un agente etiológico, administrar el/los fármaco/s más adecuado/s.
*Si no se identifica un agente etiológico y el paciente presenta en principio un riesgo bajo, y se ha instaurado un antibiótico oral sin complicaciones posteriores,
continuar utilizando los mismos fármacos.
*Si el paciente presentaba inicialmente un riesgo bajo y se instauró un tratamiento con fármacos intravenosos sin complicaciones posteriores, se puede cambiar,
después de 48 horas, a ciprofloxacino oral más amoxicilina/ácido clavulánico.
*Si el paciente presenta inicialmente un riesgo alto sin complicaciones posteriores, continuar utilizando los mismos fármacos intravenosos.
*Si presenta fiebre persistente durante los primeros 3-5 días: Volver a evaluar el tratamiento el tercer día. Si no hay empeoramiento clínico, continuar usando los mismos antibióticos; interrumpir la vancomicina si los cultivos son negativos. - En caso de progresión de la enfermedad, cambiar los antibióticos.
- Si la fiebre persiste más de cinco días, considerar añadir un antifúngico, cambiando o no la pauta antibiótica.
- Uso de antivirales: No se recomienda el uso habitual de antivirales, a menos que haya pruebas (clínicas o de laboratorio) de infección vírica.
- Uso de factores estimuladores de colonias: No se recomienda el uso indiscriminado de factores estimuladores de colonias,
aunque debería considerarse en caso de que se prevea un empeoramiento. - Profilaxis antibiótica en pacientes neutropénicos afebriles: Para evitar la aparición de resistencias, la profilaxis antibiótica no se usa habitualmente, excepto trimetoprima-sulfametoxazol para prevenir la neumonitis por Pneumocystis carinii. Es necesaria la profilaxis antifúngica con fluconazol y la profilaxis antivírica con aciclovir o ganciclovir en pacientes sometidos a trasplante alogénico de citoblastos hematopoyéticos.
- Trombocitopenia y hemorragias: Disminución del recuento sanguíneo de plaquetas (<100.000-150.000/l), que coloca al paciente en riesgo de sufrir de complicaciones hemorrágicas como epistaxis, hemoptisis, hematemesis, melenas, hematomas o petequias, es importante
- Evitar el riesgo de traumatismos o heridas.
- Precaución con las maquinillas de afeitar.
- Evitar el estreñimiento.
- Aumentar la ingesta de líquidos para una correcta hidratación.
- Emplear cepillas de dientes suaves.
- Evitar el empleo de enemas, supositorios y laxantes potentes.
- Emplear protectores gástricos (sobretodo si tiene prescritos antiinflamatorios).
- Evitar los antiagregantes plaquetarios como la Aspirina, sustituyéndolos por acetaminofen.
Hemorragias relacionadas con farmacos: Los antiangiogénicos como el Bevacizumab actúan sobre el Factor de crecimiento del endotelio vascular que tiene un papel fundamental en mantener la integridad de los tejidos y la reparación de las heridas, de modo que su inhibición puede causar retraso en la cicatrización y complicaciones hemorrágicas, de tal manera que no deben usarse dentro de los siguientes 28 días de realización de cirugía mayor.
Complicaciones Orales
Diarrea
Es una complicación frecuente en pacientes que reciben quimioterapia 5-fluorouracilo (5FU), Irinotecan, Topotecan, Metrotexate, Cisplatino, Lapatinib, Geftinib, Cetuximab, Bevacizumab, Sorafenib, Sunitinib, o por agentes antidiana, especialmente inhibidores de la tirosin-kinasa (Cetuximab, Lapatinib, Gefitinib y Erlotinib) es consecuencia del daño
producido a nivel de la mucosa del intestino delgado y del colon, produciendo un exceso de fluidos secretados en la luz intestinal. Se trata de una toxicidad limitante de dosis, y se potencia con la asociación de otros fármacos quimioterápicos, como es el caso de la combinación de cetuximab con Irinotecan para el cáncer colorrectal.
La diarrea puede generar tanto disminución de la calidad de vida del paciente como complicaciones importantes por hipovolemia y alteraciones electrolíticas su severidad se evalúa en función del número de deposiciones/ día, la presencia de deposiciones nocturnas, la necesidad de tratamiento intravenoso y la presencia de de moco y/o sangre en las heces.
El tratamiento depender de la severidad de la diarrea así como de la presencia de factores como fiebre, vómitos, neutropenia, sangrado franco en la deposición, dolor abdominal moderado/severo, deshidratación, los pacientes con diarrea leve y sin factores de riesgo pueden ser tratados ambulatoriamente con medidas farmacológicas y antidiarreicos orales mientras que los que presentan diarrea grave y/o factores de riesgo necesitarán tratamiento hospitalario, es importante definir si la diarrea es de origen infecciosos o medicamentoso para proceder a realizar tratamiento farmacológico, así mismo resulta de vital importancia evitar la deshidratación.
Estreñimiento
Consiste en la disminución del número de deposiciones (menos de dos veces a la semana), asociado a mayor dureza de las heces, se da con mayor frecuencia en mujeres y en los pacientes con tratamiento con opiáceos y con los fármacos habitualmente empleados para prevenir o tratar las nauseas y vómitos; la disminución del ejercicio físico y las deficiencias nutricionales también favorecen a la aparición de estreñimiento.
Es necesario establecer unas correctas medidas higiénico-dietéticas (dietas ricas en fibras y frutas, ingesta abundante de líquidos, ejercicio físico ligero), y si esto no lo soluciona implementar medidas terapéuticas.
Alteraciones en la Piel
- Dermatitis asociada a Metotrexate, 5-FU, Capecitabina, Arabinósido de Citosina, Docetaxel, Doxorrubicina, Bleomicina, en ocasiones aparecen fenómenos de fotosensibilización, descamación, hiperpigmentación (puede aparecer en el trayecto de las venas en las que se administra la quimioterapia)
- Eritrodisestesia palmoplantar asociada a Doxorrubicina, Capecitabina, Citarabina, Docetaxel, 5-FU, Gemcitabina, Vinorelbina. Sunitinib, Sorafenib, se presenta inicialmente como disestesias en palmas y plantas (alteraciones sensitivas, hormigueos) seguido de edema y un eritema simétrico, intenso y bien delimitado, puede progresar a descamación, ulceración, infección y pérdida de función, afecta inicialmente a palmas de manos y pies, pero puede llegar a superficie dorsal de extremidades, región inguinal y axilar, labios, incluso genitales. Aparece normalmente tras 2-3 ciclos de tratamiento. Se trata interrumpiendo o disminuyendo el fármaco implicado. También se pueden usar corticoides y piridoxina con resultados variables. Suele curar en 2-4 semanas tras finalizar el tratamiento. Recomendar al pacientes mantenerse en lugares frescos, remojar frecuentemente pies y manos con agua fría, no usar agua muy caliente para ducharse o lavarse las manos, o lavar platos. 4. Utilizar ropa ancha y calzado cómodo. 5. No hacer ejercicios intensos, especialmente los días siguientes a la infusión. 6. Evitar el sol directo Imágenes de diferentes grados de Eritrodisestesia palmoplantar
Neurotoxicida
Los efectos neurotóxicos pueden aparecer inmediatamente o diferidos (incluso tras largos periodos desde la finalización del tratamiento) y depende del fármaco empleado, la duración del tratamiento y la dosis acumulada del fármaco.
Signos de alarma de inicio de neurotoxicidad:
- Ampliación de la base de sustentación al caminar.
- Inestabilidad al caminar (más en oscuridad)
- Dolor al caminar
- Debilidad en parte distal de las extremidades
- Pérdida de fuerza en dedos de manos, dificultad para realizar tareas que requieran precisión
- Debilidad al flexionar tobillos.
- Pérdida de audición
- Pérdida de sensibilidad (también pérdida de sensación térmica)
- Alteraciones sensitivas (percepción dolorosa)
- Desaparición de los reflejos osteotendinosos
- Ruidos intestinales, a
- Alteración en la motilidad intestinal
El diagnóstico es clínico, y los síntomas o síndromes (asociación e síntomas) que aparecen dependerán de la zona del sistema nervioso dañada, pudiendo dividirse en seis grandes grupos:
- Encefalopatias agudas, asociadas a 5-Fluoruracilo, Ciclofosfamida, Carmustina, Interferón, Interleukina-2, Procarbazina, Citarabina, metrotexate, Fludarabina, se inicia durante el tratamiento, y consiste en confusión progresiva asociada a alucinaciones, afasia (alteración en el habla), letargia, somnolencia y ocasionalmente convulsiones y coma. Se resuelve habitualmente entre 10-14 días después de cese del tratamiento, aunque ocasionalmente pueden quedar daños irreversibles.
- Encefalopatia crónica, asociada a Citarabina, Metrotexate, Ifosfamida, Carmustina, Cisplatino. Consiste en la instauración progresiva de demencia, se inicia entre los 2 meses y los dos años del tratamiento, puede progresar hasta el coma y la muerte del paciente.
- Toxicidad cerebelosa asociada Citarabina, 5-Fluoruracilo. Aparecen síntomas de daño cerebeloso: ataxia, dismetría, disartria, nistagmo. Su inicio suele ser agudo (durante el tratamiento) y pueden quedar daños irreversibles.
- Paralisis de los nervios craneales asociadas a Vincristina, Paclitaxel se manifiensta de acuerdo a par afectado siendo frecuente la aparición de parálisis facial, o movimientos oculares rápidos, se inician durante el tratamiento siendo su curso variable.
- Mielopatia: asociada a Citarabina, Metrotexate, se manifiesta con a aparición de incontinencia urinaria o fecal y alteraciones sensitivas o motoras (alteraciones en la movilidad de extremidades) esta determinado por el nivel del daño medular. Su inicio puede ser a las horas o días del tratamiento, siendo su curso progresivo.
- Neuropatia periférica asociada a Sales de Platino, Vincristina, Taxanos. Se trata del daño neurológico más frecuente, aparece por alteraciones en las fibras de conducción nerviosa, lo que lleva a la pérdida de sensibilidad (posicional, vibratoria, dolorosa y/o térmica) generalmente en las extremidades (característicamente distribución en guante y calcetín). Los pacientes lo describen como presencia de hormigueos (parestesias) en dedos de manos y pies, que conforme progresan se tornan dolorosas (disestesias) Aparecen a las semanas del tratamiento, suelen ser dosis dependientes y presentan una mejoría lenta y progresiva tras el cese de la quimioterapia (generalmente persiste cierto nivel de daño irreversible). En cada visita se pregunta a los pacientes por la aparición de síntomas de daño neurológico, proponiendo reducción de dosis de quimioterapia o suspensión del tratamiento cuando el daño produce algún grado de incapacidad para realizar ciertas actividades de la vida diaria.
Leucoencefalopatia posterior reversible asociado a Bevacizumab, Sorafenib, se puede manifestar clínicamente: cefalea, letargia, confusión, ceguera y otros trastornos neurológicos consecuencia de edematización de la sustancia blanca posterior, frecuentemente se asocia a hipertensión moderada o severa pero no es preciso para el diagnóstico, el cual se hará mediante técnica de imagen con resonancia magnética, debe tomarse precaución en pacientes con hipertensión arterial mal controlada. Ante la aparición de leucoencefalopatia posterior reversible, se debe interrumpir el tratamiento con el inhibidor de la angiogénesis, e iniciar el tratamiento antihipertensivo. Los síntomas suelen mejorar y resolverse en unos días, aunque en algunos pacientes pueden quedar secuelas neurológicas.
Arritmias cardíacas y procesos isquemicos
Pueden aparecer en las primeras doce horas del fin del ciclo de quimioterapia, siendo más frecuente en el segundo ciclo cuadros de fibrilación auricular, bradicardias vasoespasmo coronarios, dolor torácico, taquicardia, disfunción cardiaca, cambios electrocardiográficos y de forma excepcional infarto de miocardio y fallo cardíaco asociados a Ifosfamida, 5-Fluoruracilo, Paclitaxel, Interleukina, Rituxima, Cisplatino, aparece y desaparece espontáneamente y responde a tratamiento farmacológico (nitritos y antagonistas del calcio). El Rituximab puede producir también arritmias supraventriculares.
Enfermedad tromboembólica venosa es una de las complicaciones más frecuentes en el paciente con cáncer, y puede estar asociada a Estramustina, Estrógenos Bevacizumab, Bortezomib, trae graves consecuencias como la trombosis venosa profunda y/o la embolia pulmonar, accidentes isquémicos transitorios (AIT), accidentes cerebrovasculares (ACV), angina de pecho e infartos de miocardio en pacientes en tratamiento con inhibidores de la angiogénesis, a menudo asociado a hipertensión y daño microvascular largamente mantenido en el tiempo. Los factores de riesgo más importantes asociados al desarrollo de estos eventos son: la edad superior a 65 años, presentar una historia previa de este tipo de patología y desde el punto de vista fisiopatológico parece ser que el daño endotelial es básico. Aunque hay datos suficientes para afirmar que el tratamiento anticoagulante combinado con Bevacizumab es seguro, ante la aparición de cualquier evento tromboembólico atribuible a un inhibidor de angiogénesis, las recomendaciones actuales consisten en la interrupción inmediata del tratamiento. Los catéteres venosos centrales (reservorios) se asocian con mayor riesgo de trombosis venosas, infecciones o flebitis.
Toxicidad Pulmonar
El daño pulmonar asociado a quimioterapia se hace mas evidente en protocolos de quimio y radio concomitantes en la región torácica, paro también se ha descrito con el uso de Metrotexate, Bleomicina, Procarbazina, BCNU, Mitoxantrone Gefitinib, Erlotinib. Trastuzumab, Temsirolimus.
Las manifestaciones aparecen inmediatamente a la administración de quimioterapia y/o hasta meses después como Pneumonitis intersticiales inflamatoria con tos, disnea (sensación de falta de aire), febrícula y alteraciones radiográficas típicas (infiltrados pulmonares algodonosos) el pronóstico es bueno, pues la alteración se resuelve con la suspensión del tratamiento y en los casos más persistentes con corticoides.
Este cuadro se ha relacionado con el tratamiento con inhibidores de la Tirosin-Kinasa, como Gefitinib y Erlotinib, aparece dentro de los primeros 90 días de tratamiento, como una neumonía Intersticial de aparición aguda, siendo fatal en un tercio de los casos y cuya frecuencia aumenta en pacientes con antecedente de fibrosis pulmonar, historial de tabaquismo y/o radioterapia torácica previa, por lo que debe ser estudiado su uso comorbilidades pulmonares, y en aquellos con sintomatología respiratoria o hallazgos radiológicos de fibrosis durante los 2 primeros meses de inicio de tratamiento, el tratamiento Pneumonitis intersticiales inflamatoria consiste en la interrupción del tratamiento y la corticoterapia sistémica, en casos severos, el paciente puede precisar del uso de ventilación mecánica, el Trastuzumab, puede producir una pneumonitis con rápida progresión de los infiltrados pulmonares y fallo respiratorio tras la primera dosis o tras 6 semanas de tratamiento.
Toxicidad Tardía
Cardiotoxicidad
Es el daño producido sobre el músculo cardíaco por los fármacos, suele presentarse como una miocardiopatía que evoluciona a insuficiencia cardíaca, o como alteraciones en la contractilidad cardíaca que se manifiestan como arritmias, esta asociada a Antraciclinas, Trastuzumab, Ciclofosfamida, Sunitinib, Lapatinib, Existen otros casos aislados reportados con otros agentes, como bleomicina, cisplatino, taxanes, 5fluoracilo, inmunomoduladores, incluso metotrexato a dosis altas.
Las antraciclinas producen un daño miocárdico que es dosis dependiente, lo que lleva a un fallo cardíaco (insuficiencia cardíaca congestiva, ICC) con el incremento de dosis, hay insuficiencia cardiaca en el 7,5% de los pacientes que han recibido una dosis acumulada de doxorrubicina de 550 mg/m2, y dicho porcentaje aumenta de forma lineal a partir de dicha dosis, excepto en la cardiotoxicidad aguda que ocurre durante el tratamiento o pocas horas después de su administración y consiste principalmente en taquicardias supraventriculares, generalmente transitorias que pueden ocurrir hasta en un 40% de los pacientes, no son dependientes de la dosis ni están relacionados con el desarrollo de miocardiopatía posterior, aunque en algunos casos pueden evolucionar a derrame pericárdico o falla cardíaca, desaparecen al interrumpir el tratamiento
Factores de riesgo
- Edades extremas, especialmente en menores de cuatro años, y en personas mayores.
- Las mujeres son más vulnerables que los hombres.
- Se ha sugerido aumento de la cardiotoxicidad cuando las antraciclinas se administran con otros agentes, principalmente ciclofosfamida.
- Radioterapia del mediastino y torácica potencia el efecto de los antracíclicos; de ahí el mayor riesgo de cardiotoxicidad.
- El tiempo de infusión menor de una hora esta complicación será frecuente, sobre todo en forma aguda. Se ha observado que el incremento en el tiempo de infusión reduce la incidencia de cardiotoxicidad temprana.
- El riesgo de disfunción cardíaca crónica puede incrementarse en pacientes con antecedentes cardiovasculares e hipertensión arterial, porque desencadena la aparición clínica de enfermedad cardiaca, aun con bajas dosis acumuladas del medicamento.
- La dosis acumulada de antraciclinas es el factor de riesgo más significativo para disfunción cardíaca. La dosis habitual de doxorrubicina es 60-75 mg/m2 cada tres semanas; cuando se rebasa la dosis acumulada de 450- 500 mg/m2 de doxorrubicina el riesgo de cardiopatía e insuficiencia cardíaca congestiva se incrementa. La dosis máxima acumulada para cardiotoxicidad varía según el tipo del antracíclico.
Manifestaciones clínicas
- Taquicardia sinusal
- Taquipnea
- Disnea
- Cardiomegalia
- Edema periférico
- Edema pulmonar
- Hepatomegalia
- Congestión venosa
- Derrame pleural
- Signos de bajo gasto (hipotensión, frialdad de extremidades, mareos)
Otras consideraciones
- Puede presentarse cardiotoxicidad tardía 6 a 20 años después del tratamiento con arritmias graves, incluyendo taquicardias y fibrilaciones ventriculares y bloqueos de segundo y tercer grados.
- La combinación Taxanos con trastuzumab de forma secuencial tras la administración de quimioterapia con régimen de antraciclinas, aumenta el riesgo absoluto de insuficiencia cardíaca congestiva sintomática (grado III/IV de la NYHA) entre el 0.6-4.1% , la cardiotoxicidad asociada a Trastuzumab es reversible, idiosincrática y no se asocia con daño estructural.
Recomendaciones:El mejor tratamiento, es la prevención, la detección precoz que se logra mediante la educación y comunicación.
- Realizar valoración de la función cardíaca previo al inicio de medicamentos cardiotoxicos y un seguimiento posterior de la misma tanto desde el punto de vista clínico como mediante la realización de una ecocardiografía.
- El principal método de prevención es limitar la dosis total acumulada de fármacos cardiotoxicos, mediante una adecuada formulación.
- Alimentación saludable, control de peso, ejercicio en cuanto sea posible
- Control de comorbilidades como la hipertensión arterial, el tabaquismo, la dislipidemia, la obesidad central, el síndrome metabólico y la diabetes.
- Empleo de agentes cardioprotectores reducen la incidencia de daño cardíaco.
- Infusión lenta de los medicamentos
- Ante la aparición de insuficiencia cardíaca congestiva se ha de interrumpir definitivamente el tratamiento.
- Interrumpir temporalmente el tratamiento cuando se detecte un descenso de la fracción de eyección del 15% (respecto a nivel basal previo a inicio del tratamiento) o por debajo del 50%.
- El Trastuzumab puede ser reiniciado a las 4-8 semanas si se comprueba que la FEVI retorna a límites normales y la disminución absoluta respecto a su nivel basal en menor al 15%.
- Hay datos que sugieren que en pacientes con enfermedad metastásica con un descenso significativo de la FEVI, el tratamiento con betabloqueantes o IECAs puede permitir la reintroducción del tratamiento con Trastuzumab, asumiendo por parte de la paciente y del médico responsable el equilibrio riesgo-beneficio
- Realizar seguimiento a los pacientes en tratamiento adyuvante libres de enfermedad, que hayan recibido regímenes con Antraciclinas y Trastuzumab, ya que la cardiotoxicidad puede aparecer a largo plazo.
- El tratamiento farmacológico es el de cualquier insuficiencia cardiaca, con el empleo de fármacos como IECAS (inhibidores de la enzima conversiva de la angiotensina:
enalapril, captopril) , betabloqueantes (carvedilol, metoprolol, bisoprolol) y diuréticos(furosemida, clortalidona, torasemida) e incluso trasplante cardíaco en enfermos refractarios al tratamiento y libres de enfermedad neoplásica.
Toxicidad Pulmonar
Asociada a Bleomicina, Busulfan, BCNU, Mitomicina-C, Ciclofosfamida, Ifosfamida, se denominado Fibrosis Pulmonar, caracterizada por la sustitución progresiva de los alveolos por tejido fribrótico, de forma que se impide el intercambio de oxígeno con el torrente circulatorio, las manifestaciones son: disnea principalmente por esfuerzo, tos seca y crónica, debilidad y fatiga, perdida del apetito, rápida pérdida de peso; el tratamiento, pasa por una correcta prevención, en fases agudas corticoides eficaces, siendo necesaria una supresión paulatina; en los casos con fibrosis pulmonar severa instaurada, el único tratamiento eficaz es el trasplante pulmonar, en los pacientes con neoplasias curadas.
Adicionalmente el Trastuzumab y el Rituximab pueden generar Alveolitis neutrofílica aguda, Neumonía organizada y Distrés respiratorio agudo
Alteraciones Sexuales
Pueden estar asociadas a los tratamientos o pueden tener una influencia psicológica, los problemas que aparecen más frecuentemente son la pérdida del deseo sexual en hombres debido a problemas para alcanzar y mantener una erección, incapacidad para eyacular o eyaculación retrógrada o imposibilidad de alcanzar un orgasmo, en las mujeres por dolor durante el coito, cambios en la sensibilidad genital, capacidad disminuida para llegar al orgasmo.
- Disfunción Gonadal en mujeres:
- Amenorrea transitoria: ausencia de menstruación durante un periodo igual o superior a 6 meses de manera reversible, esta relacionada con: estrés, malnutrición, pérdida de peso, son muchos los quimioterápicos que inducen amenorrea transitoria.
- Amenorrea permanente o menopausia: ausencia de menstruación de manera irreversible, su incidencia aumenta con la edad de la paciente en el momento del tratamiento; y puede ir precedida de una oligomenorrea (ciclos menstruales entre 40 días y 6 meses de duración) con el uso de Melfalán, Clorambucilo, Busulfán, Mitomicina, Cisplatino, Procarbacina, Etopósido; la hormonoterapia (Tamoxifeno, Anastrozol, Letrozol, Exemestano, Goserelina, Leuprolina)
- Disfunción Gonadal en Varones: asociada Clorambucil, Ciclofosfamida, Ifosfamida, Melfalan, Busulfan, BCNU, CCNU, Dacarbazina, Procarbazina, Adriamicina, por la disminución de las células madre germinales, y la inhibición de la maduración de los espermatozoides, pueden ser evidentes desde las primeras semanas, posteriormente aparece atrofia y disminución del tamaño testicular y secundariamente una disminución de la testosterona, la recuperación de la función gonadal suele ocurrir en los tres primeros años del fin del tratamiento, aunque en algunos casos suele ser más prolongada e incluso permanente.
- Disfunción sexual: puede estar asociado a alteraciones hormonales inducidas por los tratamientos, trastornos psicológicos (reacciones de ansiedad y depresión adaptativas a la enfermedad y su tratamiento, pérdida de autoestima), trastornos funcionales relacionados con el deterioro físico. En los varones el problema principal es debido a la disfunción eréctil, secundaria generalmente a los tratamientos quirúrgicos o radioterápicos. Los agentes quimioterápicos ocasionan disfunción sexual secundaria a la aparición de una disfunción gonadal, siendo las manifestaciones principales la reducción de la libido y de la capacidad de alcanzar el orgasmo, la disfunción eréctil, la alteración de la eyaculación y la disminución de la actividad sexual. Todas ellas relacionadas con la disminución de la testosterona. Los tratamientos farmacológicos pueden mejorar la disfunción eréctil, aunque su efectividad es limitada.
En la mujer, los tratamientos quirúrgicos o radioterápicos sobre la zona genital, conllevan disfunciones sexuales importantes y persistentes. Los síntomas más frecuentes son la disminución o ausencia de deseo sexual, sequedad vaginal, dispareunia (dolor vaginal durante la relación sexual), estenosis vaginales, en un porcentaje importante de pacientes diagnosticadas de cáncer de mama, se desarrollan disfunciones sexuales, siendo los factores psicológicos el origen de la mayoría de ellas (reducción del deseo sexual, frigidez). El apoyo psicológico y de las parejas supone la ayuda más importante en la adaptación de las mujeres.
Alteraciones en los órganos de los sentidos
- Conjuntivitis: asociada a Citarabina, 5-FU Aparece por acción directa sobre la conjuntiva ocular, aunque también se ve favorecida por la caída de las pestañas. Cuando se cronifican pueden producir la estenosis (obstrucción) del conducto lacrimal. Se tratan con colirios con corticoides y antiinflamatorios.
- Perdidad de visión: asociada a Cisplatino, BCNU Alteraciones de la agudeza visual, cambios en la percepción de los colores, son las alteraciones que aparecen más frecuentemente.
- Alteraciones auditivas asociadas a Cisplatino Aparece inicialmente pérdida de audición en las frecuencias altas, relacionada con la neurotoxicidad. Es una toxicidad dosis acumulada
- Alteraciones en el gusto y olfato: Se desconocen los mecanismos de producción, siendo trastornos muy frecuentes, relacionados probablemente con la toxicidad sobre las mucosas como por daño nervioso.