Programa de Tecnovigilancia
Regresar al Servicio farmacéutico
Identificación
|
Nombre |
Código |
|||
|
Programa de Tecnovigilancia |
MPF11 | |||
|
Fecha de Emisión |
Fecha de Actualización |
Versión | ||
|
2013/11/19 |
2022/08/31 |
5 | ||
Elaboro:
| Diana Carolina Valbuena |
Químico Farmacéutico de Calidad |
| Lucy Ramirez Londoño |
Coordinadora de Calidad Oncomedic ltda |
Reviso y Autorizo Última Versión: Comité de Farmacia y Terapéutica
Introducción
El programa de tecnovigilancia permite la identificación y la cualificación de eventos adversos e incidentes de seguridad, antes, durante, y después de la atención, asociados con los dispositivos médicos, así como la identificación de los factores de riesgo que contribuyen en su presentación, con base en la notificación, registro y evaluación sistemática, con el fin de determinar la frecuencia, gravedad e incidencia de los mismos para prevenir su aparición.
Política
Oncomedic se compromete a velar por el suministro de insumos medicoquirurgicos y manejo de equipo biomedico en forma segura, eficaz y de calidad, verificando y controlando su correcta gestión desde los procesos de adquisición, recepción, almacenamiento, suministro, uso, segregación y disposición final, con acciones de prevención, educación, control, identificación del riesgo, reporte, estudio y análisis de las reacciones adversas asociados a insumos y equipos biomedicos. Así mismo no está permitido el reuso de insumos dentro de la organización, como estrategia de bioseguridad.
Objetivo
Realizar procesos que permitan la protección de la salud y la seguridad de los pacientes, usuarios y todo aquel que se vea implicado directa o indirectamente con la utilización de dispositivos médicos en la organización de acuerdo a las normas, mecanismos, procesos, recursos financieros, técnicos y de talento humano, mediante la identificación, recolección, evaluación, gestión y divulgación de los eventos o incidentes adversos que presentan los dispositivos médicos durante su uso.
Alcance
El programa de Tecnovigilancia inicia con la adecuada gestión de proveedores, la adquisición, recepción del insumo médico quirúrgico, su óptimo almacenamiento, y distribución, uso idóneo, identificación de los eventos adversos para controlarlas, analizarlas establecer posibles factores causales emprender planes de mejoramiento y realizar lo reporte los organismos de control
Marco Conceptual
Sustento Legal
- Decreto 2200 y resolución 1403 por los que se reglamentan los servicios farmacéuticos, la atención farmacéutica y se describen las reacciones adversas.
- Decreto 4725 de 2005 “Por el cual se reglamenta el régimen de registros sanitarios, permiso de comercialización y vigilancia sanitaria de los dispositivos médicos para uso humano”.
- Resolucióón 2434 de 2006. Reglamenta la importación del equipamiento biomédico
- Decreto 4562 de 2006 (Paragrafo-Art 86) en el que se determina la necesidad de registro sanitario para algunos dispositivos biomedicos.
- Resolución 1403 de 2007: “Por la cual se determina el Modelo de Gestión del Servicio Farmacéutico, se adopta el Manual de Condiciones Esenciales y Procedimientos y se dictan otras disposiciones”.
- Resolución 4816 de 2008, reglamenta el Programa Nacional de Tecnovigilancia. Determina niveles de acción y las responsabilidades para cada uno de los actores.
Resolución 3100 de 2019 del Ministerio de Salud “Por la cual se definen los procedimientos y condiciones de inscripción de los Prestadores de Servicios de Salud y de habilitación de servicios de salud”.
Marco Referencial
Decreto 4725 de 2005 define los dispositivos médicos de uso humano como cualquier instrumento, aparato, máquina, software,equipo biomédico u otro artículo similar o relacionado,utilizado solo o en combinación, incluyendo suscomponentes, partes, accesorios y programas informáticos que intervengan en su correcta aplicación propuesta por el fabricante para su uso, en:
- Diagnóstico, prevención, supervisión, tratamiento o alivio deuna enfermedad.
- Diagnóstico, prevención, supervisión, tratamiento, alivio ocompensación de una lesión o de una deficiencia.
- Investigación, sustitución, modificación o soporte de la estructura anatómica o de un proceso fisiológico.
- Diagnóstico del embarazo y control de la concepción.
- Cuidado durante el embarazo, el nacimiento o después del mismo, incluyendo el cuidado del recién nacido.
- Productos para desinfección y/o esterilización de dispositivosmédicos.
- Los dispositivos médicos para uso humano, no deberán ejercer la acción principal que se desea por medios farmacológicos, inmunológicos o metabólicos
- Equipo Biomedico: Dispositivo Médico operacional y funcional que reúne sistemas y subsistemas eléctricos,electrónicos o hidráulicos, incluidos los programas informáticos que intervengan en su buen funcionamiento, destinado por el fabricante a ser usado en seres humanos con fines de prevención,diagnóstico, tratamiento o rehabilitación, No constituyen equipo biomédico, aquellos dispositivos médicos implantados en el se rhumano o aquellos destinados para un sólo uso.
- Evento adverso: Daño no intencionado al paciente, operador o medio ambiente que ocurre como consecuencia de la utilización de un dispositivo médico.
- Incidente adverso: Daño o potencial riesgo de daño no intencionado al paciente, operador o medio ambiente que ocurre como consecuencia de la utilización de un dispositivo médico.
- Referencia: Variante cualitativa o de diseño de un producto, empleado para un mismo uso y que corresponde a un mismo titular y fabricantes.
.
Clasificación del Riesgo de los dispositivos Médicos: La clasificación de los dispositivos médicos está dada por las Reglas de Clasificación descritas en el ARTÍCULO 7° del decreto 4725 (18 reglas), donde se especifian los criterios de aplicación a los distintos Dispositivos médicos: Invasivos, No invasivos, Dispositivos médicos Activos por ejemplo duración del contacto con el cuerpo, grado de invasión y efecto local contra efecto sistémico etc. y algunas otras reglas especiales.
Oncomedic Ltda. Tiene clasificado su listado de Dispositivos Médicos segun el riesgo potencial relacionado con el uso de los mismos.
- Clase I: Son aquellos dispositivos médicos de bajo riesgo, sujetos a controles generales, no destinados para proteger o mantener la vida o para un uso de importancia especial en la prevención del deterioro de la salud humana y que no representan un riesgo potencial no razonable de enfermedad o lesión.
- Clase II a: Son los dispositivos médicos de riesgo moderado, sujetos a controles especiales en la fase de fabricación para demostrar su seguridad y efectividad.
- Clase II b: Son los dispositivos médicos de riesgo alto, sujetos a controles especiales en el diseeño y fabricación para demostrar su seguridad y efectividad
- Clase III: Son los dispositivos médicos de muy alto riesgo sujetos a controles especiales, destinados a proteger o mantener la vida o para un uso de importancia sustancial en la prevención del deterioro de la salud humana, o si su uso presenta un riesgo potencial de enfermedad o lesión.
Metodologia de Diseño e Implementación del Programa
Compromiso de la Dirección
La Gerencia de Oncomedic ltda y todos sus funcionarios se comprometen a velar por el suministro de insumos medico-quirurgicos y manejo de equipo biomedico en forma segura, eficaz y de calidad, verificando y controlando su correcta gestión desde los procesos de adquisición, recepción, adecuación, dispensación, con acciones de prevención, educación, control, identificación, reporte, estudio y análisis de las reacciones adversas asociados a dispositivos y equipos biomedicos.
Diagnóstico y Autoevaluación Organizacional
Los dispositivos médicos se pueden clasificar segun la siguiente tipología:
- Consumibles
- Sobre medida
- Equipos biomédicos.
Dentro de oncomedic ltdas se usan dispositivos médicos consumibles y equipos biomedicos.
| Clasificación de los Dispositivos Médicos Oncomedic | ||||||||
| TIPO DE RIESGO | ||||||||
| No. | ID PRODUCTO | CUM | PRODUCTO | Riesgo Bajo | Riesgo Moderado | Riesgo Alto | Riesgo Muy alto | CLASE |
| 1 | 163146 | 20013591-0 | AGUJA HIPODERMICA DESECHABLE ESTERIL N0. 18 | X | IIB | |||
| 2 | 163155 | 34201-0 | AGUJA HIPODERMICA DESECHABLE ESTERIL N0. 26 | X | IIB | |||
| 3 | 163333 | 19954692-0 | AGUJAS HIPODERMICAS NIPRO NIPRO MEDICAL CORPORATION | X | IIB | |||
| 4 | 163377 | 19996994-0 | ALGODON EN POMOS MK TECNOQUIMICAS S.A. | X | I | |||
| 5 | 163343 | 20023803-0 | APLICADORES DE MADERA CON ALGODON | X | IIA | |||
| 6 | 163335 | 0-0 | BAJALENGUAS DE MADERA | X | IIA | |||
| 7 | 163194 | 19960796-0 | CATETER INTRAVENOSO No 16 | X | IIB | |||
| 8 | 163306 | 0-0 | CATETER INTRAVENOSO No 24 | X | IIB | |||
| 9 | 163251 | 0-0 | CONTENEDOR DE MATERIAL CORTOPUNZANTE 2,9 LITROS | X | I | |||
| 10 | 163344 | 20044384-0 | EQUIPO BURETA DE 150 ML | X | IIB | |||
| 11 | 163202 | 19926445-0 | EQUIPO PARA ADMINISTRACION DE SOLUCIONES (BOMBA INFUSION) | X | IIB | |||
| 12 | 163316 | 19926445-0 | EQUIPO PARA INFUSION DE SOLUCION MICROGOTEO | X | IIB | |||
| 13 | 163287 | 20027153-0 | EQUIPO PARA VENOCLISIS O SET DE INFUSION PARA MICRO Y MACROGOTEO. | X | IIB | |||
| 14 | 163273 | 19977483-0 | ESPARADRAPO CUREBAND MICROPOROSO ADHESIVOS | X | I | |||
| 15 | 163185 | 0-0 | ESPECULO VAGINAL DESECHABLE INTERNACIONAL DE PLASTICOS S.A. | X | IIA | |||
| 16 | 163340 | 19969312-0 | FREKA MIX BOLSAS X 150 ML FRESENIUS A.G. | X | IIA | |||
| 17 | 163346 | 19969315-0 | FREKA MIX BOLSAS X 2000 ML FRESENIUS A.G. | X | IIA | |||
| 18 | 163342 | 19969315-0 | FREKA MIX BOLSAS X 250 ML FRESENIUS A.G. | X | IIA | |||
| 19 | 163347 | 19969315-0 | FREKA MIX BOLSAS X 3000 ML FRESENIUS A.G. | X | IIA | |||
| 20 | 163341 | 19969315-0 | FREKA MIX BOLSAS X 500 ML FRESENIUS A.G. | X | IIA | |||
| 21 | 163113 | 20012566-0 | GASA ANTIADHERENTE-CUREBAND | X | I | |||
| 22 | 163354 | 19983812-0 | GASA NO TEJIDA LIFE CARE SOLUTIONS | X | I | |||
| 23 | 163323 | 0-0 | GUANTES PARA CIRUGIA ESTERIL No 6.5 PROTEX S.A. | X | IIA | |||
| 24 | 163362 | 20014194-0 | GUANTES PARA CIRUGIA ESTERIL No 7.0 PROTEX S.A. | X | IIA | |||
| 25 | 163321 | 19996089-0 | GUANTES PARA CIRUGIA ESTERIL No 7.5 PROTEX S.A. | X | IIA | |||
| 26 | 163353 | 19926430-0 | GUANTES PARA CIRUGIA ESTERIL No 8.0 PROTEX S.A. | X | IIA | |||
| 27 | 163198 | 0-0 | GUANTES PARA CIRUGIA ESTERIL No 8.5 PROTEX S.A. | X | IIA | |||
| 28 | 163182 | 19918065-0 | GUANTES PARA EXAMEN TALLA S ETERNA S.A. | X | IIA | |||
| 29 | 163190 | 20032337-0 | GUANTES PARA EXAMEN TALLA M ETERNA S.A. | X | IIA | |||
| 30 | 163358 | 0-0 | GUANTES PARA EXAMEN TALLA L ETERNA S.A. | X | IIA | |||
| 31 | 163121 | 19931807-0 | JERINGA DESECHABLE No 1ML ETERNA S.A. | X | IIB | |||
| 32 | 163117 | 19931807-0 | JERINGA DESECHABLE No 2 ML ETERNA S.A. | X | IIB | |||
| 33 | 163117 | 19931807-0 | JERINGA DESECHABLE No 5 ML ETERNA S.A. | X | IIB | |||
| 34 | 163117 | 19931807-0 | JERINGA DESECHABLE No 10ML ETERNA S.A. | X | IIB | |||
| 35 | 163117 | 19931807-0 | JERINGA DESECHABLE No 20ML ETERNA S.A. | X | IIB | |||
| 36 | 163117 | 19931807-0 | JERINGA DESECHABLE No 50ML ETERNA S.A. | X | IIB | |||
| 37 | 163120 | 19931807-0 | JERINGA DESECHABLE No 60ML ETERNA S.A. | X | IIB | |||
| 38 | 163262 | 0-0 | POLAINAS QUIRURGICAS NO ESTERILES MEDISPO - PROTEX | X | I | |||
| 39 | 163218 | 20014685-0 | SET DE ADMINISTRACION IV CON FILTRO DE 0.22 MICRAS | X | IIB | |||
| 40 | 163221 | 20003020-0 | TAPABOCAS DESECHABLES NONWOVEN FACE | X | I | |||
| 41 | GORROS DESECHABLES | X | I | |||||
| 42 | SEDA 3-0 | X | IIA | |||||
| 43 | AGUJA SPINOCATH N° 18 | X | IIB | |||||
| 44 | AGUJA SURECAM GRIPPERPLUS N° 20G | X | IIB | |||||
Los equipos biomedicos estan descritos en el manual Gestión de Equipos
Organización del Programa
Coordinación del Programa y Funciones del Coordinador
El coordinador del programa de tecnovigilancia es el químico farmacéutico encargado de:
- Liderar los procesos y gestión de los insumos y equipos al interior de la organización.
- Motivar la adecuada gestión de los recursos por parte de los proveedores.
- Incentivar una cultura del reporte y la notificación de eventos adversos generados por los insumos en la organización.
- Realizar la debida gestión de los incidentes y reacciones adversas asociadas con el uso de Dispositivos biomedicos.
- Elaboración y/o revisión de informes periódicos de seguridad del uso de insumos dentro de oncomedic ltda y de ser necesario las demás instituciones contratantes.
- Revisión periódica de la literatura científica sobre reacciones adversas espontáneas a los insumos usados en la organización.
- Realizar informes a los organismos de control frente a los temas de seguridad de medicamentos.
Estrategias, Acciones y Responsable
- Recepción de Medicamentos y Dispositivos Médicos
- Recepcion de Medicamentos y Dispositivos medicosAlmacenamiento de Medicamentos y Dispositivos Medicos
- Análisis de Desviaciones de la Calidad Esperada y la Calidad Observada
- Análisis de Desviaciones de la Calidad Esperada y la Calidad ObservadaBusquedas Activas que permitan verificar el desempeño, calidad y seguridad de los dispositivos médicos previos a su uso .
- Información , divulgación y aplicación prácticas adecuadas en el uso de dispositivos médicos.
- Busquedas Pasivas: Identificar, gestionar e informar de los eventos e incidentes adversos que puedan causar los dispositivos médicos .
- Tomar acciones preventivas o correctivas del caso y las que sean exigidas por el INVIMA.
- Comunicar al fabricante o importador la ocurrencia de un evento o incidente adverso.
- Desarrollar actividades de promoción de calidad con los proveedores y usuarios de los servicios.
- Cooperar y responder cualquier petición del INVIMA sobre la seguridad de los dispositivos médicos. (Artículo 9° Resolución 4816 de 2008).
Reporte interno de incidentes o eventos adversos relacionados con dispositivos médicos.
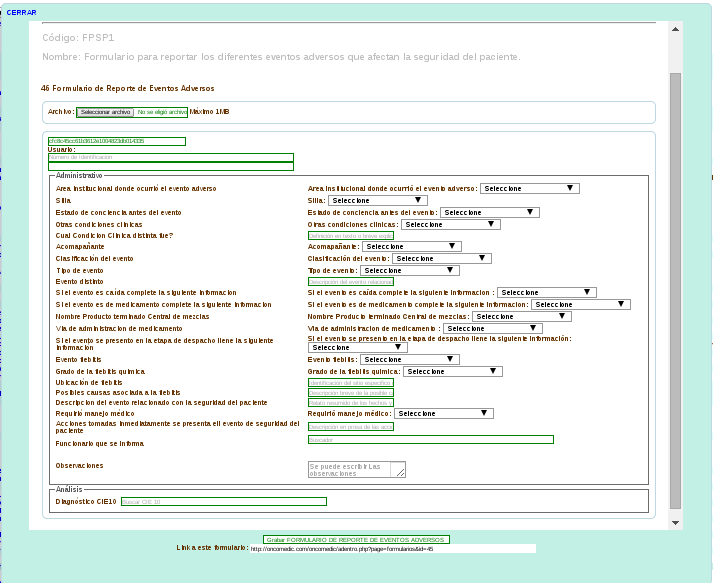
Cuando se detecta un incidente adverso a un dispositivo médico este es registrado en el Formulario de Eventos Adversos (Número 45 en el sistema Oncolinux 2). Cabe aclarar que este formulario es usado para reportar cualquier evento relacionado con la seguridad del paciente y no es exclusivo para el reporte de eventos relacionados con dispositivos médicos.
Instrucciones para llenar el formulario en caso de un evento o incidente relacionado con dispositivos médicos:
Los campos obligatorios a llenar son:
- Usuario: Se selecciona al paciente por su nombre o número de documento.
- Área institucional donde ocurrió el evento adverso: Aquí se selecciona el área de oncomedic donde sucedió el caso.
- Clasificación del evento: Se especifica si el caso corresponde a un evento o a un incidente.
- Tipo de evento: Se selecciona el tipo de evento. Los casos pertinentes para el programa de tecnovigilancia son en los que se seleccione “equipo médico/tecnología”, u “otros” siempre y cuando se especifique otro tipo de dispositivo médico en la casilla “Evento distinto”.
- Evento distinto: Se llena cuando el evento no está en las opciones desplegadas en la casilla “tipo de evento”, describiendo de forma breve el tipo de evento.
- Funcionario que se informa: Aquí se selecciona al responsable del programa de tecnovigilancia de Oncomedic Ltda. por su nombre o número de documento.
- Observaciones: Aquí se deberá hacer una descripción detallada del caso, de forma tal que permita su análisis posterior. De esta manera el reportante deberá incluir tantos detalles como le sea posible. Esto puede incluir información adicional del estado de salud del paciente, hora y fecha del evento seguimiento de protocolos, información del dispositivo que permita su identificación y trazabilidad, tales como número de lote, serial, modelo, registro invima, fabricante, fecha de vencimiento o número de reusos.
Recomendaciones adicionales:
- Si en el evento o incidente adverso se encuentra involucrado más de un (1) dispositivo médico sospechoso, diligencie un formulario por cada uno de ellos, identificando como dispositivo 1, dispositivo 2 etc.
- Al diligenciar el campo observaciones, incluya datos completos, dado que la carencia de datos como el número de Registro Sanitario, lote, modelo, referencia o serial del dispositivo médico, no permitirá iniciar la investigación.
- Si el dispositivo no tiene riesgo de contaminación, se debe entregar al servicio farmacéutico el cual lo pondrá en cuarentena por el tiempo necesario para realizar el análisis del caso. Si el proveedor realiza la reposición del dispositivo, o si es necesario realizar el desecho de este, se tomarán fotografías las cuales se adjuntarán al formulario como evidencia.
- En el caso de que el dispositivo tenga riesgo de contaminación, se procederá a tomar fotografías cuando sea posible, las cuales se adjuntarán como evidencia al formulario, y finalmente se procederá a la disposición final siguiendo los protocolos respectivos de manejo de residuos hospitalarios.
Cabe resaltar que en nuestra organización es posible realizar trazabilidad de todos los dispositivos médicos que son ingresados al inventario mediante la herramienta del código QR que nos permite identificarlos y obtener la información técnica y administrativa pertinente para realizar cualquier tipo de verificación, inspección o recogida de producto.
Análisis de los incidentes o eventos adversos relacionados con dispositivos médicos.
El responsable del programa de tecnovigilancia realizará el análisis y el seguimiento de los casos proponiendo acciones de mejora que prevengan la ocurrencia de eventos o incidentes relacionados con dispositivos médicos. Para esto, se analizarán los casos mediante el protocolo de Londres. Adicional a esto, se puede realizar un análisis de riesgo de los dispositivos médicos utilizados en Oncomedic mediante un análisis modal de falla efecto (AMFE), de esta manera identificando aquellos dispositivos críticos con el objetivo de priorizar la realización de planes de gestión de riesgos.
Reporte de incidentes o eventos adversos relacionados con dispositivos médicos a entidades externas.
El responsable del programa de tecnovigilancia, clasificará, analizará y finalmente reportará los casos enviando el formulario al INVIMA en caso de presentarse un evento o incidente adverso SERIO, dentro de las setenta y dos horas (72) siguientes al conocimiento de la ocurrencia del mismo. Si el caso corresponde a un evento adverso NO SERIO, debe remitir el consolidado trimestralmente en el formulario electrónico RETIPS003 a la Secretaría de salud del Tolima, en los tiempos establecidos en el documento “Informes a organismos de control”
Resultado Esperado, Indicadores y Metas
El programa de tecnovigilancia busca reducir la ocurrencia y severidad de los eventos adversos generados por dispositivos biomedicos
- (No..Incidentes o eventos Adversos gestionados / incidentes adversos reportados)x100
- (No. Reportes al laboratorio fabricante y/oProveedor /No. de incidentes presentados con un Dispositivo médico)x100
- (No. Reporte al INVIMA/No. De incidentes presentados con un Dispositivo médico)x100
- (No. de planes de gestión de riesgo/No de dispositivos con un riesgo alto)x100
Las metas de cumplimiento para los indicadores anteriormente descritos serian del 100%
Tiempo de Ejecución y Fecha de Revisión del Programa
El programa de farmacovigilancia es un programa permanente que se evalua mensualmente en el comite de farmacia y terapeutica y anualmente en el comite de calidad donde presenta los resultados obtenidos y las nuevas metas