Programa de Tecnovigilancia
Regresar a la Página principal
Regresar al Servicio farmacéutico
Identificación
|
Nombre |
Código |
|||
|
Programa de Tecnovigilancia |
MPF11 | |||
|
Fecha de Emisión |
Fecha de Actualización |
Versión | ||
|
2013/11/19 |
2022/08/31 |
5 | ||
Elaboro:
| Diana Carolina Valbuena |
Químico Farmacéutico de Calidad |
| Lucy Ramirez Londoño |
Coordinadora de Calidad Oncomedic ltda |
Reviso y Autorizo Última Versión: Comité de Farmacia y Terapéutica
Introducción
Se define como el conjunto de actividades que tienen por objeto la identificación y la cualificación de eventos e incidentes adversos serios e indeseados producidos asociados con los dispositivos médicos, así como la identificación de los factores de riesgo asociados a estos, con base en la notificación, registro y evaluación sistemática, con el fin de determinar la frecuencia, gravedad e incidencia de los mismos para prevenir su aparición.
La Tecnovigilancia debe ayudar a la identificación, prevención y resolución de los eventos o incidentes relacionados con el uso de los Dispositivos Médicos por medio de la evaluación de la causalidad y la gestión del riesgo con el fin de disminuir la carga de morbi-mortalidad.
El Programa Nacional de Tecnovigilancia se configura como un sistema de vigilancia post-mercado, constituido por el conjunto de instituciones, normas, mecanismos, procesos, recursos financieros, técnicos y de talento humano que interactúan para la identificación, recolección, evaluación, gestión y divulgación de los eventos o incidentes adversos no descritos que presentan los dispositivos médicos durante su uso, la cuantificación del riesgo y la realización de medidas en salud pública, con el fin de mejorar la protección de la salud y la seguridad de los pacientes, usuarios y todo aquel que se vea implicado directa o indirectamente con la utilización del dispositivo.
Política
Oncomedic se compromete a garantizar el suministro seguro, eficaz y de calidad de los insumos médicoquirúrgicos y el manejo responsable de los equipos biomédicos, en cumplimiento con los lineamientos del Programa Nacional de Tecnovigilancia liderado por el INVIMA.
Para ello, se implementan mecanismos de verificación y control en todas las etapas del ciclo de vida de los dispositivos médicos e insumos: adquisición, recepción, almacenamiento, distribución, uso, mantenimiento, segregación y disposición final, asegurando su trazabilidad y conformidad regulatoria.
Como parte integral de esta política, la organización promueve:
- Acciones de prevención, educación y control del riesgo.
- La identificación, reporte, estudio y análisis de eventos e incidentes adversos asociados a dispositivos médicos, insumos y equipos biomédicos, conforme a la normatividad vigente.
- La adopción de una cultura institucional de tecnovigilancia que favorezca la seguridad del paciente, del usuario y del entorno hospitalario.
En el marco de las buenas prácticas clínicas y de bioseguridad, queda estrictamente prohibido el reuso de insumos médicoquirúrgicos de un solo uso, salvo en los casos autorizados por normatividad específica.
Objetivos
Objetivo General
Implementar y mantener un sistema institucional de tecnovigilancia que permita la identificación, evaluación, gestión y notificación oportuna de incidentes y eventos adversos asociados al uso de dispositivos médicos, insumos médicoquirúrgicos y equipos biomédicos, con el fin de prevenir riesgos, proteger la seguridad del paciente y cumplir con los lineamientos del Programa Nacional de Tecnovigilancia del INVIMA.
Objetivos Específicos
- Establecer mecanismos de detección, notificación y análisis de eventos adversos e incidentes relacionados con dispositivos médicos, garantizando su trazabilidad y seguimiento.
- Promover una cultura de seguridad y tecnovigilancia entre los colaboradores mediante procesos permanentes de sensibilización, educación y formación.
- Implementar procedimientos internos para la gestión integral de riesgos asociados a insumos y equipos biomédicos, desde su adquisición hasta su disposición final.
- Asegurar la correcta documentación, reporte y comunicación de eventos al INVIMA, cumpliendo con los requisitos técnicos y legales establecidos.
- Ejecutar acciones correctivas, preventivas y de mejora continua derivadas del análisis de los reportes, que contribuyan a la reducción de fallas y la mejora de la calidad en la atención.
- Garantizar el uso seguro, eficaz y conforme a la normativa de todos los dispositivos médicos e insumos médicoquirúrgicos utilizados en la institución.
- Mantener actualizada la información técnica y regulatoria de los dispositivos médicos, incluyendo su registro sanitario, condiciones de uso y alertas sanitarias vigentes.
Alcance
El programa de Tecnovigilancia inicia con la adecuada gestión de proveedores, la adquisición, recepción del insumo médico quirúrgico, su óptimo almacenamiento, y distribución, uso idóneo, identificación de los eventos adversos para controlarlas, analizarlas establecer posibles factores causales emprender planes de mejoramiento y realizar lo reporte los organismos de control
Marco Conceptual
Sustento Legal
- Decreto 2200 y resolución 1403 por los que se reglamentan los servicios farmacéuticos, la atención farmacéutica y se describen las reacciones adversas.
- Decreto 4725 de 2005 “Por el cual se reglamenta el régimen de registros sanitarios, permiso de comercialización y vigilancia sanitaria de los dispositivos médicos para uso humano”.
- Decreto 4562 de 26 Diciembre 2006. por el cual se adiciona un parágrafo al artículo 86 del Decreto 4725 de 2005.
- Decreto 3275 de 31 Agosto 2009. Por el cual se modifica el artículo 1º y se adiciona un parágrafo al artículo 18 del Decreto 4725 de 2005.
- Resolución 1403 de 2007: “Por la cual se determina el Modelo de Gestión del Servicio Farmacéutico, se adopta el Manual de Condiciones Esenciales y Procedimientos y se dictan otras disposiciones”.
- Resolución 4816 de 2008, reglamenta el Programa Nacional de Tecnovigilancia. Determina niveles de acción y las responsabilidades para cada uno de los actores.
- Decreto 0582 de 4 de Abril de 2017. Por el cual se modifica el Decreto 4725 de 2005 y se dictan otras disposiciones.
- Resolución 3100 de 2019 del Ministerio de Salud “Por la cual se definen los procedimientos y condiciones de inscripción de los Prestadores de Servicios de Salud y de habilitación de servicios de salud”.
Marco Referencial
Decreto 4725 de 2005 define los dispositivos médicos de uso humano como cualquier instrumento, aparato, máquina, software,equipo biomédico u otro artículo similar o relacionado,utilizado solo o en combinación, incluyendo suscomponentes, partes, accesorios y programas informáticos que intervengan en su correcta aplicación propuesta por el fabricante para su uso, en:
- Diagnóstico, prevención, supervisión, tratamiento o alivio de una enfermedad.
- Diagnóstico, prevención, supervisión, tratamiento, alivio o compensación de una lesión o de una deficiencia.
- Investigación, sustitución, modificación o soporte de la estructura anatómica o de un proceso fisiológico.
- Diagnóstico del embarazo y control de la concepción.
- Cuidado durante el embarazo, el nacimiento o después del mismo, incluyendo el cuidado del recién nacido.
- Productos para desinfección y/o esterilización de dispositivos médicos.
- Los dispositivos médicos para uso humano, no deberán ejercer la acción principal que se desea por medios farmacológicos, inmunológicos o metabólicos
- Equipo Biomédico: Dispositivo Médico operacional y funcional que reúne sistemas y subsistemas eléctricos,electrónicos o hidráulicos, incluidos los programas informáticos que intervengan en su buen funcionamiento, destinado por el fabricante a ser usado en seres humanos con fines de prevención,diagnóstico, tratamiento o rehabilitación, No constituyen equipo biomédico, aquellos dispositivos médicos implantados en el ser humano o aquellos destinados para un sólo uso.
- Evento adverso: Daño no intencionado al paciente, operador o medio ambiente que ocurre como consecuencia de la utilización de un dispositivo médico.
- Incidente adverso: Daño o potencial riesgo de daño no intencionado al paciente, operador o medio ambiente que ocurre como consecuencia de la utilización de un dispositivo médico.
- Referencia: Variante cualitativa o de diseño de un producto, empleado para un mismo uso y que corresponde a un mismo titular y fabricantes.
Clasificación del Riesgo de los dispositivos Médicos: La clasificación de los dispositivos médicos está dada por las Reglas de Clasificación descritas en el ARTÍCULO 7° del decreto 4725 (18 reglas), donde se especifican los criterios de aplicación a los distintos Dispositivos médicos: Invasivos, No invasivos, Dispositivos médicos Activos por ejemplo duración del contacto con el cuerpo, grado de invasión y efecto local contra efecto sistémico etc. y algunas otras reglas especiales.
Oncomedic Ltda. Tiene clasificado su listado de Dispositivos Médicos según el riesgo potencial relacionado con el uso de los mismos.
- Clase I: Son aquellos dispositivos médicos de bajo riesgo, sujetos a controles generales, no destinados para proteger o mantener la vida o para un uso de importancia especial en la prevención del deterioro de la salud humana y que no representan un riesgo potencial no razonable de enfermedad o lesión.
- Clase II a: Son los dispositivos médicos de riesgo moderado, sujetos a controles especiales en la fase de fabricación para demostrar su seguridad y efectividad.
- Clase II b: Son los dispositivos médicos de riesgo alto, sujetos a controles especiales en el diseño y fabricación para demostrar su seguridad y efectividad
- Clase III: Son los dispositivos médicos de muy alto riesgo sujetos a controles especiales, destinados a proteger o mantener la vida o para un uso de importancia sustancial en la prevención del deterioro de la salud humana, o si su uso presenta un riesgo potencial de enfermedad o lesión.
Metodología de Diseño e Implementación del Programa
Compromiso de la Dirección
La Gerencia de Oncomedic ltda y todos sus funcionarios se comprometen a velar por el suministro de insumos medico-quirúrgicos y manejo de equipo biomédico en forma segura, eficaz y de calidad, verificando y controlando su correcta gestión desde los procesos de adquisición, recepción, adecuación, dispensación, con acciones de prevención, educación, control, identificación, reporte, estudio y análisis de las reacciones adversas asociados a dispositivos y equipos biomédicos.
Diagnóstico y Autoevaluación Organizacional
Los dispositivos médicos se pueden clasificar según la siguiente tipología:
- Consumibles
- Sobre medida
- Equipos biomédicos.
https://docs.google.com/spreadsheets/d/1o9IfaJHI8qRWXTYTAeYEFdKsQ0Y_Chg2/edit?gid=1064220475#gid=1064220475 Listado de Suficiencia de Dispositivos Médicos y Equipos Biomédicos
Clasificación del Riesgo de Equipos Biomedicos
| Equipo | Clasificación del Riesgo | Equipo |
Clasificación del riesgo | Equipo |
Clasificación del Riesgo |
| Adaptador /soporte de tubo para recolección de sangre |
I |
Catéter nasofaríngeo |
IIB |
Equipo de infusión (Venoclisis)para usarse con bomba para solución enteral |
IIB |
| Adaptadores (sitios de inyección) |
IIB |
Catéter venoso central multilumen (duo) |
IIB |
Equipo para infusión (Venoclisis) |
IIB |
| Aguja hipodérmica |
IIB |
Catéter venoso central multilumen (mono) |
IIB |
Equipo para infusión gran volumen |
I |
| Agujas para biopsia |
IIB |
Catéter venoso central multilumen (trio) |
IIB |
Esponja de gasa esteril |
IIB |
| Algodones en láminas |
I |
Catéter venoso subcutáneo implantable |
III |
Esponja quirúrgica |
IIB |
| Baja lengua |
I |
Catéter ventricular |
III |
Guantes de exploración de látex estériles |
III |
| Bloque para evitar mordida |
I |
Cinta adhesiva quirúrgica |
I |
Guantes de exploración no estériles |
IIA |
| Bolsa para agua fría o caliente |
I |
Contenedores de material punzocortantes |
I |
Guantes quirúrgicos |
IIA |
| Caja contenedora incinerable para jeringas |
I |
Equipo de infusión (Venoclisis) para usarse con bomba en volúmenes medidos | IIB | Hojas para bisturí |
IIA |
| Cánula nasal para oxígeno |
I |
Equipo de infusión (Venoclisis) para usarse con bomba para soluciones de sangre |
IIB |
Jeringa con o sin aguja hipodérmica |
III |
| Jeringa émbolo |
I |
Jeringa irrigadora |
IIB |
Lubricante para paciente |
IIB |
| Ropa de cama desechable |
IIA |
Ropa quirúrgica |
IIA |
Soluciones higiénicas para desinfección de instrumental quirúrgico |
IIB |
| Soluciones para desinfección de manos |
III |
Sonda nasofaríngea |
IIB |
Sonda orofaríngea |
IIB |
| Tubo para traqueostomía |
IIB |
Tubo traqueal o endotraqueal |
IIB |
Venda elástica |
IIB |
Los equipos biomédicos están descritos en el manual Gestión de Equipos
Organización del Programa
Coordinación del Programa y Funciones del Coordinador
El coordinador del programa de tecnovigilancia es el químico farmacéutico encargado de:
- Liderar los procesos y gestión de los insumos y equipos al interior de la organización.
- Motivar la adecuada gestión de los recursos por parte de los proveedores.
- Incentivar una cultura del reporte y la notificación de eventos adversos generados por los insumos en la organización.
- Realizar la debida gestión de los incidentes y reacciones adversas asociadas con el uso de Dispositivos biomedicos.
- Elaboración y/o revisión de informes periódicos de seguridad del uso de insumos dentro de oncomedic ltda y de ser necesario las demás instituciones contratantes.
- Revisión periódica de la literatura científica sobre reacciones adversas espontáneas a los insumos usados en la organización.
- Realizar informes a los organismos de control frente a los temas de seguridad de medicamentos.
Estrategias, Acciones y Responsable
- Recepción de Medicamentos y Dispositivos Médicos
- Almacenamiento de Medicamentos y Dispositivos Médicos
- Análisis de Desviaciones de la Calidad Esperada y la Calidad Observada
- Procedimiento de reuso de dispositivos médicos
- Búsquedas Activas que permitan verificar el desempeño, calidad y seguridad de los dispositivos médicos previos a su uso .
- Información , divulgación y aplicación prácticas adecuadas en el uso de dispositivos médicos.
- Búsquedas Pasivas: Identificar, gestionar e informar de los eventos e incidentes adversos que puedan causar los dispositivos médicos .
- Tomar acciones preventivas o correctivas del caso y las que sean exigidas por el INVIMA.
- Comunicar al fabricante o importador la ocurrencia de un evento o incidente adverso.
- Desarrollar actividades de promoción de calidad con los proveedores y usuarios de los servicios.
- Cooperar y responder cualquier petición del INVIMA sobre la seguridad de los dispositivos médicos. (Artículo 9° Resolución 4816 de 2008).
Procedimiento de reuso de dispositivos médicos
- Objetivo
Establecer los lineamientos que garanticen el cumplimiento del no reuso de dispositivos médicos cuando el fabricante así lo haya establecido, asegurando la seguridad del paciente y el cumplimiento normativo, conforme a lo estipulado en la Resolución 3100 de 2019.
- Alcance
Este procedimiento aplica a todos los dispositivos médicos adquiridos, almacenados,utilizados y/o procesados en Oncomedic Ltda, así como a las áreas responsables de su recepción técnica, uso y disposición final.
- Definiciones
- Dispositivo médico de un solo uso: Producto que, según el fabricante, debe ser utilizado una única vez y luego descartado.
- Dispositivo médico de reuso: Producto que, según el fabricante, puede reutilizarse bajo condiciones específicas de reprocesamiento y esterilización.
- Recepción técnica: Proceso mediante el cual se verifica que los dispositivos médicos recibidos cumplan con las especificaciones técnicas, condiciones de almacenamiento y rotulado establecidas por el fabricante.
- Responsables durante el procedimiento
- Director técnico del servicio de farmacia: Verificar las instrucciones del fabricante al momento de la recepción técnica y clasificar los dispositivos según su posibilidad o no de reuso.
- Servicio asistencial: Utilizar los dispositivos conforme a la indicación del fabricante.
- Proveedor de esterilización: Garantizar la trazabilidad y esterilización adecuada de los dispositivos médicos de reuso autorizados.
- Desarrollo del procedimiento
- Recepción técnica de dispositivos médicos
- Durante la recepción técnica, se revisa que cada dispositivo médico cuente con Información que indique si es de un solo uso.
- En caso que el fabricante indique “Solo un uso” o/y “No reutilizar”, el dispositivo se clasifica como de uso único y se prohíbe su reuso.
- Se registra la condición de reuso en el formato de control de dispositivos médicos y se informa al personal.
- Disposición final de dispositivos de un solo uso
- Una vez utilizado, el dispositivo debe ser descartado en los recipientes definidos para residuos cortopunzantes o infecciosos, según corresponda.
- No está permitido realizar ningún tipo de reprocesamiento, lavado o esterilización de dispositivos de un solo uso.
- Excepciones autorizadas
- Hojas de laringoscopio
Actualmente, en Oncomedic Ltda, el único dispositivo médico autorizado para reuso es la hoja de laringoscopio. El fabricante permite su reuso únicamente bajo condición de esterilización posterior a cada uso. - Las hojas de laringoscopio se recogen en contenedores marcados y se envían al proveedor externo autorizado para su esterilización.
- El proveedor entrega soporte de cada ciclo de esterilización y estos registros son archivados por el área de calidad.
- Hojas de laringoscopio
- Supervisión y cumplimiento
- El área de calidad realiza auditorías periódicas para verificar el cumplimiento del no reuso en servicios asistenciales.
- Cualquier hallazgo de reuso indebido será tratado como evento adverso y se iniciará el análisis respectivo.
- Registros asociados
- Formato de recepción técnica de dispositivos médicos
- Registro de dispositivos de un solo uso
- Trazabilidad de esterilización de hojas de laringoscopio
- Informe de auditoría interna
- Referencias normativas
- Resolución 3100 de 2019 – Habilitación de servicios de salud
- Buenas Prácticas de Manufactura y Uso de Dispositivos Médicos
- Manual del fabricante
- Recepción técnica de dispositivos médicos
Reporte interno de incidentes o eventos adversos relacionados con dispositivos médicos.
Cuando se detecta un incidente adverso a un dispositivo médico este es registrado en el Formulario de “acciones inseguras” de VISOF. Cabe aclarar que este formulario es usado para reportar cualquier evento relacionado con la seguridad del paciente y no es exclusivo para el reporte de eventos relacionados con dispositivos médicos.
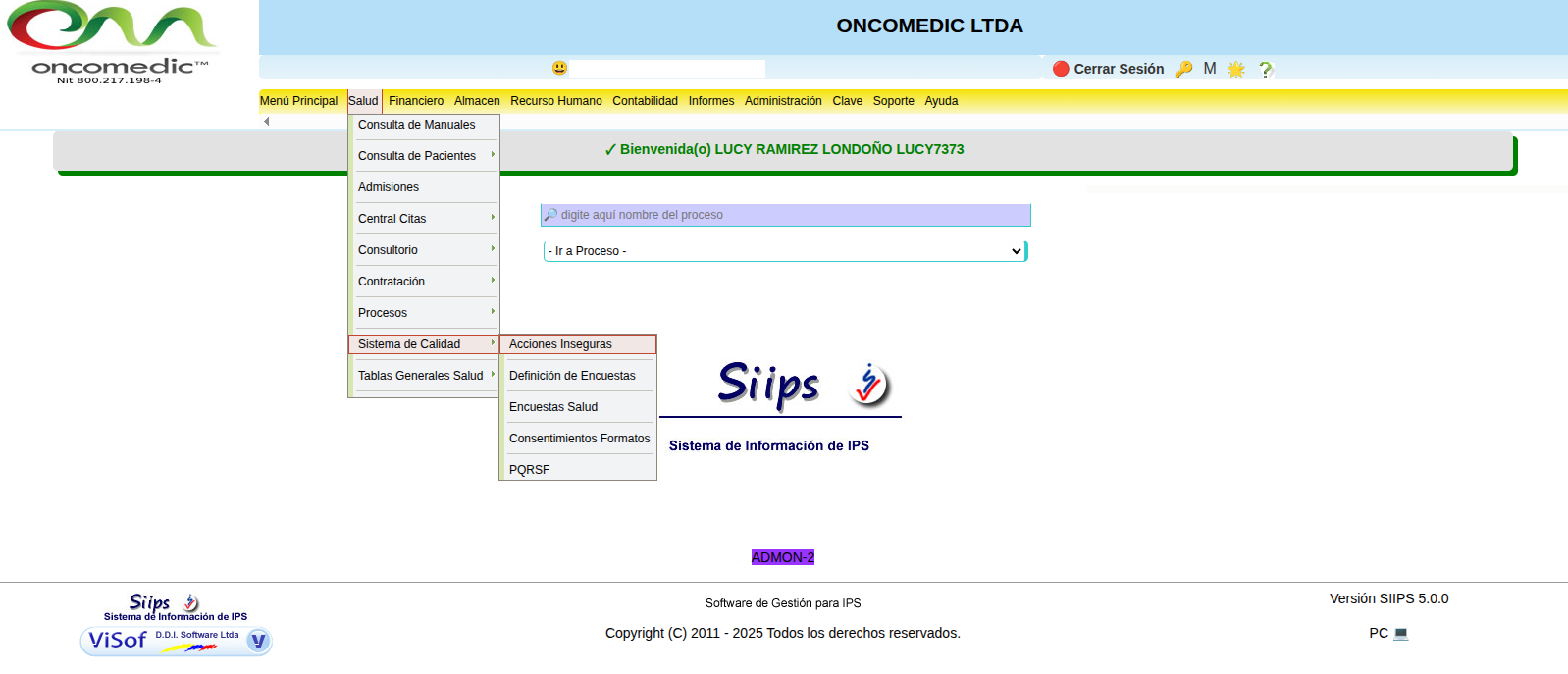
- Desde la ruta SALUD-SISTEMA DE CALIDAD-ACCIONES INSEGURAS.
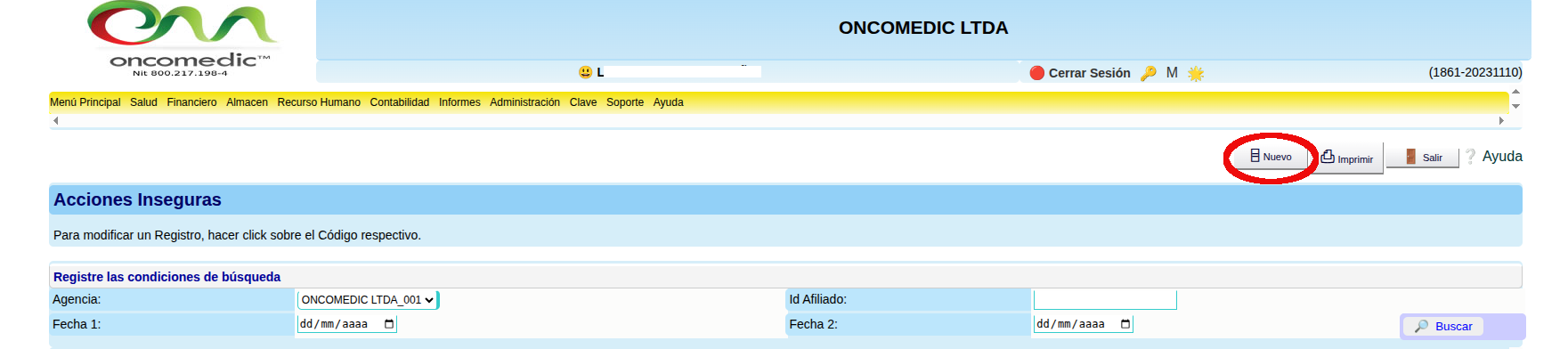
- Seleccionar el botón “nuevo” para generar el reporte del evento.
- Diligenciar el formato con la información del paciente y la descripción del evento.
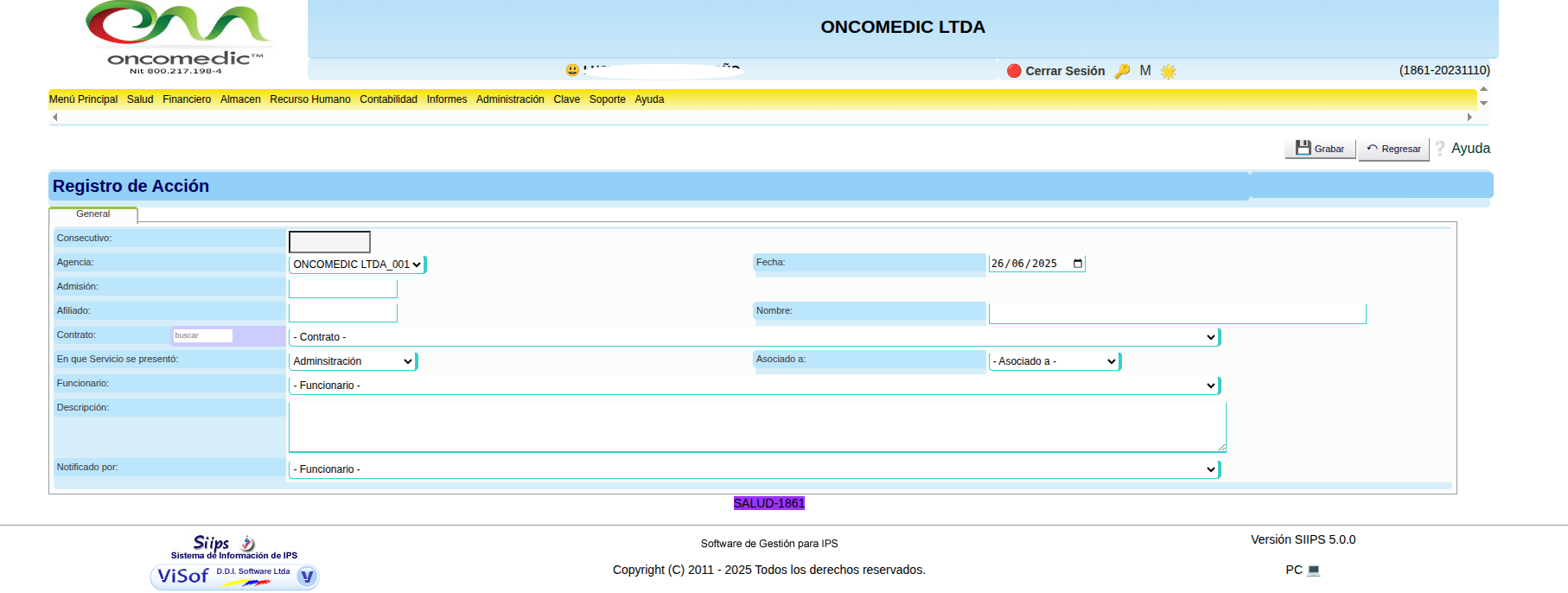
- Admisión: Número de admisión.
- Afiliado: Documento de identidad del afiliado que sufrió el evento.
- Contrato al cual pertenece el afiliado.
- Servicio: Consulta, apoyo terapéutico(aplicación de medicamentos), administración, farmacia...
- Asociado: seleccionar el caso correspondiente
- Nombre del funcionario que ejecutaba la actividad durante el evento
- Descripción del evento presentado
- En el campo “notificado por” escribir el nombre de la persona que esta realizando el reporte.
- Clic en grabar.
En caso de eventos asociados a dispositivos médicos, se completa la información de acciones inseguras, barreras y factores que pudieron contribuir al evento; para esto debe ejecutar el siguiente paso a paso:
• Salud – Sistema de calidad – Evento adverso
• Clic sobre el consecutivo del evento sobre el cual se va a realizar el informe detallado.
• Se evidencia el formulario pre llenado, en donde se debe diligenciar la parte destinada para el “Comite de seguridad” 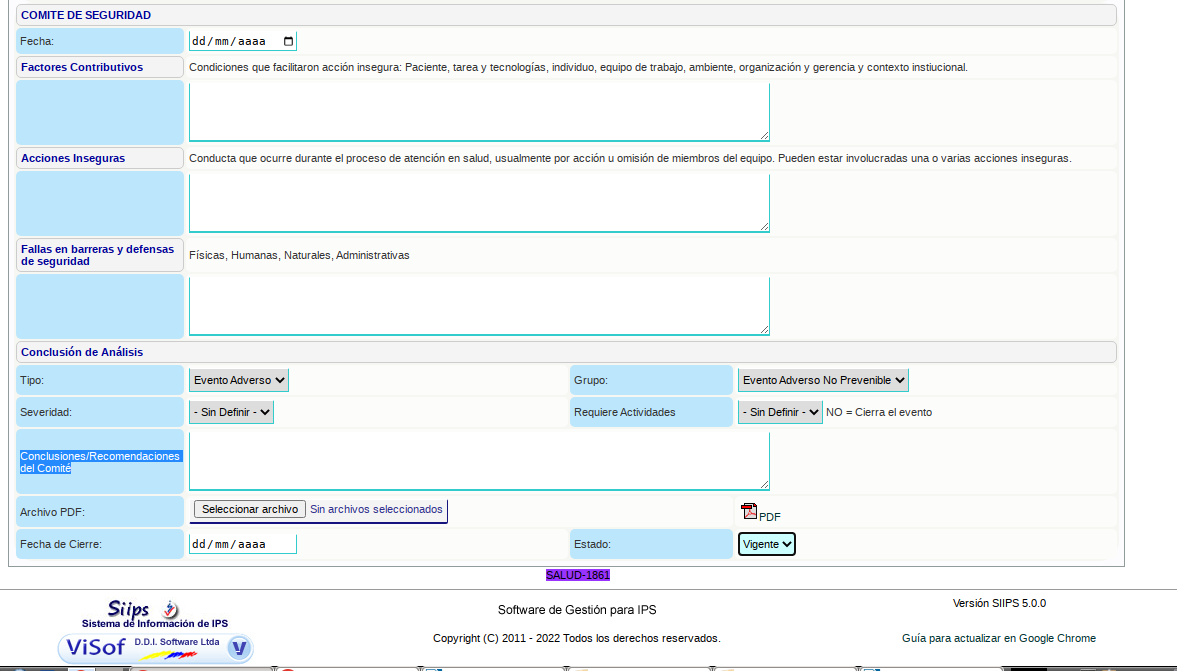 •
•
Se establece el formato Reporte de Eventos e Incidentes Adversos asociados al uso de Dispositivos Médicos. El cual debe diligenciarse en su totalidad por el químico farmacéutico responsable al programa institucional de tecnovigilancia. Este formato debe ser cargado como PDF en el reporte de acciones inseguras de VISOF generado.
Recomendaciones adicionales:
- Si en el evento o incidente adverso se encuentra involucrado más de un (1) dispositivo médico sospechoso, diligencie un formulario por cada uno de ellos, identificando como dispositivo 1, dispositivo 2 etc.
- Al diligenciar el campo observaciones, incluya datos completos, dado que la carencia de datos como el número de Registro Sanitario, lote, modelo, referencia o serial del dispositivo médico, no permitirá iniciar la investigación.
- Si el dispositivo no tiene riesgo de contaminación, se debe entregar al servicio farmacéutico el cual lo pondrá en cuarentena por el tiempo necesario para realizar el análisis del caso. Si el proveedor realiza la reposición del dispositivo, o si es necesario realizar el desecho de este, se tomarán fotografías las cuales se adjuntarán al formulario como evidencia.
- En el caso de que el dispositivo tenga riesgo de contaminación, se procederá a tomar fotografías cuando sea posible, las cuales se adjuntarán como evidencia al formulario, y finalmente se procederá a la disposición final siguiendo los protocolos respectivos de manejo de residuos hospitalarios.
Análisis de los Incidentes o Eventos Adversos Relacionados con Dispositivos Médicos.
El análisis y seguimiento de los eventos o incidentes adversos relacionados con dispositivos médicos será responsabilidad del Químico Farmacéutico, líder del Programa Institucional de Tecnovigilancia en Oncomedic LTDA. Este análisis tendrá como finalidad identificar las causas raíz y establecer medidas correctivas y preventivas que minimicen el riesgo de recurrencia, fortaleciendo la seguridad del paciente.
Para este propósito, se implementará el Protocolo de Londres como herramienta principal de análisis causal. Esta metodología permite una evaluación sistémica e integral de los factores que contribuyen a la ocurrencia del evento, considerando elementos clínicos, organizacionales, del entorno y del comportamiento humano.
De manera complementaria, se realizará un Análisis Modal de Fallos y Efectos (AMFE) orientado a identificar y valorar los riesgos potenciales asociados a los dispositivos médicos utilizados en la institución. Esta herramienta permitirá clasificar los dispositivos en función de su criticidad y establecer prioridades en la formulación de planes de gestión de riesgos, con acciones dirigidas a mitigar fallas potenciales antes de que se materialicen.
La aplicación combinada de ambas metodologías —Protocolo de Londres para análisis retrospectivo y AMFE para evaluación prospectiva— garantizará un enfoque integral en la tecnovigilancia, contribuyendo a la mejora continua de la calidad en la atención y al uso seguro de los dispositivos médicos en Oncomedic LTDA.
Reporte de incidentes o eventos adversos relacionados con dispositivos médicos a entidades externas.
El responsable del programa de tecnovigilancia, clasificará, analizará y finalmente reportará los casos en el aplicativo S.I. del invima, “para el Reporte Inmediato de Eventos e Incidentes Adversos Asociados al uso de Dispositivos Médicos (FOREIA001), por parte de Prestadores de Servicios de Salud, Fabricantes e Importadores de Dispositivos Médicos”. en caso de presentarse un evento o incidente adverso SERIO, dentro de las setenta y dos horas (72) siguientes al conocimiento de la ocurrencia del mismo. Si el caso corresponde a un evento adverso NO SERIO se consolida y se hace el reporte en la pestaña “reporte masivo trimestral”. Si en el trimestre en curso no se presentan eventos, se realiza el “reporte masivo en cero”,
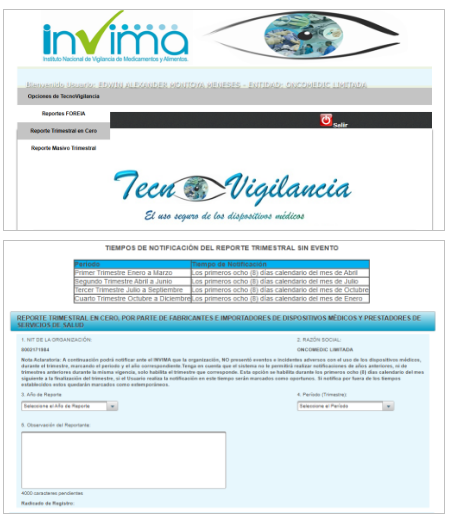
Para el reporte en el aplicativo dispuesto por el INVIMA para el reporte, se ingresa al siguiente enlace: https://farmacoweb.invima.gov.co/TecnoVigilancia/
1- Inicio del aplicativo para el reporte de eventos adversos asociados a dispositivos médicos.
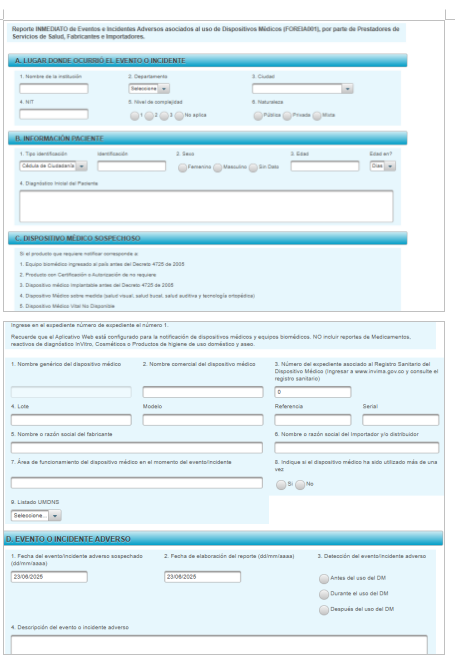
Reporte FOREIA para hacer el diligenciamiento de la información.
3. Campos requeridos para el reporte.
4. Como ultimo paso, se da clic en el botón guardar al final del documento.
Instrucciones para el reporte trimestral en cero (0).
Diligenciar si hay alguna observación y dar clic en el botón.
Recordar que los reportes en cero se realizan cada trimestre en el mes directamente después los 8 primeros días calendario.
Resultado Esperado, Indicadores y Metas
En caso de que se presente reportes.
- Indicadores de proceso
| Indicador | Fórmula | Meta sugerida |
| Tasa de notificación de eventos adversos o incidentes | (N° de eventos reportados / N° total de dispositivos médicos utilizados) × 100 | ≥ 1% |
| Cumplimiento del reporte al INVIMA dentro del tiempo requerido | (N° de reportes enviados oportunamente / Total reportes requeridos) × 100 | 100 % |
| Cobertura de capacitación en tecnovigilancia | (N° de trabajadores capacitados / Total trabajadores de la IPS) × 100 | ≥ 90% anual |
- Indicadores de resultado
| Indicador | Fórmula | Meta sugerida |
| Tasa de eventos adversos graves por dispositivos médicos | (N° de eventos graves / Total de eventos reportados) × 100 | Tendencia decreciente |
| Reducción de recurrencia de eventos similares | (N° de eventos repetidos en el año / N° total de eventos del año anterior) × 100 | ≤ 5% |
- Indicadores de gestión del riesgo
| Indicador | Fórmula | Meta sugerida |
| Porcentaje de eventos prevenibles identificados | (N° de eventos prevenibles / Total eventos reportados) × 100 | ≥ 50% |
| Tiempo promedio de respuesta a eventos críticos | (Sumatoria de días de respuesta a eventos críticos / N° de eventos críticos) | ≤ 3 días |
Tiempo de Ejecución y Fecha de Revisión del Programa
El programa de farmacovigilancia es un programa permanente que se evalúa mensualmente en el comité de farmacia y terapéutica y anualmente en el comité de calidad donde presenta los resultados obtenidos y las nuevas metas