Programa de Calidad del Servicio Farmacéutico
Regresar a Servicio Farmacéutico
Regresar a Manual de Procesos y Procedimientos de Farmacotecnia
Identificación

|
Nombre | Código | 
| |
| Manual de Procesos Gestión de Calidad del Servicio Farmacéutico | MPCF | |||
| Fecha de Emisión | Fecha de Actualización | Versión | ||
|
2010/04/01 |
2019-04-26 |
8 | ||
Elaboró: Luis Carlos Alvarez
Reviso y Autorizo Ultima Versión: Comité de Farmacia y Terapéutica
Introducción
El sistema de garantía de calidad del servicio farmacéutico permite asegurar que los productos y servicios que se brindan cuenten con los estándares de calidad exigidos, así como realizar verificación y seguimiento del que hacer de dicho servicio, su actuar se inicia con la selección de los medicamentos, la prescripción del profesional médico, la selección y adquisición de los medicamentos insumos y dispositivos médicos yluego con los procesos de recepción y distribución y finaliza con la recolección, evaluación y análisis de los posibles eventos adverso relacionados con la administración de los medicamentos o utilización de los insumos y dispositivos médicos en los pacientes, de manera que la gestión de los mismos es responsabilidad de todos los profesionales del equipo interdisciplinario de Oncomedic ltda: servicio farmacéutico, asistencial y administrativo, desde el gerente y las políticas organizacionales, hasta cada uno de los integrantes de la organización, médicos especialistas, farmacéuticos, enfermeras y personal administrativo, participando en las distintas etapas del proceso: prescripción, adquisición, almacenamiento, dispensación, administración y controles posteriores.
Cada proceso, producto o servicio de la organización es valorado desde la óptica del autocontrol, la auditoria interna y la auditoria externa y se establecen las medidas que permiten el reporte de las desviaciones, quejas y eventos adversos y de este modo verificar la calidad del servicio, identificar las oportunidades de mejora e implementar acciones para lograr el crecimiento empresarial y el mejoramiento continuo.
Objetivos
Asegurar el cumplimiento de los estándares de calidad de los productos y servicios suministrados por el servicio farmacéutico de Oncomedic limitada, estableciendo los procedimientos de control y seguimiento que permitan asegurar la seguridad en la atención, la calidad del servicio, el mejoramiento continuo y el aprendizaje organizacional.
Alcance
Este manual incluye acciones de todas las áreas y actividades relacionadas con el que hacer del servicio farmacéutico, desde el aspecto técnico y operativo permitiendo asegurar no solo la calidad sino la seguridad de la atención.
Marco conceptual
Marco Referencial
Para lograr el objetivo de calidad del servicio farmacéutico, se ha diseñado e implementado el Sistema de Garantía de la Calidad que busca estandarizar las operaciones internas, mejorar la capacidad de atender las demandas de los clientes, así como identificar y corregir posibles desviaciones y quejas incluso antes de que ellas ocurran.
El desarrollo de este sistema esta enfocado en los conceptos de garantía de calidad, seguridad del paciente y demás aspectos de la normatividad vigente dado que los medicamentos y dispositivos biomedicos son un eje fundamental en la atención, por lo tanto dentro de la institución se tienen un proceso de trazabilidad desde la adquisición, almacenamiento, traslado a preparación en la central de mezclas externa, recepción de dosis unitaria, aplicación o dispensación, seguimiento y atención farmacéutica. Para alcanzar este objetivo el servicio farmacéutico tiene un sistema documentado y supervisado de auto-control, auditorias internas y externas de la calidad que contempla las normalizaciones y registros de todas las fases del servicio:
- Prescripción
- Recepción
- Almacenamiento
- Preparación (Auditoria central de mezclas externa)
- Conservación y traslado
- Control de calidad institucional
- Administracion
- Seguimiento y control Efectos en el paciente y alertas sanitarias
Descripción del Proceso
En todas las fases del trabajo del servicio farmacéutico se puede determinar que un producto no cumple con las especificaciones requeridas para su uso o administración, la actividad de auto-control permite que el responsable de cada procedimiento se encargue de reportar la NO conformidad e iniciar la gestión del producto no conforme rotulando el medicamento o insumo medico que presenta la desviación y llevándolo a una zona especial identificada como área de producto no conforme que impida su uso equivocadamente, también se realizan auditorias internas y externas para corroborar la calidad.
Autoinspección: Las actividades de autoinspección permiten detectar cualquier desviación, se realiza rutinariamente por parte de cada funcionario del servicio farmacéutico dejando evidencia de su actividad, así mismo el cliente interno y externo verifica la calidad.
Auditoria interna: Consiste en una evaluación con el propósito de identificar la coherencia entre la calidad esperada y la calidad encontrada que permita el conocimiento de la situación de la organización, el análisis de los resultados y la elaboración de planes de mejoramiento de ser necesario, se deben realizar a:
- Personal.
- Instalaciones y Equipamiento.
- Adquisición y Proveedores
- Recepción.
- Almacenamiento.
- Documentación
- Sanitización e higiene
- Control de rótulos
- Control en la entrega de medicamentos
- Seguimiento farmacológico.
Auditoria externa: diversos organismos de control cumplen una importante labor de auditoria para nuestra institución.
Personal:
El personal de Oncomedic es valorado en el cumplimiento de sus funciones y en la idoneidad para su cargo, luego de la selección del personal este recibe una inducción general y del cargo, con re inducción periódica y evaluación de desempeño según se programa
Instalaciones y equipamiento:
Adquisiciones y proveedores:
- Fuente: Listado de pedidos/Lista de verificación.
- Método: Retrospectivo.
- Muestra: 100% de los pedidos realizados en el período evaluado.
- Responsable: Regente de farmacia verificación químico farmacéutico.
- Frecuencia: Cada seis meses.
- Objetivo: Evaluar el grado de ajuste de las adquisiciones a la política de IPS
- Expresión Matemática:
Control en la Recepción:
Verificaciones Técnicas
Fecha de Vencimiento
- Número de lote de fabricación
- Registro Sanitario
- Código de Barras, EAN
- Estado del Empaque
- Estado del Envase
- Estado de las etiquetas
- Información contenida en las etiquetas del envase/empaque
- Características físicas y organolépticas del producto
- Condiciones de almacenamiento (aquellos productos que requieran condiciones especiales, deben identificarse y guardarse inmediatamente de acuerdo a las instrucciones).
- Nombre del fabricante
Verificación Administrativas e Ingreso a Inventario
Nombre del producto solicitado Vs. Nombre del producto recibido
Concentración del producto solicitado Vs. Concentración del producto recibido
Forma Farmacéutica del producto solicitado Vs. Forma Farmacéutica del producto recibido
Precio Unitario
Fecha y Forma de entrega
Cantidad Pedida Vs Cantidad Recibida Vs Cantidad Facturada
Factura en concordancia con el documento de compra, que cumpla con las especificaciones legales y que contenga el número de copias exigidas.
Lo proveedor de las materias primas y dispositivos médicos deben ser certificados. Procedimiento de Evaluación y Selección del Proveedor
Recepción
1) Tipo: Tasa.
2) Fuente: Fichas de recepción
3) Método: Retrospectivo. -
4) Muestra: Totalidad de entradas en el Servicio Farmaceutico (muestra significativa). -
5) Responsable: Administrativo. -
6) Frecuencia: Semestral.
7) Objetivo: Evaluar si se comprueba la conformidad de lo recibido con lo que figura en la factura o vale de entrada.
8) Expresión Matemática: # de vales comprobados con los medicamentos recibidos x 100
# total de vales recibidos
9) Nivel de de cumplimiento 99%
Conformidad con el pedido
1) Tipo: Tasa.
2) Fuente: Fichas de recepción técnica, Formato de solicitud de pedidos
3) Método: Retrospectivo. -
4) Muestra: Totalidad de entradas en el Servicio Farmacéutico (muestra significativa). -
5) Responsable: Administrativo. -
6) Frecuencia: Semestral
7) Objetivo: Evaluar si se comprueba la conformidad de lo recibido, con lo solicitado solicitado.
8) Expresión Matemática: # de vales comprobados con pedidos x 100
Control de Almacenamiento
Durante el almacenamiento, se deben controlar el inventario asegurando la rotación de inventario y del conteo físico, comparado con el registro de existencias. Se debe realizar inventario general y pruebas selectivas que permitan identificar.
- Condiciones ambientales de temperatura y humedad relativa de almacenamiento
- Verificar que los productos fotosensibles se almacenen protegidos de la luz.
- Mantenimiento de la cadena de frío a temperaturas de refrigeración entre 2ºC y 8ºC.
- Integridad del producto durante el almacenamiento.
- Control de existencias
- Fechas de vencimiento.
Cualquier no conformidad en este aspecto debe generar el reporte, la rotulación con producto no conforme y la respectiva gestión de la desviación
- Estos deben almacenarse en un lugar apropiado de acuerdo a las exigencias de almacenaje de cada producto, de uso exclusivo, con control y registro de temperatura y humedad
- Deberán protegerse de la luz aquellos productos que lo requieran.
- Para el almacenaje de los lotes deberá utilizarse el sistema FIFO.
- Se recomienda una inspección periódica del stock almacenado.
- Cualquier anormalidad debe ser registrada.
- Para las materias primas que requieran refrigeración, las condiciones de almacenamiento deben incluir la supervisión y documentación diaria de los refrigeradores, para asegurar que mantienen su temperatura entre 2° y 8°C y la inspección de todos los lugares de almacenamiento al menos una vez al mes.
Conservación Especial
1) Tipo: Tasa.
2)Fuente: Relación (listado) de medicamentos de conservación especial/Ficha técnica de los productos. Comprobación del lugar de almacenamiento. -
3) Método: Concurrente (se refiere a lo que hay ese día físicamente). -
4) Muestra: Totalidad de medicamentos de conservación especial. -
5) Responsable: Personal auxiliar. -
6) Frecuencia: Un día al azar cada seis meses.
7) Objetivo: Evaluar si la conservación de medicamentos se realiza de forma adecuada según las condiciones de conservación que figuran en la ficha técnica del producto.
8) Expresión Matemática: # de especialidades incorrectamente almacenadas x 100
# total de especialidades de conservación especial
Revisión de Caducidades
1) Tipo: Tasa.
2) Fuente: Inspección visual de la fecha de caducidad. -
3) Método: Concurrente. -
4) Muestra: Totalidad de medicamentos almacenados (muestra significativa). -
5) Responsable: Personal auxiliar. -
6) Frecuencia: Cada seis meses.
7) Objetivo: Evaluar la eficacia del control de caducidades.
8) Expresión Matemática: # de especialidades caducadas x 100
Costo de las Caducidades
1) Tipo: Tasa.
2) Fuente: Listado del costo de las adquisiciones realizadas por el Servicio Farmaceutico/ Relación de los costos de las especialidades caducadas en el período a evaluar. -
3) Método: Retrospectivo. -
4) Muestra: Totalidad de medicamentos adquiridos. -
5) Responsable: Administrativo. -
6) Frecuencia: semestral.
7) Objetivo: Evaluar las pérdidas económicas por medicamentos caducados.
8) Expresión Matemática: Importe económico de las especialidades caducadas x 100
Importe económico de las adquisiciones
Control Del Proceso o Procedimiento
Hacen parte del proceso de autocontrol y auditoria interna, se realiza verificación de:
- Elementos y equipos a usar en el proceso productivo
- Cumplimiento de protocolos
- Verificación de procesos en puntos crícticos
Producto del análisis de estos aspectos se pude generar conformidades o no conformidades, estas ultimas generarían una Desviaciones de Calidad que debe ser reportada y analizada de acuerdo a el procedimiento establecido
Indicadores generales de elaboración
Selección de Materias Primas
1) Tipo: Tasa.
2) Fuente: Registro de materias primas adquiridas. Archivo de hojas de control de materias primas. -
3) Método: Retrospectivo. -
4) Muestra: Total de materias primas recibidas. -
5) Responsable: Quimico Farmacéutico. -
6) Frecuencia: Trimestral.
7) Objetivo: Estimar el grado de comprobación de la calidad y especificaciones de la materia prima en el momento de su adquisición.
4) Expresión Matemática: # de materias primas que no debieron admitirse x 100
No total de materias primas recibidas
Existencia de Protocolos de Fabricación
1) Tipo: Tasa.
2) Fuente: Libro recetario oficial o registro de fórmulas. Archivo de protocolos de fabricación. -
3) Método: Retrospectivo. -
4) Muestra: 100% de las fórmulas elaboradas un día al azar. -
5) Responsable: Quimico Farmacéutico. -
6) Frecuencia: Mensual
7) Objetivo: Estimar el grado de exactitud y estandarización de los procesos de elaboración utilizados.
8) Expresión Matemática:# de fórmulas elaboradas sin protocolo x 100
Total de fórmulas distintas elaboradas
Cumplimiento de las Hojas de Elaboración
1) Tipo: Tasa.
2) Fuente: Libro recetario oficial o registro de fórmulas. Archivo de hojas de elaboración. -
3) Método: Retrospectivo. -
4) Muestra: 100% de los lotes elaborados un día al azar.
5) Responsable: Quimico Farmacéutico. -
6) Frecuencia: Mensual
7) Objetivo: Estimar el grado de documentación de las características de los lotes elaborados.
4) Expresión Matemática: # de lotes sin hoja de elaboración x 100
No de Lotes elaborados
Registros de Indicadores Gestión ENERO 2011
Control de Calidad en Fabricación
1) Tipo: Tasa.
2) Fuente: Libro recetario oficial o registro de fórmulas. Archivo de hojas de elaboración (en base a los protocolos). -
3) Método: Retrospectivo. -
4) Muestra: 100% de los lotes elaborados un día al azar.
5) Responsable: Quimico Farmacéutico.
6) Frecuencia: Mensual.
7) Objetivo: Estimar el grado de cumplimiento de los ensayos de control de calidad de las fórmulas elaboradas.
4) Expresión Matemática: # de lotes sin controles x 100
No de lotes elaborados
Calidad en Fabricación
1) Tipo: Tasa 2) Recogida de datos: -Fuente: Protocolos de fabricación y archivo de hojas de elaboración y control de calidad -Método: Retrospectivo -Muestra: 100% de los lotes fabricados -Responsable: Farmacéutico -Frecuencia: Cada mes 3) Objetivo: Estimar el grado de calidad obtenido en la elaboración
4) Expresión Matemática: # de lotes con controles fuera de intervalo x 100
No de lotes elaborados
Identificación de la fórmula elaborada
1) Tipo: Tasa 2) Recogida de datos: -Fuente: Libro recetario oficial o registro de fórmulas. Etiquetas de las fórmulas elaboradas y Protocolos de elaboración -Método: Retrospectivo -Muestra: 100% de las preparaciones elaboradas un día al azar -Responsable: Farmacéutico -Frecuencia: Cada mes 3) Objetivo: Evaluar la correcta identificación de las fórmulas elaboradas de acuerdo a las especificaciones que figuran en el protocolo de elaboración
4) Expresión Matemática: # de preparaciones incorrectamente etiquetadas x 100
No total de preparaciones
Acondicionamiento
1) Tipo: Tasa 2) Recogida de datos: -Fuente: Libro recetario oficial o registro de fórmulas. Control visual de las preparaciones y Protocolos de elaboración -Método: Concurrente -Muestra: 100% de las preparaciones elaboradas en un día al azar -Responsable: Farmacéutico -Frecuencia: Cada mes 3) Objetivo: Evaluar el correcto acondicionamiento de la fórmula elaborada para que se mantenga su eficacia y seguridad
4) expresión Matemática: # de preparaciones incorrectamente acondicionadas x 100
total de preparaciones elaboradas
Validación de la prescripción
1) Tipo: Tasa 2) Recogida de datos: -Fuente: Libro recetario oficial o registro de fórmulas. Prescripciones para elaboración de fórmulas y Archivo de hojas de elaboración -Método: Retrospectivo -Muestra: 100% de las fórmulas elaboradas -Responsable: Farmacéutico -Frecuencia: Cada mes 3) Objetivo: Estimar el grado de verificación de la prescripción por el farmacéutico antes de la elaboración
4) Expresión Matemática:# de fórmulas que no deberían ser elaboradas x 100
No de fórmulas elaboradas
Indicadores Específicos de Elaboración (mezclas intravenosas)
Control de Esterilidad
1) Tipo: Tasa.
2) Fuente: Registro de mezclas elaboradas. Archivo de hojas de control de esterilidad -
3) Método: Retrospectivo. -Muestra: 20% de las mezclas elaboradas un día al azar
4) Responsable: Quimico Farmacéutico. -
5) Frecuencia: Variable (según tipo de mezcla)
6) Objetivo: Estimar el grado de cumplimiento de los controles de esterilidad establecidos
7) Expresión Matemática: # de mezclas controladas x 100
No de mezclas elaboradas x 0.2
Esterilidad
1) Tipo: Tasa.
2) Fuente: Archivo de controles de esterilidad. -
3) Método: Retrospectivo. -
4) Muestra: 100% de las mezclas controladas. -
5) Responsable: Farmacéutico. -
6) Frecuencia: Mensual.
7) Objetivo: Estimar el grado de contaminación de las fórmulas (mezclas) elaboradas. (un indicador similar puede ser para otros parámetros de calidad: pH,...etc.)
4) Expresión Matemática: # de mezclas contaminadas (o fuera de rango) x 100
No de mezclas controladas
Cálculo de los componentes
1) Tipo: Tasa.
2) Recogida de datos: -Fuente: Archivo de hojas de elaboración y Prescripciones médicas -
3) Método: Retrospectivo. -
4) Muestra: 100% de las mezclas elaboradas un día al azar. -
5) Responsable: Farmacéutico. -
6) Frecuencia: Mensual.
7) Objetivo: Estimar el grado de exactitud en la elaboración de las mezclas respecto a los requerimientos del paciente y/o la prescripción
4) Expresión Matemática:# de mezclas incorrectamente calculadas x 100
No de mezclas elaboradas
Control de Producto Terminado Unidosis, Nutriciones Parenterales Formulas Magistrales
Luego de la adecuación de la mezclas, nutrición o magistral pasa por un periodo de cuarentena mientras es evaluado por el químico de calidad quien corrobora la idoneidad del producto mediante los siguientes análisis:
Inspección Visual
Todas las preparaciones deben ser inspeccionadas individualmente, para detectar la presencia de partículas visibles u otros elementos extraños inmediatamente después de terminar la preparación y como condición para su liberación. Deben ser inspeccionadas cuanto a:
- Precipitación
- Separación de fases
- Cambio de color
- Turbidez
- Cualquier evidencia de reacción anormal que indique la posibilidad de presentarse una incompatibilidad en la mezcla.
- Verificación de hermeticidad
- Presencia de material en suspensión en mezclas Liquidas
Otros datos a tomar en cuenta
- Ph
- Conductividad del agua purificada
Los producto en los que se detectan defectos, debe descartarse inmediatamente, para impedir su administración accidental a los pacientes.
Además, es importante que antes de la administración, el profesional a cargo de ésta, inspeccione nuevamente las características de la preparación que se describieron previamente con el fin de corroborar la idoneidad del producto.
Control de Volúmenes
Control de Etiquetado
Es fundamental controlar el etiquetado de toda unidosis, nutrición, magistral o medicamento reembazado o reempacado así:
- Revisión de cada etiqueta contra la receta recibida de cada paciente, antes de que éstas sean ingresadas al área de preparación.
- Identificar cuantas etiquetas requiere el producto, por ejemplo una en la bolsa del preparado (envase primario), otra en el envase secundario de la preparación (bolsa estéril protectora) y otra para pegar en la historia clínica como control y testigo de la administración al paciente, por parte de la enfermería.
- Verificar nombre del paciente
- Medicamento o mezcla
- Dosis
Además, es importante que antes de la administración, el profesional a cargo de ésta, inspeccione nuevamente las características de la etiqueta que se describieron previamente con el fin de corroborar la idoneidad del producto.
Integridad del Envase Primario y Secundario
Es imprescindible revisar el estado de la bolsa EVA una vez terminada la preparación para verificar la integridad de los sellos o cualquier otro defecto visible, además de la correcta inclusión de los equipos de infusión que pueden conducir a la filtración de las bolsas durante el transporte o almacenamiento. El envase secundario debe quedar perfectamente sellado para evitar el contacto directo de la preparación con el medio ambiente.
Control Gravimétrico
Hace referencia al control del peso del producto, para el caso de las nutriciones se puede utilizar la diferencia relativa entre el peso real de la nutrición y el peso teórico que se halla tomando en cuenta las las densidades de todos los productos y el peso de las bolsas utilizadas, apareciendo el mismo en la hoja de elaboración. El error gravimétrico se calcula en porcentaje respecto al peso teórico mediante la siguiente ecuación:
Error gravimétrico(%) = [(peso real-peso teórico) × 100]/peso teórico. Esta diferencia, expresada en porcentaje, define el error gravimétrico de preparación (EGP). Es aceptable por debajo del 5%
Controles Microbiologicos
El análisis microbiologico para lotes de preparación mayores a 30 unidades se tomara una muestra representativa
Distribución o dispensación
- La distribución o dispensación de los productos, se efectuarse en contenedores que las protejan de cambios bruscos de temperatura tomando en cuenta los tiempos requeridos para su traslado
- Se realiza acta de entrega, que contenga los siguientes datos:
- Nombre del paciente
- Ubicación de éste (en sala y/o cama)
- Vía administración
- Nombre del farmacéutico responsable
- Nombre y firma de quién entrega
- Fecha y hora de entrega
- Nombre y firma de quién recepciona
- Revisión del transporte e integridad de la bolsa
Este registro tiene como finalidad, asegurar que la preparación sea dispensada al paciente que corresponda.
El transporte de los productos que se suministran para externos debe asegurar el cumplimiento de todas las exigencias necesarias para mantener la integridad y estabilidad del producto, con una temperatura ideal entre 4-8°C
Liberación del Producto
Luego de las inspecciones que permiten verificar la calidad del producto se procede a realizar la liberación del producto para su distribución a los clientes del servicio farmacéutico
Auditoria de la Distribución del Producto
valuación del Servicio de Dispensación
Para garantizar el adecuado desarrollo de la dispensación, y la mejora progresiva del servicio, es necesario evaluar la práctica realizada. La evaluación se basará en la valoración del grado de cumplimiento de los procedimientos normalizados de trabajo para esta actividad.
Esta se realiza mediante:
— Análisis del sistema de registro que permite medir la actividad.
— Observación directa del funcionamiento.
— Entrevista a pacientes.
La evaluación del servicio puede hacerse por el propio farmacéutico responsable o por un evaluador externo
El servicio de seguimiento farmacoterapéutico personalizado debe pretender los siguientes objetivos:
a) Buscar la obtención de la máxima efectividad de los tratamientos farmacológicos.
b) Minimizar los riesgos asociados al uso de los medicamentos, y por tanto, mejorar la seguridad de la farmacoterapia.
c) Contribuir a la racionalización del uso de los medicamentos como principal herramienta terapéutica de nuestra sociedad.
d) Mejorar la calidad de vida de los pacientes.
Son requisitos del servicio de seguimiento farmacoterapéutico personalizado La oferta y realización del seguimiento farmacoterapéutico de un paciente concreto es un servicio novedoso y complejo que conlleva una serie de exigencias y requisitos ineludibles, expuestos a continuación:
a) Compromiso del farmacéutico con los resultados de la farmacoterapia en cada paciente. Puesto que el contrato asistencial es un contrato de medios, esto significa que el farmacéutico, de acuerdo con el paciente, asume la responsabilidad de haber puesto todos los medios a su alcance para que los medicamentos que éste utilice le produzcan efectos beneficiosos para su salud.
b) Garantía de continuidad en el servicio. Esto implica que el compromiso anteriormente adquirido va a ser ofrecido y prestado mientras el paciente esté de acuerdo con ello.
c) Disponibilidad de información actualizada sobre el paciente y su tratamiento.
d) Documentación y registro de la actividad, tanto de las intervenciones realizadas como de los resultados obtenidos. <b
Transcripción de prescripciones médicas
1) Tipo: Tasa.
2) Fuente: Prescripciones médicas y Fichas farmacoterapéuticas. -
3)Método: Retrospectivo. -
4)Muestra: Muestra significativa en función del # de prescripciones. -
5)Responsable: Qumico Farmacéutico. -
6) Frecuencia: Trimestral
7) Objetivo: Evaluar el grado de exactitud en la transcripción de las prescripciones médicas a la ficha farmacoterapéutica.
8) Expresión Matemática: # de medicamentos incorrectamente transcritos x 100
# total de medicamentos prescritos
Para el caso de la IPS oncomedic este Proceso es digital por tal motivo no se requiere
Preparación de carros
1) Tipo: Tasa.
2) Fuente: Listado de preparación de carros. Fichas farmacoterapéuticas. Revisión de medicamentos en los carros. -
3)Método: Concurrente. -
4)Muestra: 100% de la medicación preparada un día escogido al azar. -
5) Responsable: Quimico Farmacéutico. -
6) Frecuencia: Trmestral.
4) Objetivo: Estimar el grado de exactitud en la preparación de carros de acuerdo a los listados obtenidos de las fichas farmacoterapéuticas.
4) Expresión Matemática: # de medicamentos incorrectamente preparados x 100
No total de medicamentos a dispensar
Dispensación
1) Tipo: Tasa.
2) Fuente: Listado de preparación de carros. Fichas farmacoterapéuticas. Revisión de medicamentos devueltos en los carros. Reclamaciones hechas desde los servicios. -
3) Método: Retrospectivo.
4) Muestra: 100% de la medicación devuelta un día escogido al azar y el 100% de las reclamaciones de ese día. -
5) Responsable: Farmacéutico. -
6) Frecuencia: Trimestral
7) Objetivo: Estimar el grado de exactitud en la dispensación de medicamentos de acuerdo con la prescripción médica.
8) Expresión Matemática:# de medicamentos incorrectamente preparados x 100
#total de medicamentos a dispensar
Distribución
1) Tipo: Tasa.
2)-Fuente: Medicación preparada para la distribución / Formularios de solicitud de pedidos.
3) Método: Concurrente.
4) Muestra: 100% de los vales de pedidos de un día escogido al azar. -
5) Responsable: Quimico Farmacéutico. -
6) Frecuencia: Mensual.
7) Objetivo: Estimar el grado de exactitud en la distribución (entrega) de medicamentos de acuerdo con los Formularios de solicitud de pedidos
4) Expresión matemática: # de medicamentos incorrectamente preparados para distribuir x 100
No total de medicamentos solicitados
Validación de los Pedidos de Sala
1) Tipo: Tasa.
2)Fuente: Solicitud de pedidos de los servicios del hospital.
3) Método: Retrospectivo. -
4) Muestra: 100% de los vales de pedidos de un día escogido al azar. -
5) Responsable: Farmacéutico.
6) Frecuencia: Mensual.
4) Objetivo: Estimar el grado de validación por el farmacéutico de las dispensaciones efectuadas a los servicios del hospital mediante los vales de pedidos de estos
6) Expresión Matemática: # de vales de pedidos revisados por el farmacéutico x 100
No total de vales de pedidos dispensados
Medicamentos de control especial
Dispensación de medicamentos de control especial
1) Tipo: Tasa.
2)Fuente: Prescripciones médicas de medicamentos de control especial. Normas o protocolos para la dispensación de medicamentos de control especial. -
3) Método: Retrospectivo.
4) Muestra: 100% de las dispensaciones efectuadas en un día escogido al azar. -
5) Responsable: Quimico Farmacéutico. -
6) Frecuencia: Mensual.
7) Objetivo: Estimar el grado de cumplimiento de las especificaciones sobre dispensación de medicamentos de control especial.
8) Expresión matemática: # de medicamentos de control especial dispensados sin cumplir norma o protocolo x 100
total medicamentos de control especial dispensados
Revisión de Depósitos de Medicamentos en Salas
1) Tipo: Tasa.
2) Fuente: Impreso de revisión de los depósitos de medicamentos en sala. Medicamentos en depósitos de medicamentos en sala. -
3) Método: Concurrente. -
4) Muestra: Totalidad de los depósitos de medicamentos en sala. -
5) Responsable: Quimico -Farmacéutico.
6) Frecuencia:Semestral por depósito de sala.
7) Objetivo: Estimar el estado de la medicación almacenada en los depósitos de medicamentos situados en los servicios del hospital y por consiguiente de su funcionalidad y seguridad.
4) Expresión matemática: # de medicamentos (en unidades) rechazados en la revisión x 100
No total medicamentos (en unidades) revisados
Gestión de Producto no Conforme o No Conformidad
Producto del auto-control, las auditorias internas o externas y la información de los clientes pueden reportarse:
- No Conformidad: Es el incumplimiento de un requisito cualquiera especificado en el sistema de calidad, tales como el incumplimiento a normas o procedimientos. Las no conformidades son usualmente establecidas en auditorias, inspecciones programadas o seguimientos no programados a la empresa.
- Producto No Conforme: Aquel producto que no cumple parcial o totalmente con las especificaciones de calidad exigidas por parte de los usuarios o clientes. Un producto no conforme puede ser o no rechazado, en este último caso puede tener defectos menores tales como etiquetas borrosas que no requerirían rechazar el producto.
- Producto Rechazado: Producto o lotes completos que son rechazados por el cliente o por la empresa debido a que se clasifica como no conforme y que además el grado de incumplimiento de las especificaciones lo hacen inútil, inservible o no apto para su uso por razones de riesgo para la salud, la imagen de la empresa o el incumplimiento de las normas técnico-legales para su comercialización y uso. Un producto rechazado generalmente implica la devolución del producto.
El producto detectado y clasificado como no conforme debe ser reportado al Director Técnico identificando las causas de la devolución o no conformidad:
- Deficiencias de la calidad
- Envío equívoco
- Incumplimiento contractual
- Incumplimiento comercial
- Revocación de los términos contractuales y/o modificación de acuerdos comerciales post-entrega del producto
Los productos devuelto o rechazados por razones diferentes a la calidad, se rotulan como PRODUCTO DEVUELTO. El proceso de reporte se puede por dos vías dependiendo la fuente de modo que si la no conformidad o producto no conforme se identifica dentro del servicio por parte del personal que produce o libera el producto, o por un auditor se establece una Desviaciones de Calidad y si la no conformidad es reportada por un cliente externo se constituye como una Queja o Reclamo
La persona responsable del control de la calidad realiza el análisis causal que incluya la evidencias de trazabilidad del producto y genera las debidas correcciones, acciones correctivas, re-proceso, re-clasificación, reparación, desecho, concesión, permiso de desviación o liberación según el caso y de acuerdo a los protocolos establecidos.
Casos Especiales: Si el producto no conforme es detectado antes del envió al cliente y no es clasificado como rechazado, se procederá a corregir la desviación de la calidad, esto aplica en casos tales como:
- Deterioro menor en etiquetas o empaques.
- Deterioro del material de embalaje que no afecta el contenido ni la presentación del producto.
Producto Rechazado
Si el producto se considera rechazado debe demarcarse con el correspondiente rotulo de PRODUCTO RECHAZADO y se ubicará en el área de almacenamiento destinada a los productos rechazados con el fin de minimizar los riesgos de liberación del producto. Esta actividad se realizará lo más rápido posible una vez se haya detectado la desviación del producto y se procederá a la disposición final del producto. En caso de que el producto rechazado además deba ser recogido del mercado, se aplicará el procedimiento de RETIRO DE PRODUCTOS DEL MERCADO.
Gestión de Productos Retirados del Mercado
Un producto retirado del mercado es aquel que después de haber sido entregado por venta, comodato o muestra, se identifica que no cumple con las especificaciones de calidad ya sea porque no es efectivo para el uso propuesto, o que afecte de algún modo la salud del usuario.
El retiro del mercado de un producto puede realizarse por mandato de una autoridad competente como el INVIMA (Instituto de Vigilancia de Alimentos y Medicamentos) o la Secretará de Salud, por un cliente interno, por un cliente mayorista y destinario de la distribución directa, por la existencia de alertas internacionales y nacionales que emiten las agencias de la red de tecnovigilancia a la que está adscrita la empresa a través del INVIMA.
La gestión de un producto retirado del mercado se realiza mediante el siguiente proceso
- Registrar las quejas, análisis y seguimiento individual, una vez se ha informado la No conformidad del producto se realiza la gestión de la queja con su respectivo plan de mejoramiento, en caso de ser un producto con riesgo alto se realiza el tramite inmediato para el retiro del producto
- Realizar seguimiento y análisis sistemático de las quejas presentadas en el periodo de un año y mediante un histograma de frecuencia que presente el número de quejas versus el tipo de queja.
- Colectar si es posible una muestra de producto no conforme y una muestra de retención (si existiese) para corroborar el incumplimiento de especificaciones de la calidad del producto.
- Analizar el porcentaje de quejas de acuerdo a origen y gravedad.
- Realizar informe de gestión de las queja que incluye las acciones correctivas y demas que permitan el manejo de las causas repetitivas de las quejas, esto en caso de que el análisis señale claramente el origen común de la mayor parte de las quejas.
- Informe a gerencia de la situación y emición de autorización para retirar el producto en menos de 48 horas despues de detectada la necesidad de retirar los productos del mercado.
- Presentar informe al director de la subdirección de insumos para la salud del INVIMA, con copia al responsable del programa nacional de tecnovigilancia de esa institución, en un término no mayor a 72 horas contados desde el momento en que se detecta la necesidad de retirar los productos del mercado en un oficio firmado por el Gerente y el Director Técnico con los siguientes datos:
- Datos informativos de la empresa
- Explicación detallada del motivo de retiro del producto de mercado
- Descripción de los productos retirados y descripción de lotes
- Cronograma de acciones a tomar
- Firma del Gerente General y Director Técnico
- Planear del despliegue logístico necesario para realizar el retiro del producto del mercado.
- Ubicar todos y cada uno de los clientes mediante la información consignada en las tarjetas kardex, archivos y/o facturas de venta e informarlos del retiro del producto y la necesidad de mantener acceso restringido del mismo.
- Recoger los productos y enviar a la bodega de almacenamiento.
- Recibir los productos en la bodega de almacenamiento y se ubicarlos en el área de productos RECHAZADOS, cada caja contenedora debe tener inscrito el Rótulo de Producto Retirado del Mercado.
- Una vez se determine que han sido devueltas el número de unidades mayor al 80% se procede a la destrucción del producto rechazado, esta destrucción la debe realizar una empresa contratada que se acredite en destrucción y disposición de materiales de rechazo. La documentación resultante de la destrucción se adjuntará al batch record del producto descrito en el procedimiento correspondiente. La destrucción de las unidades será realiza bajo los mismos parámetros indicados para la destrucción de productos rechazados por deficiencias de la calidad señalados en el procedimiento de GESTIÓN DE PRODUCTO NO CONFORME
- El Director Técnico y el Gerente General deben realizar la conciliación de la cantidad producida, distribuida, y retirada del mercado, el cual se anexa al registro de lote del producto y junto con las conclusiones
- El área de ventas y Dirección Técnica emitirán el informe final definiendo:
- Tiempo de recolección
- Unidades recogidas
- Estado de las devoluciones
- Clientes más eficientes en la devolución
- Clientes menos colaboradores con la devolución
- Costos finales del retiro de los productos
- Inconvenientes no previstos y consecuencias técnicas y comerciales del retiro de productos
- Informar al INVIMA los resultados obtenidos del retiro del mercado con datos que presenten el porcentaje de producto retirado y las acciones tomadas con estos productos.
Divulgación del Estado de Producto Rechazado:
El Director Técnico informará con evidencias (fotografías, actas, documentos probatorios) al Gerente la existencia de productos rechazados y propondrá las actividades de recolección del producto para evitar su uso y con ello la afectación a los clientes y/o a las relaciones comerciales de la empresa en general.
El Director Técnico realizará un acta escrita que describe las actividades realizadas para el retiro del producto y la hará firmar por el Gerente General y el Representante Legal. De dicha acta se enviará al INVIMA una copia y otra se archivará en los archivos de desviaciones de la calidad.
Se considera que la No conformidad está cerrada cuando se emita el informe final, en el cual se evalúa el mayor número de variables del proceso realizado. Se adjuntará al informe copia del formato diligenciado de REGISTRO DE GESTIÓN DE PRODUCTO NO CONFORME y a su vez otra copia se anexará a los documentos que hacen parte de la trazabilidad de los productos conforme con el instructivo de trazabilidad de los productos.
Destino Final del Producto Rechazado:
Los productos rechazados deben destruirse o devolverse al proveedor según lo que se manifieste en el respectivo contrato de compraventa del producto, las actividades en ambos casos son las siguientes:
- Devolución del producto al proveedor: Se debe obtener la carta de aceptación de devolución por parte del proveedor del producto y el Director Técnico debe verificar la correcta puesta en marcha de las actividades de envío del producto rechazado y la confirmación de recepción del producto por parte del proveedor, de dicha actividad se debe archivar copia de los documentos que evidencien la gestión de devolución del producto al proveedor, junto con el respectivo expediente de desviaciones de la calidad elaborado por el Director Técnico. Devoluciones
- Destrucción del producto: En caso de que el producto requiera ser destruido se enviara a la empresa encargada de la gestión de residuos siguiendo todos los procesos para su disposición final se debe conservar un acta de destrucción del producto elaborado por la empresa responsable en donde se indique:
Nombre de los responsables de la destrucción
Fecha de destrucción
Lugar de la destrucción
Método o modo de destrucción
Firmas autorizadas del acta de destrucción De dicha actividad de destrucción del producto se debe archivar copia de los documentos que evidencien la gestión de destrucción del producto. Dichos documentos serán archivados junto con el respectivo expediente de desviaciones de la calidad elaborado por el Director Técnico.
FORMATO DE PRODUCTO NO CONFORME
Auditoria Interna de Oportunidad en la Entrega de Medicamentos
En el desempeño institucional consideramos la oportunidad en la atención como un valor fundamental por lo cual se monitoriza y estudia constantemente para optimizar los resultados, al momento es un proceso sistematizado que se realiza mendiante solicitud al area de sistemas quien provee la información pertinente
Cuadro de Procedimiento de Oportunidad en la Entrega de Medicamentos
| Nombre del Procedimiento |
Auditoria interna en oportunidad en la entrega de medicamentos. |
| Responsable |
Auditor. |
| Alcance |
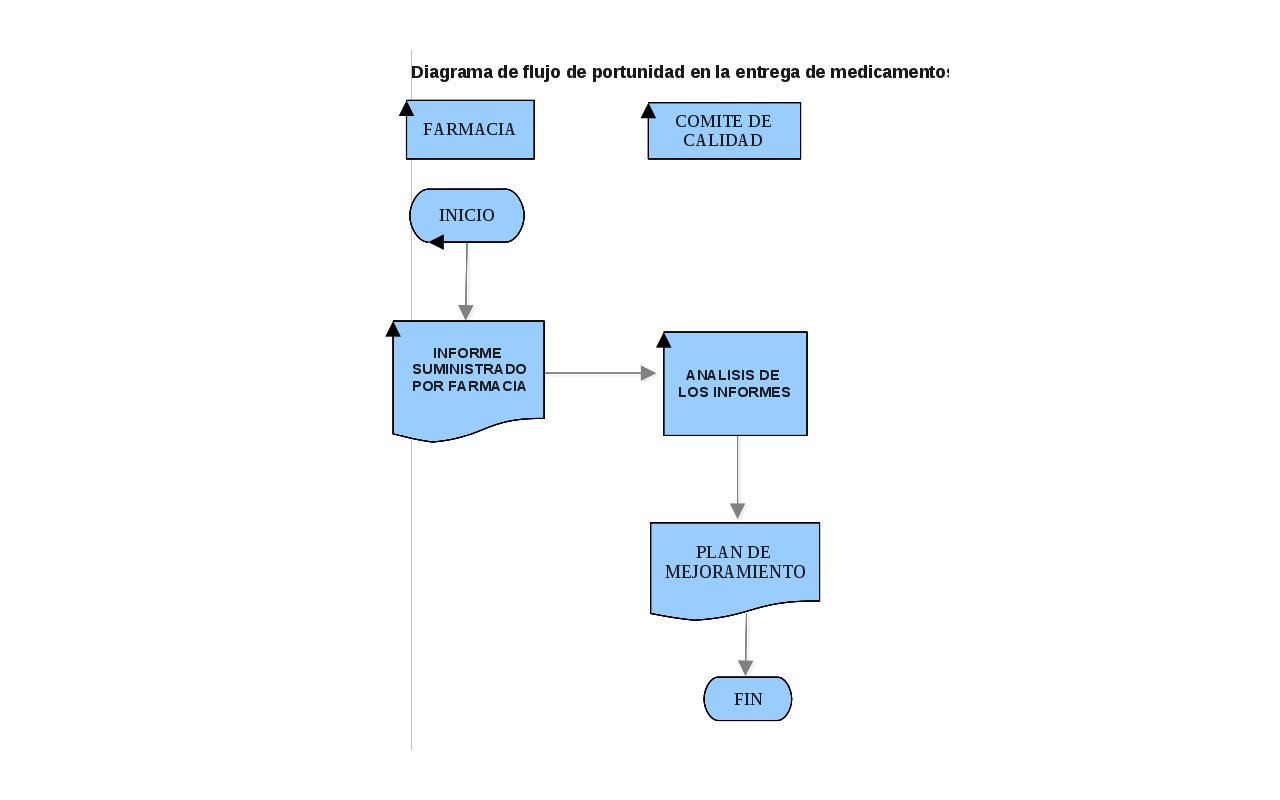
Inicio: Registro del día de solicitud del medicamento y el día.
Fin: Plan de mejoramiento |
| Descripción de los procedimientos |
Revisión de la información suministrada por el área de farmacia, según formato anexo, en cuanto a la diferencia en días entre el momento de solicitud del medicamento con previa autorización de la EPS y el día en que se entrega.
Estudio y análisis por parte del comité de calidad Plan de mejoramiento |
| Periodicidad |
Mensual |
| Estándar |
Tiempo maximo para entrega de medicamentos 15 dias |
Diagrama de Flujo de Oportunidad en la Entrega de Medicamentos
Reevaluación de programas
1) Tipo: Tasa
2) -Fuente: Protocolo del programa de evaluación del uso del medicamento en en la IPS ambulatoria ONCOMEDIC LTDA
3)-Método: Retrospectivo -
4) Muestra: Total de programas de evaluación del uso de medicamentos realizados en en la IPS
5) Responsable: Quimico Farmacéutico -
6) Frecuencia: Anual
7) Objetivo: Estimar el grado de seguimiento de los resultados de un programa de evaluación del uso de medicamentos y de las actuaciones establecidas
4) Expresión Matemática: # de revisiones del programa no realizadas x 100
No de revisiones del programa previstas
Cuadro de Procesos:
| Nombre del proceso | Gestión de calidad de los productos del servicio farmaceutico |
| Coordinador del proceso |
Director técnico servicio farmaceutico |
| Producto |
Cumplimiento de la calidad de los produductos suministrados por el servicio farmacéutico de Oncomedic limitada |
| Entrada |
Auto-control Auditoria interna Auditoria externa Queja |
| Salidas |
Liberación del producto en optimas condiciones |
| Procedimientos |
CONTROLES EN PRODUCTO TERMINADO
LISTADO DE CONTROLES:
Verificacion de hermeticidad, Verificacion de Correspondencia del producto con el paciente; Controles Microbioolgicos, Verificacion de Etiquetas; Verificacion de de resultado de Controles en proceso: pH, Conductividad del agua purificada, Gravimetria, Color; Prsencia de material en suspension en mezclas Liquidas
Nota: para Lotes de preparacion mayores a 30 unidades se tomara una muestra representativa para determinar esterilidad
Analisis Microbiologico que se le realizan al Producto Terminado
Nota: Para Lotes de preparacion mayores a 30 unidades se tomara una muestra representativa para determinar esterilidad
Esterilidad
Se realizan por medio de las Ensayos descrito en la USP o BP vigentes, que consiste en uso del reactivo LAL y recuento total de microorganismo mesofilos en placas
FRECUENCIA
Para Lotes de preparacion mayores a 30 unidades se tomara una muestra representativa para determinar esterilidad
<Auditoria de Procesos Productivos
TÉCNICA ASÉPTICA, PREPARACIÓN Y PRODUCTO TERMINADO.
El proceso de preparación es fundamental, para asegurar la calidad de cada mezcla de nutrición parenteral, porque una muestra no es extrapolable a la preparación diaria de NP, y las condiciones no siempre son las mismas, ya que estamos hablando de preparaciones magistrales, en las cuales constantemente está variando la concentración de los nutrientes y los volúmenes totales. Es por esta razón, que se hace indispensable asegurar la calidad de los procesos productivos, como un mecanismo propicio para tomar acciones preventivas, y posteriormente, acciones correctivas. La Unidad de Farmacia en los centros de salud debe contar con procedimientos operativos estándar escritos y debidamente aprobados para asegurar la calidad del entorno en el que se elaboran las mezclas de nutrición parenteral (ver capítulo 797, USP 30) El personal de preparación magistral debe verificar que los ingredientes utilizados en la elaboración de las mezclas de nutrición parenteral, tengan la identidad y calidad correctas, utilizando la información provista por los certificados de calidad de los productos, el etiquetado del producto verificando la fecha de validez de los mismos, certificados de análisis microbiológico, análisis químico directo y el conocimiento de las condiciones de almacenamiento en las instalaciones. Para cumplir con esto, se debe seguir un procedimiento escrito para la inspección física de cada unidad antes de su uso, para asegurar que estos componentes sean estériles, estén libres de defectos y sean adecuados para el uso al cual están destinados.
CALIFICACIÓN DEL PERSONAL QUE PREPARA LA NP.
(ver: Safe Practice for Parenteral Nutrition, ASPEN Board of Directors, 2004.JPEN,2004, v.28(6).U.S. Pharmacopeia National Formulary (USP 30 NF 25) , The Official Compendia of Standards (volume 1), 2007; Chapters <797> Pharmaceutical Compounding.
VALIDACIÓN DEL PROCESO DE PREPARACIÓN
La validación del proceso aséptico se puede realizar por el procedimiento de “llenado con medios de cultivo” (media fill), el mismo consiste en realizar una simulación de un procedimiento aséptico a través del uso de medios de cultivo procesados de una manera similar al procesamiento de la NP y empleando el mismo sistema de envase/cierre. De esta manera se puede evaluar la habilidad del personal, este procedimiento debe repetirse periódicamente.
Se debe considerar lo siguiente:
a. El procedimiento de llenado con medios de cultivo
b. La selección del medio de cultivo
c. El tiempo y la temperatura de incubación de la bolsa llenada con medio de cultivo
d. La inspección de las unidades llenadas
e. La documentación requerida, la interpretación de resultados y las posibles medidas correctivas requeridas
Las pruebas de llenado con medios deben representar las condiciones más exigentes o difíciles con las que el personal puede encontrarse durante la elaboración de la Nutrición Parenteral. Se puede emplear un medio multifuncional enriquecido como por ej.: “medio líquido de caseina de Soja”, que se ha controlado para la promoción de crecimiento con una batería de micro-organismos indicadores a un nivel por debajo de 100 ufc/unidad.
Procedimiento de Llenado con Medios de Cultivo
El llenado con medio de cultivo debe representar las condiciones más desfavorables para el personal durante la elaboración de la Nutrición Parenteral.
La selección del medio de cultivo – se debe utilizar un medio de cultivo que permita el desarrollo de bacterias y hongos como por ejemplo: Caldo Digerido de Caseína-Soja (Caldo tripteína soja)
Tiempo y temperatura de incubación de la bolsa llenada con medio de cultivo
Las bolsas con el medio de cultivo deben incubarse a una temperatura de 25º a 35ºC, durante 14 días.
Inspección de las unidades llenadas
Después del período de incubación, se deben inspeccionar los envases conteniendo el medio, para detectar si hubo crecimiento, si el medio desarrolla una turbidez visible dentro de los 14 días, significa que no ha pasado la prueba. Los microorganismos aislados durante el llenado de medios, se deben identificar por género y cuando sea posible por especie, con el objeto de investigar las fuentes de contaminación.
Se sugiere realizar tres operaciones de llenado con medios de cultivo durante la validación inicial del proceso de llenado aséptico y revalidar con una frecuencia mínima de 1 llenado semestral sin contaminación.
MONITOREO DE CALIDAD EN EL EQUIPAMIENTO DE LA UNIDAD
CONTROL DE EQUIPAMIENTOS:
Calibración: Este proceso se debe realizar a lo menos una vez al año y cada vez que se realicen traslados o cambios en el equipamiento o áreas o cuando existan dudas en las mediciones rutinarias. Debe ser realizado por una empresa externa que tenga sus instrumentos de medición con certificación vigente.
EQUIPAMIENTO DE FLUJO UNIDIRECCIONAL
ENSAYO DE UNIFORMIDAD DE AIRE
Se realiza para verificar el correcto funcionamiento de los filtros HEPA y del motor de la cabina, a través de un instrumento llamado Anemómetro, el cual indica la velocidad del flujo laminar en m/seg. Se testea dividiendo el filtro en 3 partes iguales hacia arriba y en 3 ó 4 partes iguales hacia el lado, dependiendo del ancho de ésta y determinando la velocidad y uniformidad del aire entregado por la misma
ENSAYO DE INTEGRIDAD Y ESTANQUEIDAD DEL FILTRO HEPA:
Se realiza para verificar la integridad del filtro y la estanqueidad de las juntas del filtro HEPA con el marco de cabina y las posibles fugas puntuales del filtro HEPA en su superficie total y uniones.
ENSAYO DE CONTAJE DE PARTICULAS
Se realiza para determinar si el numero de partículas está de acuerdo con la clase esperada, diseñada y se realiza tanto en la chamarra de flujo laminar como en la sala.
TEST DE RUIDO
Debe cumplir con los decretos ley establecidos en cada país (en Chile, corresponde al decreto 745 de la Ley 16.744, con el artículo 75° del Decreto Supremo N° 594/99 que aprueba el Reglamento sobre Condiciones Sanitarias y Ambientales Básicas en los Lugares de Trabajo, siendo el límite máximo permitido para una jornada laboral de 10 horas, de 84,03 decibeles (A) lento, sin protección auditiva). Si se utilizan las curvas NCB que entregan recomendaciones respecto de los valores de presión sonora máximos para distintos puestos y lugares de trabajo, se puede elegir la curva NCB-50 que entrega valores de ruido para espacios de trabajo en los laboratorios, expresados en frecuencia medida en Herz. 3.2.5. TEST DE LUMINOSIDAD: No debe ser inferior a 500 LUX como promedio final de las medidas realizadas.
CALIBRACIÓN PERIÓDICA DE BALANZAS
utilizadas para el control gravimétrico, de acuerdo a las especificaciones del fabricante. Certificados de calibraciones de equipos
CONTROL PERIÓDICO DEL SISTEMA AUTOMATIZADO DE LLENADO
(si corresponde): de acuerdo a las especificaciones del fabricante.
CALIBRACIÓN DEL pH-METRO
de acuerdo a las especificaciones del fabricante. Manuales de equipos
CONTROLES DE PRODUCTOS UNIDOSIS, NPT Y FORMULAS MAGISTRALES DE LA LIBERACIÓN.
INSPECCIÓN VISUAL
Todas las preparaciones deben ser inspeccionadas individualmente, en conformidad con los procedimientos escritos, para que de esta manera, se detecte la presencia de partículas visibles u otros elementos extraños inmediatamente después de terminar la preparación y como condición para su liberación. Deben ser inspeccionadas cuanto a precipitación y separación de fases y cambio de color. Cualquier producto con defectos observados, debe descartarse inmediatamente, para impedir su administración accidental a los pacientes. Además, es importante que antes de la administración, el profesional a cargo de ésta, inspeccione la preparación para observar si se ha producido precipitación, turbidez o alguna reacción anormal que indique la posibilidad de presentarse una incompatibilidad en la mezcla.
Control de Etiquetado
Se realiza revisión de cada etiqueta contra la receta, antes de que éstas sean ingresadas al área de preparación. Es también necesario que cada unidad de nutrición parenteral posea más de una etiqueta, una que se pegue directamente en la bolsa del preparado (envase primario), la otra que se presente en el envase secundario de la preparación (bolsa estéril protectora) y otra para pegar en la historia clínica como control y testigo de la administración al paciente, por parte de la enfermera.
Personal
- Instrucción sobre los principios básicos de microbiología, fisiología microbiana, desinfección y saneamiento.
- Capacitación adicional para efectuar la recolección de los datos de control ambiental.
- Entregar el conocimiento de los procedimientos operativos estándares referentes a medidas correctivas que se toman cuando las condiciones ambientales así lo requieran.
- La enseñanza de las políticas de cumplimiento reglamentario y las responsabilidades de cada individuo, en lo que se refiere a buenas practicas de preparación (BPP).
- Control microbiologico
Validación del Proceso de Preparación
Procedimiento de Llenado con Medios de Cultivo
La validación del proceso aséptico se puede realizar por el procedimiento de “llenado con medios de cultivo” (media fill), el mismo consiste en realizar una simulación de un procedimiento aséptico a través del uso de medios de cultivo procesados de una manera similar al procesamiento de la NP y empleando el mismo sistema de envase/cierre. De esta manera se puede evaluar la habilidad del personal, este procedimiento debe repetirse periódicamente.
Se debe considerar lo siguiente:
a. El procedimiento de llenado con medios de cultivo
b. La selección del medio de cultivo
c. El tiempo y la temperatura de incubación de la bolsa llenada con medio de cultivo
d. La inspección de las unidades llenadas
e. La documentación requerida, la interpretación de resultados y las posibles medidas correctivas requeridas
Las pruebas de llenado con medios deben representar las condiciones más exigentes o difíciles con las que el personal puede encontrarse durante la elaboración. Se puede emplear un medio multifuncional enriquecido como por ej.: “medio líquido de caseina de Soja”, que se ha controlado para la promoción de crecimiento con una batería de micro-organismos indicadores a un nivel por debajo de 100 ufc/unidad.
El llenado con medio de cultivo debe representar las condiciones más desfavorables para el personal durante la elaboración de la Nutrición Parenteral.
La selección del medio de cultivo – se debe utilizar un medio de cultivo que permita el desarrollo de bacterias y hongos como por ejemplo: Caldo Digerido de Caseína-Soja (Caldo tripteína soja)
Tiempo y temperatura de incubación de la bolsa llenada con medio de cultivo
Las bolsas con el medio de cultivo deben incubarse a una temperatura de 25º a 35ºC, durante 14 días.
Inspección de las unidades llenadas
Después del período de incubación, se deben inspeccionar los envases conteniendo el medio, para detectar si hubo crecimiento, si el medio desarrolla una turbidez visible dentro de los 14 días, significa que no ha pasado la prueba. Los microorganismos aislados durante el llenado de medios, se deben identificar por género y cuando sea posible por especie, con el objeto de investigar las fuentes de contaminación.
Se sugiere realizar tres operaciones de llenado con medios de cultivo durante la validación inicial del proceso de llenado aséptico y revalidar con una frecuencia mínima de 1 llenado semestral sin contaminación.
Referencias Bibliográficas:
Campbell SM, Braspenning J, Hutchinson A, Marshall M. Research methods used i
Marshall MN, Shekelle PG, McGlynn EA, Campbell S, Brook RH, Roland MO. Can
Cipriano SL. Proposta de um conjunto de indicadores para utilização na Farmaci
Santó MM.; Lacasa Díaz, C y col. “Programa de Garantía de Calidad en el Servicio
Santó MM.; Lacasa Díaz, C y col. “Programa de Garantía de Calidad en el Servicio
Font I., López E., Ordovás JP., Ruiz C., Sirvent M. Evaluación y mejora de la calidad
Traverso ML, Salamano MC, Pérez B, Botta CA, Sopranzetti V, Campella M.
Pérez Romero M. Servicios Farmacéuticos Hospitalarios Cubanos. Diagnóstico de
Cuba MM, Monzón AL, Pérez M. Necesidad de un programa de calidad para los
Cuba MM. Calidad de los Servicios Farmacéuticos Hospitalarios. Rev Cubana
Ardón N, Cubillos AF. Sistema para el Monitoreo de la Calidad de la Atención en
Massip C, Ortiz RM, Llantá MC, Peña M; Ochoa I. La evaluación de la satisfacción
Sociedad Española de Farmacia Hospitalaria. “Guía de Gestión de los Servicios de
Hospital Accreditation Standards. Joint Commission on Accreditation of Healthcare
Allen J, Dyas J, Jones M. Building consensus in health care: a guide to using the
Campbell SM, Cantrill JA, Richards D. Prescribing indicators for UK general