Diferencia entre revisiones de «Farmacovigilancia»
| Línea 56: | Línea 56: | ||
= Introducción: = | = Introducción: = | ||
Oncomedic Ltda. implementa su Programa de Farmacovigilancia como parte esencial del Sistema Institucional de Información sobre Medicamentos. Este programa busca garantizar el uso seguro, efectivo y racional de los medicamentos, mediante la identificación, análisis y gestión de riesgos asociados al proceso farmacoterapéutico. | |||
El programa se desarrolla de forma articulada con las directrices del Programa Nacional de Farmacovigilancia del INVIMA, las Secretarías de Salud y los lineamientos de la Organización Mundial de la Salud (OMS), con el propósito de mejorar la seguridad del paciente, prevenir eventos adversos evitables y contribuir a la calidad de la atención en salud. | |||
La OMS, a través de su campaña global “Medicación sin daño”, ha señalado que los errores de medicación causan más de 1,3 millones de muertes prevenibles cada año y representan un costo mundial estimado en más de US$ 42.000 millones. En Colombia, se ha fortalecido el marco normativo e institucional para enfrentar estos riesgos, reconociendo que hasta un 67% de las prescripciones pueden contener errores y que cerca del 12% de las consultas en urgencias están relacionadas con medicamentos, siendo hasta un 70% de estos casos prevenibles. | |||
En | |||
== Política de Farmacovigilancia – Oncomedic Ltda. == | |||
Oncomedic Ltda. se compromete a implementar y mantener un Programa de Farmacovigilancia institucional robusto, enfocado en la seguridad del paciente y la calidad del uso de medicamentos, mediante las siguientes acciones: | |||
* Garantizar el suministro y uso de medicamentos que cumplan con estándares de calidad, seguridad y eficacia, en concordancia con la normativa vigente. | |||
* Establecer mecanismos efectivos para la identificación, notificación, análisis, intervención y seguimiento de reacciones adversas, eventos adversos y errores de medicación. | |||
* Promover la capacitación continua del talento humano en el reconocimiento y manejo de riesgos asociados a la farmacoterapia. | |||
* Fomentar una cultura institucional de farmacovigilancia, basada en el reporte voluntario, oportuno, veraz y no punitivo de eventos adversos. | |||
* Consolidar y remitir la información requerida a las autoridades sanitarias competentes, en especial al INVIMA, como parte del Sistema Nacional de Farmacovigilancia. | |||
* Integrar el programa a los procesos institucionales de calidad, seguridad del paciente y gestión del riesgo, con el fin de disminuir los eventos adversos prevenibles y mejorar los desenlaces clínicos. | |||
Esta política reafirma el compromiso de Oncomedic Ltda. con la salud y bienestar de sus pacientes, mediante el uso seguro y responsable de los medicamentos, la vigilancia activa del riesgo farmacoterapéutico y la mejora continua de la atención en salud. | |||
= Objetivos = | = Objetivos = | ||
Revisión del 22:12 25 jun 2025
Regresar a Servicio Farmacéutico
Identificación
|
Nombre |
Código |
|||
|
Manual del Programa de Fármaco-Vigilancia |
MPF3 | |||
|
Fecha de Emisión |
Fecha de Actualización |
Versión | ||
|
2010/04/01 |
2022-08-31 |
5 | ||
Elaboro Ultima versión: Químico Farmacéutico
Reviso y Autorizo Ultima Versión: Comite de Farmacia y Terapéutica
Introducción:
Oncomedic Ltda. implementa su Programa de Farmacovigilancia como parte esencial del Sistema Institucional de Información sobre Medicamentos. Este programa busca garantizar el uso seguro, efectivo y racional de los medicamentos, mediante la identificación, análisis y gestión de riesgos asociados al proceso farmacoterapéutico.
El programa se desarrolla de forma articulada con las directrices del Programa Nacional de Farmacovigilancia del INVIMA, las Secretarías de Salud y los lineamientos de la Organización Mundial de la Salud (OMS), con el propósito de mejorar la seguridad del paciente, prevenir eventos adversos evitables y contribuir a la calidad de la atención en salud.
La OMS, a través de su campaña global “Medicación sin daño”, ha señalado que los errores de medicación causan más de 1,3 millones de muertes prevenibles cada año y representan un costo mundial estimado en más de US$ 42.000 millones. En Colombia, se ha fortalecido el marco normativo e institucional para enfrentar estos riesgos, reconociendo que hasta un 67% de las prescripciones pueden contener errores y que cerca del 12% de las consultas en urgencias están relacionadas con medicamentos, siendo hasta un 70% de estos casos prevenibles.
Política de Farmacovigilancia – Oncomedic Ltda.
Oncomedic Ltda. se compromete a implementar y mantener un Programa de Farmacovigilancia institucional robusto, enfocado en la seguridad del paciente y la calidad del uso de medicamentos, mediante las siguientes acciones:
- Garantizar el suministro y uso de medicamentos que cumplan con estándares de calidad, seguridad y eficacia, en concordancia con la normativa vigente.
- Establecer mecanismos efectivos para la identificación, notificación, análisis, intervención y seguimiento de reacciones adversas, eventos adversos y errores de medicación.
- Promover la capacitación continua del talento humano en el reconocimiento y manejo de riesgos asociados a la farmacoterapia.
- Fomentar una cultura institucional de farmacovigilancia, basada en el reporte voluntario, oportuno, veraz y no punitivo de eventos adversos.
- Consolidar y remitir la información requerida a las autoridades sanitarias competentes, en especial al INVIMA, como parte del Sistema Nacional de Farmacovigilancia.
- Integrar el programa a los procesos institucionales de calidad, seguridad del paciente y gestión del riesgo, con el fin de disminuir los eventos adversos prevenibles y mejorar los desenlaces clínicos.
Esta política reafirma el compromiso de Oncomedic Ltda. con la salud y bienestar de sus pacientes, mediante el uso seguro y responsable de los medicamentos, la vigilancia activa del riesgo farmacoterapéutico y la mejora continua de la atención en salud.
Objetivos
Objetivo General
Prevenir en el usuario la presencia de eventos adversos relacionados con medicamentos asi como detección, análisis y notificación de los mismos contribuyendo en el uso seguro, adecuado y efectivo de los farmacos durante el proceso de atención.
Objetivos Específicos
1.Realizar un diagnóstico de las condiciones de manejo y utilización de los medicamentos.
2.Identificar, detectar y cuantificar los problemas relacionados con medicamentos (PRM).
3.Identificar causas e implementar las acciones necesarias para prevenir y resolver los PRM detectados.
4.Implementar mecanismos que permitan involucrar al personal asistencial en el análisis de los PRMs reportados.
5.Identificar, caracterizar y abordar los problemas relacionados con la utilización de medicamentos (PRUM), tomando como base la clasificación general de los PRM
6.Implementar estrategias de orientación, información y educación al usuario y/o su familia en relación con el uso y administración de medicamentos
7.Contribuir a la elección de la mejor opción posible de medicamentos con énfasis en el costo-efectividad
Alcance
El programa de farmacovigilancia inicia con la adecuada gestión de proveedores, la adquisición, recepción de los medicamentos, su optimo almacenamiento, adecuación y distribución, la educación al paciente, la administración idónea tanto en la sala de aplicación como por parte del paciente de acuerdo a las instrucciones de prescripción y a los protocolos establecidos, el seguimiento a los pacientes para verificar los efectos de los medicamentos, identificación de los eventos adversos y las RAMs esperadas y no esperadas para controlarlas, analizarlas establecer posibles factores causales emprender planes de mejoramiento y realizar lo reporte los organismos de control
Marco conceptual
Sustento Legal
- Decreto 677 1995 por el que se reglamentan las licencias y control de calidad de los medicamentos
- Resolución 1403 DE 2007 del Ministerio de la Protección Social por los que se reglamentan los servicios farmacéuticos, la atención farmacéutica y se describen las reacciones adversas. .
- El Decreto 780 de 2016 que compila y simplifica todas las normas reglamentarias preexistentes en el sector de la salud, tiene como objetivo racionalizar las normas de carácter reglamentario que rigen en el sector y contar con un instrumento jurídico único.
- Resolución 003100 de 2019 por la cual se definen los procedimientos y condiciones de inscripción de los prestadores de servicios de salud y de habilitación de los servicios de salud y se adopta el Manual de Inscripción de Prestadores y Habilitación de Servicios de Salud.
- Circular externa N.º 3000-0526-2021. se emiten los lineamientos de articulación del Programa Nacional de Farmacovigilancia para el reporte de eventos adversos a través del sistema VigiFlow®
Marco Referencial
- Evento adverso: Cualquier suceso médico desafortunado que puede presentarse durante el tratamiento con un medicamento, pero que no tiene necesariamente una relación causal con dicho tratamiento
- Evento adverso serio: Se considera serio un evento adverso cuando su desenlace es la muerte o una amenaza a la vida, o cuando genera o prolonga una hospitalización, causa discapacidad, interrupción del embarazo o malformaciones.
- Evento adverso inesperado: Es aquel del cual no se tiene un conocimiento previo hasta la fecha de su ocurrencia por no haber sido consignado en la información de seguridad de un medicamento.
- Farmacovigilancia: Ciencia y actividades relacionadas con la detección, evaluación, entendimiento y prevención de los eventos adversos o cualquier otro problema relacionado con medicamentos.
- Problema Relacionado con Medicamentos: Problemas de salud entendidos como resultados clínicos negativos, derivados de la farmacoterapia que, producidos por diversas causas, conducen a la no consecución del objetivo terapéutico o a la aparición de efectos no deseados.
Clasificación de los problemas relacionados con los medicamentos: Los problemas relacionados con medicamentos (PRM), se clasifican en: Relacionados con la necesidad. Relacionados con la efectividad. Relacionados con la seguridad.
Relacionados con la necesidad:
- PRM 1: El paciente sufre un problema de salud consecuencia de no recibir una medicación que necesita.
- PRM 2: El paciente sufre un problema de salud consecuencia de recibir un medicamento que no necesita
Relacionados con la efectividad: - PRM 3: El paciente usa un medicamento que está mal seleccionado.
- PRM 4: El paciente usa una dosis, pauta y/o duración inferior a la que necesita.
Relacionados con la seguridad:El paciente usa un medicamento que está mal seleccionado: - PRM 5: El paciente usa una dosis, pauta y/o duración superior a la que necesita.
- PRM 6: El paciente usa un medicamento que le provoca una Reacción Adversa a Medicamentos.
Nota aclaratoria: Un medicamento es necesario cuando ha sido prescrito o indicado para un problema de salud concreto que presenta el paciente. Un medicamento es inefectivo cuando no alcanza suficientemente los objetivos terapéuticos esperados. Un medicamento es inseguro cuando produce o empeora algún problema de salud. Un PRM se considera cuantitativo cuando depende de la magnitud de un efecto.
- Problemas relacionados con la utilización de medicamentos (PRUM): Corresponden a causas prevenibles de problemas relacionados con medicamentos (factores de riesgo) asociados a errores de medicación (prescripción, dispensación, administración o uso por parte del paciente o cuidador), incluyendo los fallos en el sistema de suministro de medicamentos, relacionados principalmente con la ausencia en los servicios de procesos administrativos y técnicos que garanticen la existencia de medicamentos que realmente se necesiten, acompañados de las características de efectividad, seguridad, calidad de la información y educación necesaria para su uso correcto.
Clasificación de los problemas relacionados con la utilización de medicamentos (PRUM): Los problemas relacionados con la utilización de medicamentos se pueden clasificar de la siguiente forma:
- Relativos a la disponibilidad
- Relativos a la calidad Relativos a la prescripción
- Relativos a la dispensación
- Relativos a la administración
- Relativos al uso
- Reportante primario: Es el profesional de la salud que entra en contacto directo con el paciente, identifica un Problema Relacionado con Medicamentos o Evento Adverso y lo informa al titular de registro sanitario y/o al fabricante.
- Reporte: Es el medio por el cual un reportante notifica sobre un evento adverso sucedido a un paciente, a un sistema de farmacovigilancia.
- Señal: La información reportada sobre una posible relación causal entre un evento adverso y un fármaco, siendo desconocida o incompletamente documentada previamente. Usualmente más de un único reporte se requiere para generar una señal, dependiendo de la severidad del evento y de la calidad de la información.
- VIGIFLOW: Se trata de un programa que funciona como la base de datos en farmacovigilancia de su país. VigiFlow permite la recolección, procesamiento y análisis de reportes de Reacción Adversa a medicamentos (RAM) y de Eventos Supuestamente Atribuibles a la Vacunación o a la Inmunización, además de contar con la característica de poder compartir éstos con la base de datos mundial de la OMS-UMC u otros centros nacionales.
- MedDRA:* Es la única terminología médica disponible en VigiFlow. Ésta será usada para reportar reacciones adversas, indicaciones de medicamentos, historial médico, causa de muerte, exámenes de laboratorio/gabinete y diagnósticos.
Metodología de Diseño e Implementación del Programa
Compromiso de la Dirección
Salud@rte oncomedic y todo su equipo de trabajo se compromete a velar por el suministro de medicamentos en forma segura, eficaz y de calidad, verificando y controlando su correcta gestión desde los procesos de adquisición, recepción, adecuación, dispensación, con acciones de prevención, educación, control, identificación, reporte, estudio y analisis de las reacciones adversas asociadas a los medicamentos.
Diagnóstico y Autoevaluación Organizacional
La gestión de los medicamentos en Salud@rte oncomedic es fundamental debido a la complejidad de los principios activos que se manejan, su alta toxicidad y el estrecho margen terapéutico, sumado al deterioro de las condiciones de salud de los pacientes que se atienden y a la convergencia de modalidades terapéuticas en las que se tienen que incluir medidas no farmacológicas que pueden incrementar los efectos tóxicos de los medicamentos por tal razon es de fundamental importancia establecer los factores de riesfo para cada paciente tomando en cuenta la clasificación de los problemas relacionados con los medicamentos que se pueden encontrar:
Relacionados con la Necesidad.
PRM 1: La efectividad de los medicamentos antineoplasicos es mas adecuada en la medida en que se administren de acuerdo a los tiempos establecidos en los protocolos, cuando esto no ocurre la respuesta a la terapéutica instaurada se reduce con consecuencias para la sobre-vida del paciente, la falta de aplicación en los tiempos apropiado en la organización se presenta por diversas causas entre las que se pueden citar:
- Falta de acceso a los servicios médicos por asuntos administrativo
- Falta de acceso a los servicios médicos por asuntos de orden asistencial
- Abandono del tratamiento
PRM 2: El paciente sufre un problema de salud consecuencia de recibir un medicamento que no necesita
Relacionados con la Efectividad:
PRM 3: El paciente sufre un problema de salud consecuencia de una inefectividad no cuantitativa de la medicación.
PRM 4: El paciente sufre un problema de salud consecuencia de una inefectividad cuantitativa de la medicación.
Relacionados con la seguridad:
PRM 5: El paciente sufre un problema de salud como consecuencia de una inseguridad no cuantitativa de un medicamento
PRM 6: El paciente sufre un problema de salud consecuencia de una inseguridad cuantitativa de un medicamento
Coordinación del Programa y Funciones del Coordinador
El coordinador del programa de farmacovigilancia es el químico farmacéutico de calidad encargado de
- Liderar los procesos y gestión de los medicamentos al interior de la organización
- Insentivar una cultura del reporte y la notificación de eventos adversos generados por medicamentos en la organización
- Realizar la debida gestión de las sospechas de reacciones adversas.
- Elaboración y/o revisión de informes periódicos de seguridad del uso de los medicamentos dentro de oncomedic ltda y de ser necesario las demás instituciones contratantes
- Revisión periódica de la literatura científica sobre reacciones adversas espontáneas a los principios activos usados en la organización
- Realizar informes a los organismos de control frente a los temas de seguridad de medicamentos.
Estrategias, Acciones y Responsable
Prevención de la Ocurrencia de Eventos Adversos
Relacionados con la Necesidad.
PRM 1: Para lograr la mayor efectividad de los medicamentos antineoplasicos y la aplicación en los tiempos apropiado que permitan reducir este tipo de PRM la organización realiza las siguientes actividades
- Falta de acceso a los servicios médicos por asuntos administrativos: Oncomedic limitada a ideado un plan de trabajo donde el servicio asistencial esta pendientes de los tratamientos requeridos por los pacientes y los tiempos que toman los tramites administrativos de modo que se reduzca el riesgo de este problema, de igual manera contamos con personal a cargo de facilitar el proceso de autorización en las diferentes instituciones.
- Falta de acceso a los servicios médicos por asuntos de orden asistencial: El recurso humano en oncología es de alto costo y especificidad, en algunos casos es difícil acceder a el, por tal motivo Oncomedic a ideado un modelo de prestación de servicios en red con diferentes profesionales del área, así como un triage que permita dirigir a los usuarios a los servicios que requiere.
- Abandono del tratamiento: La educación es el pilar fundamental para que se presente con poca frecuencia esta situación, sin embargo después de explicar al paciente toda la situación se permite al paciente tomar la decisión y se respeta cualquiera que ella sea
PRM 2: El paciente sufre un problema de salud consecuencia de recibir un medicamento que no necesita, este problema se reduce al máximo mediante el seguimiento de los protocolos establecidos para las respectivas patologías que se manejan en nuestra institución, el personal conoce estos protocolos y verifica las inconsistencias que se pueden presentar en la formulación o preparación de los mismos, existen múltiples filtros que permiten reducir el riesgo
Relacionados con la Efectividad:
PRM 3: El paciente sufre un problema de salud como consecuencia de una inefectividad no cuantitativa de la medicación
Para reducir este problema en nuestra institución solo se reciben procesan y administran medicamentos que cumplan con los estándares de calidad suministrados por el INVIMA para cada caso se cuenta con la adecuada parametrización de los mismos y un exhaustivo control al momento de realizar la recepción de los medicamentos al servicio farmacéutico
PRM 4: El paciente sufre un problema de salud consecuencia de una inefectividad cuantitativa de la medicación, esta situación se reduce al máximo al utilizar los protocolos de preparación de medicamentos en dosis unitarias
Relacionados con la seguridad:
PRM 5: El paciente sufre un problema de salud como consecuencia de una inseguridad no cuantitativa de un medicamento, esta situación se reduce al máximo al utilizar los protocolos de preparación de medicamentos en dosis unitarias y la administración de los mismos con adecuadas medidas de control
PRM 6: El paciente sufre un problema de salud consecuencia de una inseguridad cuantitativa de un medicamento, esta situación se reduce al máximo al utilizar los protocolos de preparación de medicamentos en dosis unitarias y la administración apropiada de los mismos
Educación al paciente
Adicionalmente para la prevención del PRUM durante la dispensación de los medicamentos que se administran por vía oral el personal del servicio farmacéutico da instrucciones a los usuarios para su correcta administración, de igual a manera los pacientes que reciben medicamentos por via parenteral se les da instrucciones sobre los efectos, señales de alarma y medidas de prevención
Identificación y Gestión de Eventos Adversos
| Nombre del Procedimiento |
Vigilancia de eventos adversos asociados a medicamentos . |
| Responsable |
Químico Farmacéutico |
| Alcance |
Inicio: Reporte de los eventos adversos ocurridos durante y posterior al tratamiento instaurado Búsquedas activas, Búsquedas pasivas |
| Descripción de los procedimientos |
|
| Periodicidad |
Mensual |
| Estándar |
100% Numerador:Numero de eventos adversos gestionados X 100 Numero de eventos adversos presentados |
Formato de Registro de RAM
Ir al Programa de Seguridad del Paciente para ver protocolo de Londres e información adicional sobre el manejo de eventos adversos
Seguimiento de Alertas Sanitarias
Se realiza una verificación de los medicamentos y dispositivos médicos ingresando al portal www.invima.gov.co dentro de los links de farmaco y tecnovigilancia a fin de verificar la seguridad de dispositivos médicos y medicamentos usados así mismo se realiza seguimiento de las alertas enviadas a los correos organizacionales por los organismos de control.
- Periodicidad de la verificación: Semanal
- Las alertas se consolidan en el Formato de Consolidado de alertas sanitarias INVIMA”
- Seguimiento: Una vez sea detectada una alerta positiva se informa al encargado de la solicitudes de compra (gerencia comercial) y recepción de medicamentos y dispositivos para evitar la adquisición de este producto, en caso de tener en stock este producto se realizara el respectivo informe al dueño del producto, a los organismos de control y al laboratorio para su recolección, en caso de haber sido usado se realizara el reporte a fin de realizar vigilancia del caso.
- Se divulgaran las alertas sanitarias pertinentes mediante Comité de Farmacia y terapéutica y por correo electrónico interno de la organización, para el conocimiento general.
Reporte aplicativo VIGIFLOW.
De acuerdo a la normatividad vigente con el reporte de eventos adversos, en Colombia se ha habilitado un aplicativo para este fin, permite la recolección, procesamiento y análisis de reportes de eventos adversos no solo de nuestra organización, sino de todo el país y el mundo.
Para el registro se tienen que seguir estos pasos:
1. Ingresar al aplicativo desde el siguiente link: https://vigiflow.who-umc.org
2. Introducir usuario y clave asignados.
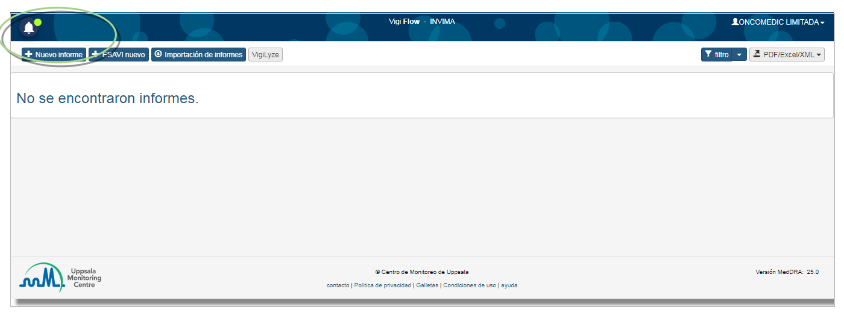
3. Generar nuevo informe, para desplegar todos los ítems necesarios para el reporte.
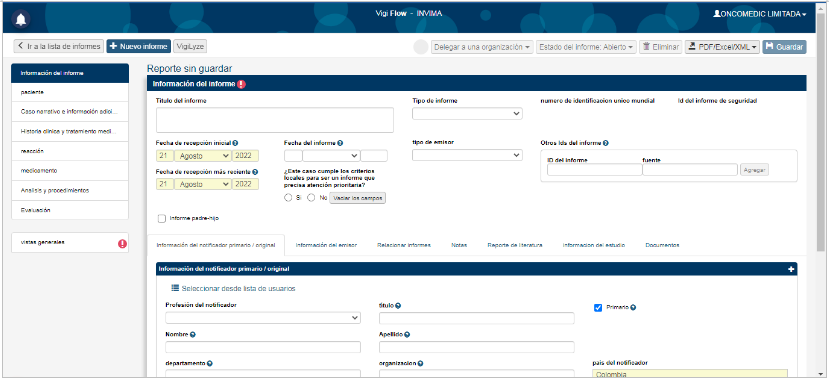
4. Diligenciar los campos con la información encontrada y recopilada del evento a reportar. Al llenar los campos se puede ir guardando el progreso del reporte. Esto con el fin de reportar la información primaria y luego de que se realice el análisis en el comité se ingresa este resultado, dentro de los tiempos establecidos por el INVIMA.
Finalizado todo este proceso se envía el caso desde esta plataforma hacia los centros de estudio.
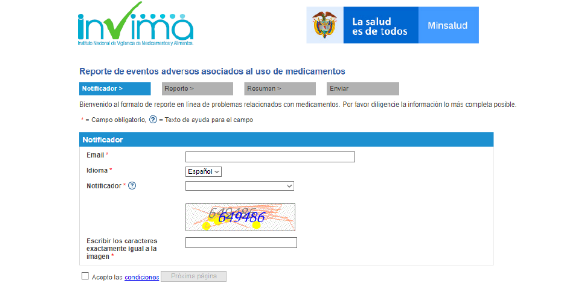
Reporte eReporting:
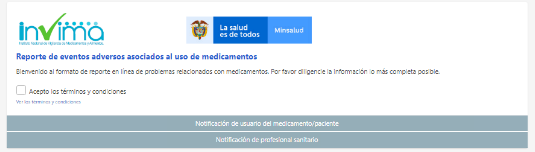
Una opción complementaria para VigiFlow, es una forma estandarizada para reportar reacciones adversas a medicamentos a través de internet, desarrollada por el UMC para facilitar el reporte de estos eventos desde pacientes y profesionales de la salud. ▪ El reporte se transmite directamente a VigiFlow . ▪ La información ingresada a través de eReporting es colocada automáticamente en los campos correspondientes en VigiFlow. ▪ eReporting reduce la necesidad de ingresar información manualmente en los centros nacionales o en la autoridad encargada de farmacovigilancia. Link de ingreso: https://primaryreporting.who-umc.org/CO
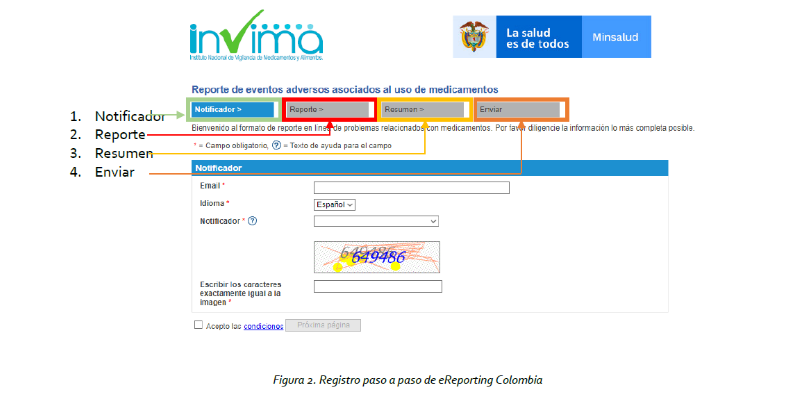
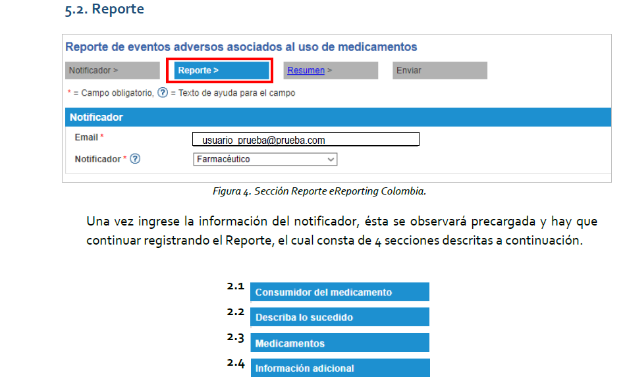
1. Diligenciar los datos requeridos en cada pestaña.
2. Detallado del paso a paso.
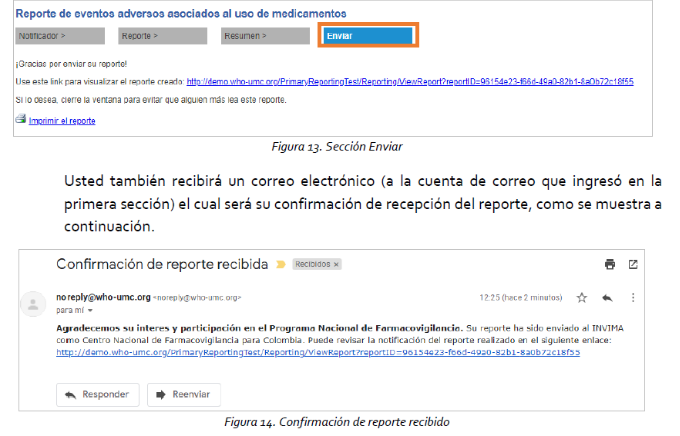
3. Finalizado el diligenciamiento se envía y se confirma el recibido de la información al correo ingresado al inicio.
Resultado Esperado, Indicadores y Metas
Gestionar los Eventos Adversos Asociados a Medicamentos
- Indicador: Gestión de Eventos Adversos
- Periodicidad: Mensual
- Unidad de medida: porcentaje
- Numerador: Numero de Eventos Adversos presentados
- Denominador: Numero de eventos Adversos Gestionados
- Meta: 100% de los eventos adversos identificados y reportados
Notificaciones al INVIMA
- Tipo: Tasa.
- Fuente: Notificaciones de RAM enviadas al CDF -
- Método: Retrospectivo. -
- Muestra: Total de notificaciones tramitadas -
- Responsable: Quimico Farmacéutico. -
- Frecuencia: Anual
- Objetivo: Estimar la eficacia del Servicio Farmaceutico en la evaluación y notificación de las reacciones adversas a medicamentos (RAM) detectadas en en la IPS
- Expresión Matemática: # de notificaciones de RAM no evaluables x 100
No de notificaciones de RAM tramitadas
Detección de RAM
- Tipo: Tasa.
- Fuente: Prescripciones médicas, fichas farmacoterapéuticas -
- Método: Concurrente
- Muestra: Total de prescripciones alertantes con intervención farmacéutica -
- Responsable: Farmacéutico -
- Frecuencia: Anual
- Objetivo: Estimar la eficacia del SF en la detección de las RAM no detectadas o comunicadas en la IPS
- Expresión Matemática:# de pacientes con sospecha de RAM no comunicada x 100
No pac. con prescripción alertantes e intervención farmacéutica
Tiempo de Ejecución y Fecha de Revisión del Programa
El programa de farmacovigilancia es un programa permanente que se evalúa mensualmente en el comité de farmacia y terapéutica y anualmente en el comité de calidad donde presenta los resultados obtenidos y las nuevas metas.
Diagrama de flujo
Bibliografía
- https://mail-attachment.googleusercontent.com/attachment/u/0/?ui=2&ik=c574f64541&view=att&th=140e9ae4302d4eba&attid=0.1&disp=inline&realattid=f_hl6q78d20&safe=1&zw&saduie=AG9B_P80aAmszgLpJ3kh0hpl2EuI&sadet=1378310079441&sads=A4kHKPhZcYoMAMN_EEz_AQ8tXiI&sadssc=1
- http://www.anmat.gov.ar/farmaco/GUIA_BPFV.pdf
- https://www.dssa.gov.co/images/vacunacion/farmacovigilancia/Instructivo_Reporte_de_PRM_por_parte_de_Pacientes_y_otros_actores_del_Sistema_de_Salud_Colombiano_eReporting.pdfhttps://who-umc.org/media/165645/1-introduccion-y-caracteristicas-basicas-de-vigiflow.pdf