|
|
| (No se muestran 24 ediciones intermedias del mismo usuario) |
| Línea 1: |
Línea 1: |
| = Introduccion =
| | [[Proceso de consulta especializada|Regresar a Consulta Especializada]] |
|
| |
|
| <br>El cáncer broncogénico es la primera causa de muerte por cáncer en Estados Unidos y Europa. En Colombia es la tercera causa de muerte por cáncer en los hombres después de estómago y de próstata y la cuarta en las mujeres después de estómago, cuello uterino y seno. En el mundo el cáncer pulmonar exhibe un franco ascenso en su incidencia en el sexo femenino. Igualmente, en la mujer colombiana el cáncer pulmonar seguramente encuentra en incremento, y tal vez sobrepase pronto aun al cáncer mamario, muy seguramente como resultado del hábito de fumar. Las tasas de incidencia se incrementan con la edad, a partir de los 40 años. Las regiones de más alta mortalidad por cáncer pulmonar son Antioquia, con énfasis en Medellín, Caldas, con énfasis en Manizales, Risaralda, principalmente Pereira (en hombres), y Quindío (en mujeres). El cigarrillo es un factor etiológico importante en el cáncer de pulmón y la tasa de mortalidad aumenta en relación directa con la intensidad del tabaquismo. También son factores etiológicos la contaminación ambiental y algunos agentes químicos y físicos, tales como asbesto, radón, arsénico, radiación ionizante, níquel, berilio, compuestos de cromo, alquitranes y otros agentes de reconocido potencial carcinogénico. El pronóstico del cáncer pulmonar es ominoso. Globalmente, apenas alrededor de 10-15% de los pacientes sobreviven 5 años, tasa que se mantiene sin mayor modificación desde hace medio siglo. Sin embargo, los cánceres en estados tempranos son de relativo buen pronóstico y se les puede ofrecer tratamiento quirúrgico, con una expectativa de supervivencia a largo plazo del orden de 60%. El carcinoma del pulmón es un tumor de gran agresividad que presenta extensión linfática en el momento del diagnóstico en más o menos la mitad de los casos, la cual es muy común en los carcinomas anaplásicos de células pequeñas, donde ocurre con una frecuencia del 80%; se presenta con frecuencia decreciente en los tumores de células gigantes, adenocarcinomas y carcinomas escamocelulares.
| | [[Procedimiento_de_Evaluaci%C3%B3n_y_Adopci%C3%B3n_de_Guias_de_Practica_Cl%C3%ADnica|Regresar a Procedimiento de evaluación de guías de practica clínica]] |
|
| |
|
| = HISTOPATOLOGÍA = | | = Identificación = |
|
| |
|
| <br>Universalmente se ha utilizado la clasificación establecida por la Organización Mundial de la Salud (OMS 1967, 1982). Los carcinomas del pulmón se dividen en dos grandes grupos clínicos que reflejan las diferencias en la biología y el manejo: cáncer de célula pequeña y los de célula no pequeña. Cerca del 80% son del tipo de célula no pequeña. Los dos tipos difieren en histología y pronóstico clínico, pero en realidad estas categorías pueden coexistir, lo que sugiere un origen común para todos los tipos de cáncer pulmonar. | | {| width="665" cellspacing="0" cellpadding="4" |
| | |- valign="TOP" |
| | | width="129" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" rowspan="4" | |
| | <br> [[Image:Oncomedic.png]]<br> |
|
| |
|
| CLASIFICACIÓN HISTOLÓGICA DE TUMORES MALIGNOS EPITELIALES DEL PULMÓN CLASIFICACIÓN DE LA ORGANIZACIÓN CLASIFICACIÓN PROPUESTA MUNDIAL DE LA SALUD WHO (1981) En el INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) (tomada de Rosai, Saldana) Carcinoma de células escamosas Carcinoma de células escamosas (carcinoma epidermoide) (carcinoma epidermoide). Variante: fusocelular Bien, moderado y mal diferenciado (Grados I, II y III respectivamente) Carcinoma basaloide Carcinoma escamoso<br> fusocelular Carcinoma de célula pequeña Carcinoma de células neuro-endocrinas. Carcinoma de células en avena Carcinoma de células en avena, Carcinoma tipo célula intermedia indiferenciado (Grado IV) Carcinoma combinado con células en Carcinoma de célula grande Avena neuroendocrina (Grado III) Carcinoma tipo célula intermedia Célula madre Célula glandular Célula escamosa CA. ESCAMOSO CA. CÉLULA GRANDE INDIFERENCIADO CA. BRONQUIOLOALVEOLAR ADENOCARCINOMA TUMORES MIXTOS CA. CÉL. PEQUEÑA CARCINOIDE TÍPICO CARCINOIDE ATÍPICO Célula de Kultschitsky 273 CÁNCER BRONCOGÉNICO (carcinoide atípico- Grado II) Carcinoide típico (Grado I) Carcinoma combinado con células en avena (menos de 5% de carcinoma escamoso o adenocarcinoma) Adenocarcinoma Adenocarcinoma Adenocarcinoma acinar Adenocarcinoma acinar Adenocarcinoma papilar Adenocarcinoma papilar Carcinoma bronquiolo-alveolar Carcinoma sólido con presencia de Carcinoma sólido con presencia de moco Moco Carcinoma bronquiolo-alveolar Carcinoma de célula grande Carcinoma de célula grande (Grado IV) Variantes: Célula gigante (sin diferenciación escamosa, glandular Célula clara o neuroendocrina) Variantes: Célula gigante Célula clara Pleomórfico fusocelular Linfo-epitelial Carcinoma adenoescamoso Carcinoma adenoescamoso Carcinoma de glándulas bronquiales Carcinoma de glándulas bronquiales Carcinoma adenoide quístico Carcinoma adenoide quístico Carcinoma mucoepidermoide Carcinoma mucoepidermoide Tumor carcinoide Otros Otros Por uniformidad, conformidad y consistencia en los informes, se recomienda la clasificación histológica para carcinoma del pulmón, publicada por la OMS (WHO 1981). Sin embargo se sabe que se usan otras clasificaciones y la que proponemos se utiliza en el INSTITUTO NACIONAL DE CANCEROLOGÍA . En esta clasificación se define el tipo histológico por el componente celular y el grado por el factor de diferenciación: Grado X, tumor sin asignación de grado. Grado I, bien diferenciado. Grado II, moderadamente diferenciado. Grado III, mal o pobremente diferenciado. Grado IV, indiferenciado. Por definición, los carcinomas de células en avena y los de célula grande son Grado IV. 1. Carcinoma de células no pequeñas Son morfológicamente diversos y se subdividen en carcinomas de células escamosas, adenocarcinomas y de células grandes (incluye algunos tumores neuroendocrinos de célula grande). El carcinoma escamocelular es el más frecuente de los cánceres pulmonares, aunque su incidencia está disminuyendo en relación con los demás tipos histológicos, especialmente en las dos últimas décadas del siglo XX. Es de localización central y es el que aparece mayormente relacionado con el tabaquismo. Típicamente es de crecimiento lento y produce síntomas relacionados con efecto de masa, tiene tendencia a la necrosis y a la cavitación y es el que más fácilmente se detecta en la citología de esputo. Microscópicamente, el diagnóstico está basado en la identificación de queratina en células aisladas o en perlas y puentes intercelulares. La ausencia de este cuadro, clasifica el tumor como carcinoma de célula grande indiferenciado. Estos carcinomas se clasifican según su diferenciación en: bien, moderadamente y mal diferenciados. Ocasionalmente, puede encontrarse una pequeña población de células con mucina o de células pequeñas. El adenocarcinoma es el tipo más común de cáncer pulmonar en Japón y Hong Kong y, recientemente, el de mayor prevalencia en Norte América y Europa. Se puede originar como lesión central o periférica. El subtipo de adenocarcinoma periférico más común, frecuentemente exhibe un patrón bronquiolo-alveolar: mucinoso o no mucinoso. Se ha reconocido la relación entre la fibrosis intersticial difusa, las cicatrices pulmonares y el adenocarcinoma. Microscópicamente presenta una amplio rango de diferenciación, pero se identifican dos tipos morfológicos principales: formación de túbulos o papilas y producción de mucina. Se subdividen en acinares, papilares y sólidos con producción de moco. El esputo es frecuentemente negativo para malignidad en los nódulos tumorales únicos y periféricos, pero positivo en los nódulos múltiples o en las formas neumónicas del tumor. Es manifiesta la tendencia a producir metástasis al cerebro, hígado y huesos. Los carcinomas indiferenciados de célula grande son pleomórficos, sin evidencia de diferenciación escamosa, glandular o neuroendocrina. Los estudios de microscopia electrónica han demostrado una frecuencia mayor de diferenciación glandular. En los tumores adeno-escamosos la cantidad de células tumorales de ambos tipos es similar. De lo contrario, se consideran como tumores mixtos con diferenciación específica (escamosa o glandular, definiendo los porcentajes). 2. Carcinoma de células pequeñas Es considerado como un tipo de neoplasia neuroendocrina. En el pulmón y el árbol bronquial, el espectro de estos tumores puede incluir neoplasias bien diferenciadas y asintomáticas, hasta las muy indiferenciadas y agresivas. Frecuentemente expresa algunas hormonas que pueden actuar local o sistémicamente con manifestaciones clínicas paraneoplásicas. Los de célula pequeña tipo avena corresponden a las agresivas y representan el 20% de los tumores pulmonares y usualmente son centrales. Histológicamente son muy celulares, con poco citoplasma, escaso estroma y actividad mitótica variable, la cual es muy importante para definir el pronóstico. De acuerdo con estas características, se clasifican en bien diferenciados (incluye el carcinoide típico), moderadamente diferenciados (incluye el carcinoide atípico) y pobremente diferenciados.
| | | width="327" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" colspan="2" | |
| | '''Nombre''' |
|
| |
|
| | | width="64" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Código''' |
|
| |
|
| | | width="111" style="border: 1px solid #000000; padding: 0.1cm" rowspan="4" | |
| | [[Image:Saludarte.png]] |
|
| |
|
| = CUADRO CLÍNICO = | | |- valign="TOP" |
| | | width="327" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" colspan="2" | |
| | Guía de Practica clínica (GPC) Para el Tratamiento Farmacologico y Seguimiento del Paciente con Cancer de Pulmon |
|
| |
|
| <br>La presencia de síntomas en el momento del diagnóstico varía desde el 40% hasta el 98%. Los síntomas pueden ser causados por extensión local, metástasis o manifestaciones paraneoplásicas. Síntomas Frecuencia (%) Tos 45 - 75 Pérdida de peso 8 - 68 Disnea 37 - 58 Hemoptisis 27 - 57 Dolor torácico 27 - 49 Disfonía 2 - 18 Cuadros clínicos asociados Derrame pleural: puede ser debido a la invasión pleural del carcinoma o a otras causas, como obstrucción linfática, atelectasia, neumonitis obstructiva y aun a condiciones no relacionadas con el tumor (falla cardíaca y otras). Tumor de Pancoast: Es el tumor del estrecho torácico superior. Frecuentemente compromete el plexo braquial, los nervios torácicos, la cadena simpática, las costillas y las vértebras superiores. El síndrome de Pancoast es una tríada de síntomas que incluye dolor del hombro o brazo ipsilateral, síndrome de Horner y atrofia de los músculos intrínsecos de la mano. Síndrome de vena cava superior: La obstrucción del flujo sanguíneo en la vena cava superior puede causar un síndrome dramático. Está frecuentemente secundario a la compresión extrínseca de la vena cava superior, con o sin trombosis intraluminal secundaria. La causa más común en los adultos es el carcinoma broncogénico. Los síntomas más frecuentes son plétora de la cabeza y el cuello, y disnea. La tos, el dolor y la disfagia son menos frecuentes. Otros signos son la dilatación de las venas del cuello, edema facial y de los miembros superiores, apariencia pletórica, papiledema, cianosis facial y, ocasionalmente, derrame pleural. Enfermedad metastásica: Las manifestaciones clínicas del cáncer pulmonar pueden ser el resultado de extensión local-regional, diseminación hematógena, linfática o intraalveolar. Las de diseminación hematógena se presentan más frecuentemente en el hígado, sistema nervioso central, huesos y glándulas suprarrenales. INVESTIGACIÓN DIAGNÓSTICA La investigación diagnóstica tiene como propósito definir el tipo histológico, estadificar la enfermedad y determinar el riesgo operatorio, principalmente con base en el estado de la función pulmonar. La radiografía de tórax es el estudio imagenológico inicial que se realiza a un paciente con sospecha de enfermedad pulmonar o alto riesgo de desarrollar cáncer pulmonar. Es económica, ampliamente disponible y reproducible; debe realizarse en las proyecciones postero anterior y lateral, utilizando técnica de alto kilovoltaje y bajo miliamperaje. La citología de esputo se utiliza para la evaluación inicial del paciente que presenta una masa en la radiografía del tórax, pero su utilidad disminuye notablemente en los casos de tumores periféricos. Un examen negativo no descarta un cáncer pulmonar.La tomografía axial computadorizada (TAC) de tórax, utilizando medio de contraste yodado para realzar las estructuras vasculares y facilitar la visualización de los ganglios, es un examen indispensable en la evaluación del tumor primario en cuanto a tamaño, forma, bordes, extensión local así como su diseminación linfática y a distancia. El estudio se realiza desde los ápices pulmonares hasta el abdomen superior, para evaluar hígado y glándulas suprarrenales. La técnica espiral con medio de contraste intravenoso, ofrece mayor sensibilidad para detección de nódulos pulmonares y metástasis hepáticas. En pacientes asintomáticos con el diagnóstico de adenocarcinoma y carcinoma de células pequeñas y aquellos con signos o síntomas neurológicos y/o esqueléticos, independientemente de la histología, se recomienda TAC cerebral simple y con contraste, y gamagrafía ósea. La resonancia magnética del tórax suministra excelente detalle anatómico en áreas de difícil evaluación por TAC o radiografía convencional, particularmente los ápices pulmonares, la ventana aortopulmonar, las regiones supradiafragmáticas, vasos hiliares y mediastinales. La broncoscopia rígida o de fibra óptica, con lavados bronquiales, broncoalveolares, cepillados, biopsias bronquiales, transbronquiales y aspiración transbronquial con aguja, es un procedimiento importante de diagnóstico. Su rendimiento depende del tamaño del tumor y su localización, incrementándose cuando se combinan múltiples técnicas de recolección de las muestras. Las biopsias guiadas por TAC son útiles para el diagnóstico de masas pulmonares sospechosas de cáncer, accesibles por vía percutánea, con las ventajas de ser un procedimiento ambulatorio, de baja incidencia de complicaciones y aplicable a lesiones posiblemente metastásicas. Es recomendable que el patólogo verifique inmediatamente la calidad de la muestra obtenida. Frecuentemente con los anteriores métodos diagnósticos descritos, no se completa el proceso diagnóstico y de estadificación, lo cual hace necesario la realización de procedimientos invasores como la mediastinoscopia, mediastinotomía, videotoracoscopia y aun toracotomía. La mediastiniscopia, también denominada exploración mediastinal transcervical, tiene indicaciones absolutas y relativas como se describen en el cuadro 1. Cuadro 1 Indicaciones Ganglios mediastinales aumentados (mayor de 1,5 cm) en la TAC. Absolutas: Tumores T2 o T3 resecables. Lesión localizada en el tercio interno del campo pulmonar. Adenocarcinoma o carcinoma indiferenciado de célula grande. Citología de célula pequeña con lesión en estado I, aparentemente resecable. Indicaciones Sospecha de lesiones primarias múltiples o tumores pulmonares sin- Relativas: crónicos. Parálisis de cuerda vocal con lesión primaria en el lóbulo superior. Intención de utilizar quimioterapia neoadyuvante. La mediastinotomía anterior, o procedimiento de Chamberlain, con resección de cartílago por vía extrapleural, se realiza para evaluar los ganglios de la ventana aorto-pulmonar (estación 5) y de la región paraaórtica (estación 6). 277 CÁNCER BRONCOGÉNICO La videotoracoscopia, a través de pequeñas incisiones en los espacios intercostales ofrece una vista panorámica del hemitórax ipsilateral del tumor en evaluación, permitiendo estadificación del hilio y los ganglios paratraqueales. En el lado izquierdo ofrece la ventaja de exponer los ganglios del mediastino posterior cerca al bronquio fuente izquierdo, así como los ganglios del ligamento pulmonar inferior. Igualmente, identifica nódulos pleurales y aun derrames que no son identificados mediante imágenes. En tumores de menos de 3 cm se puede realizar la biopsia excisional. Todo paciente candidato a resección pulmonar debe ser sometido a una evaluación clínica meticulosa, con énfasis en las pruebas de función cardiaca y respiratoria. Los siguientes son parámetros indicativos de alto riesgo anestésico: PaO2 <50 mm Hg, PaCO2 >45 mm Hg, consumo de oxígeno en ejercicio (MVO2) <10 ml/kg/min, capacidad de difusión de CO <60 %, VVM <50 % o VR / CPT >50%. El VEF1 debe ser de un litro luego de la resección, lo cual puede ser determinado preoperatoriamente mediante una prueba de ventilación o perfusión pulmonar isotópica que predice el porcentaje de tejido pulmonar que quedará luego de la resección, al multiplicar tal porcentaje por el VEF. Valores predichos postoperatorios cercanos a 800 ml, usualmente requieren de otros estudios para estimar el riesgo real, como consumo de oxígeno en ejercicio. Debe tenerse en cuenta la valoración cardiológica completa, por cuanto muchos de los factores etiológicos del cáncer pulmonar también causan enfermedades cardiovasculares importantes que comprometen la tolerancia al tratamiento quirúrgico. Según los factores de riesgo puede ser necesario practicar prueba de esfuerzo convencional, estudio isotópico de perfusión miocárdica, coronariografía y aun procedimientos de revascularización. La hipertensión pulmonar de moderada a severa, el infarto miocárdico reciente o una severa enfermedad coronaria son contraindicaciones para la resección pulmonar. ESTADIFICACIÓN La estadificación TNM de la Unión Internacional Contra el Cáncer es utilizada universalmente (UICC 1998), para los tumores de célula no pequeña. Los ganglios linfáticos regionales son intratorácicos, escalénicos y supraclaviculares. Los ganglios intratorácicos son clasificados en dos grandes grupos: A) Mediastinales, con diez estaciones: 1. Mediastinal alta (superior). 2. Paratraqueal (paratraqueal superior). 3. Pretraqueal. a) mediastinal anterior. b) retrotraqueal (mediastinal posterior). 4. Traqueobronquial paratraqueal inferior e incluye los ganglios ázigos. 5. Subaórtica (ventana aórtica). 6. Para-aórtica (aorta ascendente o frénica). 7. Subcarinal. 8. Paraesofágica (inferior a la carina). 278 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) 9. Ligamento pulmonar interior. 10. Traqueobronquiales. B) Peribronquiales, con cuatro estaciones: 1. Interlobar 2. Lobar 3. Segmentaria 4. Subsegmentaria Clasificación TNM T tumor primario TX El tumor primario no puede ser evaluado, o el tumor diagnosticado por citología de esputo o bronquial no es visible en imágenes ni en broncoscopia. T0 No hay evidencia de tumor primario. Tis Carcinoma in situ. T1 Tumor <3 cm. de diámetro mayor, rodeado de tejido pulmonar o de pleura visceral, sin evidencia broncoscópica de invasión proximal al bronquio lobar (o sea, no ubicado en el bronquio principal). T2 Tumor con alguna de las siguientes características: - >3 cm. de diámetro mayor. - Invasión del bronquio principal a más de 2 cm. distales a la carina. - Invasión de la pleura visceral. - Atelectasia o neumonitis obstructiva de la región hiliar pero no de la totalidad del pulmón. T3 Tumor de cualquier tamaño, que invada directamente cualquiera de las siguientes estructuras: pared torácica (incluso los tumores del surco superior), diafragma, pleura mediastinal o pericardio parietal; o el bronquio principal a menos de 2 cm. distales a la carina, pero sin invadirla; o asociado a atelectasia o neumonitis de la totalidad del pulmón. T4 Tumor de cualquier tamaño que invada cualquiera de las siguientes estructuras: mediastino, corazón, grandes vasos, tráquea, esófago, vértebras o carina; o con derrame pleural o pericárdico malignos o nódulos tumorales separados en el mismo lóbulo pulmonar del tumor primario. 279 CÁNCER BRONCOGÉNICO Fuente: Atlas TNM 1998, UICC Springer Verlag Ibérica. Fuente: Atlas TNM 1998, UICC Springer Verlag Ibérica. T3 T3 T3 Derrame cleural con citología negativa T3 Atelectasia o neumonía obstructiva de todo el pulmón T = pT ³ 2 cm T2 T2 Atelectasia o neumonía obstructiva T= pT T2 > 3 cm ³ 2 cm ³ 2 cm T2 280 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) Fuente: Atlas TNM 1998, UICC Springer Verlag Ibérica. N - Ganglios regionales NX Los ganglios regionales no pueden ser evaluados N0 No hay metástasis ganglionares regionales N1 Metástasis en ganglios peribronquiales ipsilaterales y/o hiliares ipsilaterales y/o ganglios intrapulmonares incluso compromiso por invasión directa. N2 Metástasis a ganglios mediastinales ipsilaterales y/o subcarinales. N3 Metástasis a ganglios mediastinales, hiliares contralaterales, escalénicos ipsilaterales o contralaterales o supra-claviculares. M- Metástasis distantes MX No es posible determinar la presencia de metástasis distantes M0 No hay metástasis distantes M1 Hay metástasis distantes, incluyendo nódulos tumorales en un lóbulo diferente (ipsilateral o contralateral). T4 pT4 Grandes vasos Corazón 281 CÁNCER BRONCOGÉNICO Fuente: Atlas TNM 1998, UICC Springer Verlag Ibérica. Fuente: Atlas TNM 1998, UICC Springer Verlag Ibérica. N2 N2 N = pN N1 N1 Peribronquiales Hiliares N = pN 282 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) Fuente: Atlas TNM 1998, UICC Springer Verlag Ibérica. ESTADOS CLÍNICOS SEGÚN LA CLASIFICACIÓN TNM Estado 0 Tis N0 M0 Estado IA T1 N0 M0 Estado IB T2 N0 M0 Estado IIA T1 N1 M0 Estado IIB T2 N1 M0 T3 N0 M0 Estado IIIA T3 N1 M0 T(1-3) N2 M0 Estado IIIB T4 cualquier N M0 cualquier T N3 M0 Estado IV cualquier T cualquier N M1 CÁNCER BRONCOGÉNICO DE CÉLULA PEQUEÑA El grupo de estudio del cáncer pulmonar de la Administración de Veteranos de los Estados Unidos (Mountain 1997), desarrolló un sistema simple de dos estados. Este clasifica los pacientes con enfermedad limitada, cuando el tumor está confinado a un hemitórax y sus ganglios regionales, incluyendo los mediastinales ipsilaterales, supraclaviculares ipsilaterales y ganglios contralaterales. En esencia esta enfermedad puede definirse simplemente como un tumor localizado que puede fácilmente ser comprendido dentro de un campo aceptable de radioterapia, y son aceptados aun con presen- N3 N3 N3 M1 N3 N = pN M= pM 283 CÁNCER BRONCOGÉNICO cia de derrame pleural ipsilateral, compromiso del nervio laringeo recurrente izquierdo o síndrome de vena cava superior. Se clasifica como enfermedad extendida la presencia de derrame pericárdico y el compromiso parenquimatoso pulmonar bilateral, así como la evidencia de enfermedad fuera del tórax.
| | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | PGD1E7 |
|
| |
|
| | |- valign="TOP" |
| | | width="156" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Fecha de Emisión''' |
|
| |
|
| | | width="163" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Fecha de Actualización''' |
|
| |
|
| = TRATAMIENTO = | | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Versión''' |
|
| |
|
| <br>Tratamiento quirúrgico El único tratamiento capaz de curar el carcinoma broncogénico de células no pequeñas es la resección quirúrgica completa. Desafortunadamente, sólo una pequeña proporción, menos del 10% de los casos, es operable y resecable, puesto que generalmente el diagnóstico se establece cuando el tumor ya se encuentra en estado avanzado. El tratamiento se planea según la estadificación, tomando decisiones por consenso de neumología, oncología clínica, cirugía de tórax, radioterapia y el especialista en cuidados paliativos. Se deben tener en cuenta los criterios de operabilidad y la calificación de las contraindicaciones absolutas o relativas, las cuales dependen de las condiciones generales del paciente, de la experiencia del cirujano y de la capacidad técnica del centro hospitalario. Algunas contraindicaciones relativas en un hospital altamente sofisticado, se convierten en absolutas en un hospital de menor capacidad técnica. El muy sombrío pronóstico del carcinoma anaplásico de células en avena hizo que muchos consideraran inútil la resección quirúrgica, a menos que fuera un tumor incipiente y muy localizado. Igualmente, ciertos tumores con manifestaciones muy graves que en primera instancia los calificarían como inoperables, pueden ser candidatos a resección después de<br> radioterapia y/o quimioterapia de inducción. Tal es el caso de los tumores de Pancoast del surco superior. Se ha logrado mejorar la supervivencia mediante irradiación seguida tres semanas más tarde de resección en bloque de las costillas superiores, partes de las vértebras, las raíces nerviosas intercostales, la porción inferior del plejo braquial y la cadena simpática dorsal, en conjunto con el lóbulo superior y una disección ganglionar radical hiliar y mediastinal, procedimiento que deja secuelas neurológicas. El procedimiento quirúrgico consiste en la resección de la porción afectada del pulmón mediante lobectomía o bilobectomía, junto con márgenes adecuados de pulmón y de bronquio normales, en continuidad con los ganglios linfáticos, reservando la neumonectomía para las lesiones más extensas. La segmentectomía y las resecciones en cuña no son procedimientos aconsejados, por la alta tasa de recaída local (25-30%) y sólo pueden ser recomendadas en pacientes con tumores periféricos y reserva funcional pulmonar limitada. En general, los factores determinantes del pronóstico son la extensión de la lesión y la estadificación TNM. También el tipo histológico juega papel importante en cuanto a supervivencia, y en general los carcinomas epidermoides exhiben supervivencias globales del orden de 35% a 5 años, contra <10% para los adenocarcinomas, y todavía menos para los carcinomas indiferenciados de células gigantes. En los carcinomas de células pequeñas el pronóstico es muy malo, aun en estados tempranos. 284 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) En el caso de los tumores de Pancoast sin invasión ganglionar del mediastino, con la resección en bloque del tumor y de áreas localizadas de invasión en la pared torácica se logran supervivencias a 5 años hasta del 30%, y una satisfactoria paliación del dolor. La lobectomía con resección bronquial (broncoplastia) en manguito constituye una alternativa real a la neumonectomía en el caso de tumores centrales. La broncoplastia es una modalidad terapéutica establecida para pacientes debidamente seleccionados. PLAN DE TRATAMIENTO SEGÚN ESTADIFICACIÓN ESTADO IA - IB - IIA - IIB Estado IA El tratamiento de elección es la resección quirúrgica con linfadenectomía mediastinal y periesofágica, del ligamento pulmonar inferior y de la ventana aortopulmonar en el lado izquierdo. En los pacientes con restricción pulmonar severa que no puedan tolerar una lobectomía, se practica resección segmentaria o una resección en cuña, amplia. En los pacientes con tumores completamente estirpados no está indicada la radioterapia postoperatoria y tampoco ofrece beneficio la quimioterapia adyuvante. En los estados I y II que no sean candidatos a cirugía, la radioterapia puede ser considerada como el tratamiento opcional más adecuado. Estado IIIA En los pacientes con tumores clasificados como T3, con mediastinoscopia negativa, se recomienda la resección quirúrgica completa de primera intención. La cirugía también es el tratamiento definitivo si el estudio patológico del espécimen resecado demuestra compromiso tumoral de los ganglios N1. Si por el contrario, se encuentra compromiso de los ganglios N2, se indican radioterapia postoperatoria y quimioterapia adyuvante o postoperatoria a fin de disminuir la posibilidad de recurrencia local y sistémica. En este grupo se incluyen también los pacientes con N2, cuyo tratamiento se presta a controversia porque no se consideran quirúrgicos en primera instancia. En la actualidad se ha identificado un grupo de estos enfermos que pueden ser considerados para resección, luego de haber recibido quimioterapia preoperatoria (neoadyuvante o de inducción) y habiendo obtenido una respuesta parcial (>50%), se continúa con la resección quirúrgica y la disección mediastinal, seguida de quimioterapia y radioterapia adyuvantes. Cuando las malas condiciones del paciente impidan realizar la operación, están indicadas la radioterapia y la quimioterapia como tratamiento paliativo. Un tipo particular de cáncer pulmonar es el tumor del surco pulmonar superior o tumor de Pancoast, para el cual está indicado un tratamiento combinado: radioterapia preoperatoria con resección en bloque, método que ha logrado supervivencias a 5 años de cerca del 30%, con buen control de los síntomas, siempre y cuando no exista compromiso de los ganglios del mediastino, caso en el cual la supervivencia global no es mayor de 1 año. Tumores próximos a la carina. Algunos de estos tumores y otros que comprometen el orificio lobar llevan a que la lobectomía estándar deje márgenes positivas del tumor y tienen como alternativa a la neumonectomía, la realización de broncoplastia o resección en manguito, preservando tejido pulmonar funcionante sin comprometer la resecabilidad. Estado IIIB En casos especiales de T4 y con un buen estado funcional cardio-pulmonar, algunos cirujanos realizan la neumonectomía intrapericárdica con resección de pericardio y aun 285 CÁNCER BRONCOGÉNICO de segmentos de la aurícula izquierda comprometida o traqueobroncoplastia en caso de compromiso de la carina o de porciones de la vena cava superior, con buenos resultados. Para los pacientes no candidatos a cirugía, se utiliza la quimioterapia y la radioterapia en combinación. Antes de 1990 la radioterapia fue la modalidad terapéutica principal en estos pacientes, pero posteriormente se ha demostrado la superioridad de la combinación de quimioterapia y radioterapia con drogas más activas y menos tóxicas. El derrame pleural maligno, por invasión tumoral de la pleura, se presenta hasta en 50% de los enfermos con carcinoma broncogénico. El manejo incluye drenaje del líquido y pleurodesis, una vez lograda la expansión pulmonar completa. La sustancia esclerosante más efectiva es el talco libre de asbesto y de fibra, en dosis de 2 gramos; en casos especiales de derrrame recidivante se realiza decorticación pleural. Estado IV Es el estado de enfermedad diseminada y el tratamiento es paliativo, pero no se limita al manejo del dolor y de los síntomas que producen las metástasis a distancia; pueden considerarse esquemas de quimioterapia con nuevos agentes que han mostrado beneficio en cuanto a supervivencia, calidad de vida y costo-efectividad, cuando se comparan con el tratamiento de apoyo óptimo. Radioterapia La radioterapia se aplica preoperatoriamente, asociada con quimioterapia, a pacientes con carcinoma pulmonar de células no pequeñas, inicialmente no resecable y localmente avanzado. También se utiliza en forma postoperatoria cuando existen márgenes quirúrgicos positivos, compromiso de ganglios hiliares o mediastinales o invasión a la pared, para reducir la tasa de recurrencia local. La dosis postoperatoria es de 50 a 60 Gy en dosis de 1,8 a 2 Gy por día. Cuando hay márgenes positivos, la dosis requerida es de 66 a 70 Gy. La radioterapia radical está indicada como alternativa única de tratamiento cuando existe contraindicación para cirugía y quimioterapia, en el mismo fraccionamiento de dosis, hasta completar 70 Gy. La braquiterapia endobronquial se puede utilizar con intención curativa en tumores con carcinoma in situ endobronquial o paliativa en tumores con compromiso endoluminal que produzcan síntomas como disnea, tos, hemoptisis, atelectasia y neumonía obstructiva. Puede utilzarse sola o como refuerzo de la radioterapia externa. También es útil en el tratamiento de las recidivas tumorales y de segundos tumores primarios pulmonares y metastásicos con localización endobronquial. La radioterapia es útil en el tratamiento de metástasis óseas y del SNC. La técnica de la radioterapia debe contar siempre con la disponibilidad de equipos para simulación de tratamientos, dirigidos por un radioterapéuta oncólogo, con la ayuda de un físico médico. Quimioterapia La quimioterapia para el Estado IIIB utiliza las mismas combinaciones que en el Estado IV, con lo cual se logra 40% de respuestas y una supervivencia media de 8 a 10 meses. Apenas 20% de los pacientes viven 2 años y sólo el 3% viven 5 años. En protocolos de estudio se puede utilizar el tratamiento combinado de radioterapia y quimioterapia. · Estado I Cirugía · Estado II Cirugía Radioterapia en casos de alto riesgo, por problemas médicos. · Estado IIIA Quimioterapia neoadyuvante con Ifosfamida 1.6 mg/m2/ día x 3 días, más Vinorelbina 30 mg/m2, día x 2 días, por 3 ciclos, seguida de cirugía y/o radioterapia. · Estado IIIB Quimioterapia, radioterapia, cirugía según respuesta. Cisplatino 80 mg/m2 día 1 Vinorelbina 30 mg/m2, día 1, por 3 ciclos · Estado IV: Sin compromiso de SNC Cisplatino 100 mg/m2/día, día 1 Etopósido 80 mg/m2/día, x 3 días, por 6 ciclos Con compromiso de SNC: Radioterapia Tratamiento sintomático Protocolos a evaluar 1. Carboplatino, AUC 7,5 día 1 Paclitaxel 135 mg/m2 2. Gemcitabina 1000 mg/m2, días 1,8 y 15 Cisplatino 75 mg/m2, día 2 CÁNCER DE PULMÓN DE CÉLULA PEQUEÑA Quimioterapia Etopósido 120 mg/m2 x 3 Carboplatino 300 mg/m2, día 1 En personas seniles o médicamente comprometidas por enfermedad extensa, con compromiso importante de su escala funcional (IK<70%): Etopósido oral 50 mg/m2 x 21 días, reiniciando después de una semana de descanso. Radioterapia en enfermedad localizada, profilaxis del sistema nervioso central y para metástasis óseas y cerebrales. SEGUIMIENTO La resección quirúrgica es el tratamiento para el cáncer pulmonar de célula no pequeña, enfermedad localizada. Sin embargo, después de una aparente resección completa, los tumores recurren en una tasa estimada de 20% a 30% para el estado I, 50% para el estado II y 70% para el estado III a cinco años. Las recurrencias pueden ser locales, regionales o a distancia. Una vez el cáncer recurre, el pronóstico es pobre, con una tasa de supervivencia de dos años de 37%, 20% y 14% para los estados I, II, III respectivamente. El cáncer de célula pequeña es generalmente incurable. 287 CÁNCER BRONCOGÉNICO Los pacientes con recurrencia local o a distancia pueden ser tratados en algunas ocasiones con resección quirúrgica o con modalidades paliativas, como radioterapia externa o braquiterapia. Por tanto, luego de la resección quirúrgica para el cáncer pulmonar, debe continuarse una supervisión del paciente para identificar y tratar las recurrencias o una nueva enfermedad primaria tan rápido como sea posible. Se recomienda controles clínicos y con radiografía de tórax cada tres meses durante el primer año post-operatorio, cada 6 meses durante el segundo y anualmente a partir del tercer año.
| | |- valign="TOP" |
| | | width="156" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | 2011/09/08 |
|
| |
|
| LECTURAS RECOMENDADAS <br>1. AYGUN C, BLUM JE. Treatment of unresectable lung cancer with brachytherapy. World J Surg 19:823,1995. 2. BEZJAK A, PAYNE DAVID. Radiotherapy in the management of non-small-cell lung cancer. World J Surg 17:741,1993. 3. BROWN JS, ERAUT D, TRASK C, DAVIDSON AG. Age and the treatment of lung cancer. Thorax 51:564,1996. 4. BROWNSON RC, LOY TS, INGRAM E, ET AL. Lung cancer in nonsmoking women: Histology and survival patterns. Cancer 75:29,1995. 5. CAMACHO F, RUSSI H, SCHRADER C, ET AL. Broncoplastia: su utilidad en el tratamiento de las lesiones benignas y malignas. Rev Col Cir 3:77, 1988. 6. COLICE, GL. Chest CT for known or suspected lung cancer. Chest 106:1538, 1994. 7. COTE RJ, BEATTIE EJ, CHAIWUN B, SHI SHR. Detection of occult bone marrow micrometastases in patients with operable lung carcinoma. Ann Surg 222:415, 1995. 8. CRINO L, SCAGLIOTTI G, MARANGOLO M, ET AL. Cisplatin-gemcitabine combination in advanced non-smallcell lung cancer: A Phase II study. J Clin Oncol 15:297, 1997. 9. DE GIACOMO T, RENDIN EA, VENUTA F, ET AL. Thoracoscopic staging of IIIB non-small cell lung cancer before neoadjuvant therapy. Ann Thorac Surg 64:1409, 1997. 10. EINHORN LH. Neoadjuvant and adjuvant trials in non-small cell lung cancer. Ann Thorac Surg 65:208,1998. 11. FUNATSU T, MATSUBARA Y, IKEDA S, ET AL. Preoperative mediastinoscopic asessment of N factors and the need for mediastinal lymph node dissection in T1 lung cancer. J Thorac Cardiovasc Surg 108:321, 1994. 12. GOLDBERG-KAHN B, HEADY JC, BISHOP JW. The cost of diagnosis: a comparison on four different strategies in the workup of solitary radiographic lung lesions. Chest 111:870, 1997. 13. IANNETTINI MD, LYNCH WR. Lung cancer. Sem Resp Crit Care Med 20: 405, 1999. 14. IZBICKI JR, PASSLICK B, KARG O, ET AL. Impact of radical systematic mediastinal lymphadenectomy on tumor staging in lung cancer. Ann Thorac Surg 59:209, 1995. 15. LÓPEZ HG, SCHRADER C, BUITRAGO R Y POSSO H, Síndrome de vena cava superior. Rev Inst Nal Cancerol 2:39, 1993. 16. MARTINI N, KRIS MG, FLEHINGER BJ, ET AL. Preoperative Chemotherapy for Stage IIIa (N2) Lung Cancer: The Sloan-Kettering Experience with 136 patients. Ann Thorac Surg 55:1365,1993. 17. MARTINI N. Mediastinal lymph node dissection for lung cancer: The Memorial experience. Chest Surg Clin N Am 5:189, 1995. 18. MENTZER SJ, SWANSON SJ, DECAMP MM, ET AL. Mediastinoscopy thoracoscopy, and video-assisted thoracic surgery in the diagnosis and staging of lung cancer. Chest 112:239s,1997. 19. MOUNTAIN CF. Revisions in the international system for staging lung cancer. Chest 111:1710,1997. 288 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) 20. NARUKE T, TSUCHIYA R, KONDO H, ET AL. Implications of staging in lung cancer Chest 112:242s, 1997. 21. PASSLICK B, IZBICKI JR, KUBUSCHOK B, THETTER O, ET AL. Detection of Disseminated Lung Cancer Cells in Lymph Nodes: Impact on Staging and Prognosis. Ann Thorac Ssurg 61:177, 1996. 22. PATIÑO JF. Carcinoma pulmonar. En: JF Patiño. Lecciones de Cirugía. Editorial Médica Panamericana. Buenos Aires, Bogotá, p 774-785. 23. REED MF, SUGARBAKER DJ. Mediastinal Staging En: Lung Cancer. Pass HI, Mitchell JB, Johnson DH, Turrisi AT (eds). Philadelphia. Lipincott-Raven Publishers, 1996. 24. ROSAI J. Ackerman s Surgical Patholoy 8th edition. Lungand pleura. St Louis MO. Mosby, 1996, p 338-434. 25. RUCKDESCHEL JC. Combined modality therapy of non-small cell lung cancer. Semin Oncol 24:429, 1997. 26. SALDANA MJ, MONES JM, GARCÍA-MOLIWER M, FRABLE WJ. Localized Diseases of the Bronchi and Lung. In: Principles and practice Surgical Pathology and Cytophatholoy, Third Edition, Vol 2. Silverberg SG, Delellis RA; Frable, WI (eds). New York, Churchill Livinestone, 1997 p. 1189. 27. SCHAFFER K. Radiologic evaluation in lung cancer: Diagnosis and staging. Chest 112:235s.1997. 28. SHEPHERD FA. Induction chemotherapy for locally advanced non-small cell lung cancer. Ann Thorac Surg 55:1585, 1993. 29. SWEENEY C, SANDLER A. Treatment of advanced (Stages III and IV) non-small cell lung cancer. Curr Probl Surg 22:85,1998. 30. SWYER TE, BONNER JA, GOULD PM, ET AL. Effectiveness of postopertive Irradiation in Stage IIIA nonsmall cell lung cancer according to regression tree analyses of recurrence risks. Ann Thorac Surg 64:1402,1997. 31. TAPIAS L, BUITRAGO R. Tumores del pulmón. En: Neumología. Roa J, Bermúdez M, Acero R. (Editorial. Mc Graw Hill Interamericana) Bogotá, 2000. p383-401. 32. TRAVIS WD, LINDER J, MACKAY B. Classification, histology, cytology, and efectron microscopy. En: Lung Cancer. Pass HI, Mitchell JB, Johnson DH, Turrisi AT (eds). Philadelphia. Lippincott. Raven Publishers, 1996. UICC. Como ref. 25, pag. 190. 33. TRAVIS WD, TRAVIS LB, DEVESA SS. Lung cancer. Cancer 75:191,1995. 34. UICC. Atlas TNM. Guía ilustrada para la clasificación TNM/pTNM de los tumores malignos. 4ª edición. Editada por P Hermanek, RVP Hutter, LH Sobin, G Wagner, Ch Writtekind. Springer-Verlag Ibérica SA, 1998. 35. VANSTEENKISTE JF, STROOBANTS SG, DE LEYN PR, DUPONT PJ. Mediastinal lymph node staging with FDGPET scan in patients with potentially operable non-small cell lung cancer: A prospective analysis of 50 cases. Chest 112:1480, 1997. 36. VISBAL A, SCHRADER C, REY M Y BUITRAGO R. Cáncer d epulmón de células no pequeñas. INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda), Bogotá, 1998 (Inédito). 37. WARREN WH, FABER LP. Extended resections for locally advanced pulmonary carcinomas En: Lung Cancer. Pass HI, Mitchell JB, Johnson DH, Turrisi AT (eds). Philadelphia. Lippincott-Raven Publishers, 1996. 38. WHO. Histologic Typing of Lung Cancer, 2nded. World Health Organization. Geneva, 1981. 39. WOLPAW DR. Early detection in lung cancer. Med Clin North Am 80:63, 1996. 40. YANO M, ARAI T, INAGAKI K, MORITA T, ET AL. Intrapulmonary satellite nodule of lung cancer as a T factor. Chest 114:1305, 1998. 41. YOKOI K, KAMIYA N, MATSUGAMA H, MACHIDA S, ET AL. Detection of Brain Metastasis in Potentially Operable Non-small Cell Lung Cancer: A Comparison of CT and MRI. Chest 115:714,1999. 289
| | | width="163" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | 2025-10-31 |
| | |
| | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | 4 |
| | |
| | |} |
| | |
| | <br> <u>'''Elaboró'''</u>''': '''Documento adaptado de las guías de manejo del Instituto Nacional de Cancerología de Colombia y el Ministerio de Protección Social |
| | |
| | <u>'''Revisó y Autorizo Ultima Versión'''</u>: Comité de tumores 2019/05/11 |
|
| |
|
| <br> | | <br> |
| | |
| | = Objetivo = |
| | |
| | Servir de apoyo al personal de Oncomedic ltda, para establecer los criterios mínimos indispensables para el adecuado manejo y seguimiento de pacientes con cáncer de pulmon céluas pequeñas, de acuerdo al estadio, que garanticen una atención médica integral, homogénea, con calidad, equidad y eficiencia articulada a los protocolos de manejo del instituto Nacional de Cancerologia. |
| | |
| | = Alcance = |
| | |
| | Las recomendaciones generadas en esta guía podrán contribuyen a la toma de decisiones clínicas. |
| | |
| | = Marco Conceptual = |
| | |
| | El cáncer de pulmón es la patología maligna mas frecuente en el mundo durante varias décadas, en 2008 se estimaron 1.610.000 casos nuevos, lo que representa el 12,7% del total de casos nuevos de cáncer (sin incluir cáncer de piel) de todo el mundo. En Colombia se estiman 2.697 casos nuevos anuales en hombres, y 1.772 en mujeres, con tasas de incidencia de 16,3 casos nuevos por 100.000 hombres y 8,6 casos nuevos por 100.000 mujeres (1).<br>El cáncer de pulmón es clasificado clínicamente como de células pequeñas (14%), y de células no pequeñas (85%), para efectos de tratamiento.<br><br><br>El instituto nacional de cancerologia publico la 1 versión del Protocolo de manejo de la paciente con cáncer de cuello del útero en el 2009 y fue actualizado noviembre del 2010 como un aporte para el adecuado manejo de esta entidad patológica. |
| | |
| | Acorde a la propuesta del ministerio de protección social y articulada a las características de oncomedic ltda la organización adapta las guías, de modo que aplica sin modificación las recomendaciones que pueden ser seguidas dentro de la organización de acuerdo a los estados clínicos de la enfermedad. |
| | |
| | = Descripción = |
| | [[Archivo:Ca pulmon.jpg]]'''Ruta de atención en cáncer de pulmón''' |
| | |
| | |
| | |
| | |
| | ==== Clasificación TNM ==== |
| | |
| | American Joint Committee on Cancer, (6a edición) .<br>'''Tumor primario''' <br> |
| | |
| | *T0: No hay evidencia de tumor primario. |
| | |
| | *TX: Tumor primario que no puede ser evaluado, o tumor certificado por la presencia de células malignas en el esputo o lavado bronquial, pero no visualizado por imágenes o broncoscopia<br> |
| | |
| | *TIS: Carcinoma in situ. |
| | |
| | *T1: Tumor menor de 3 cm en su diámetro mayor, rodeado por pulmón o pleura visceral, sin evidencia broncoscópica de invasión más proximal del bronquio lobar (no en bronquio principal). |
| | *T2: Tumor con cualquiera de los siguientes características de tamaño o extensión: |
| | |
| | #Mas de 3 cm en su diámetro mayor |
| | #Compromiso de bronquio principal, a >2 cm distal de la carina |
| | #Invasión de pleura visceral asociado a atelectasia o neumonitis obstructiva extendida al hilio, pero que no compromete el pulmón entero |
| | |
| | *T3: Tumor de cualquier tamaño que invade directamente cualquiera de los siguientes sitios: |
| | |
| | #Pared torácica (incluyendo tumores del sulcus superior) |
| | #Diafragma |
| | #Pleura mediastinal |
| | #Pericardio parietal |
| | #Tumor en bronquio principal a mas de 2 cm distal de la carina, pero sin compromiso de ésta o atelectasia asociada, o neumonitis obstructiva del pulmón entero |
| | |
| | *T4: Tumor de cualquier tamaño que invade cualquiera de los siguientes estructuras: |
| | |
| | #Mediastino |
| | #Corazón |
| | #Grandes vasos |
| | #Tráquea |
| | #Esófago |
| | #Cuerpos vertebrales |
| | #Carina |
| | #Tumor con derrame pleural o pericárdico maligno, o con nódulos(s) tumoral(s) satélite(s) dentro del lóbulo tumoral primario del pulmón. |
| | |
| | '''Ganglios linfáticos regionales (N)''' |
| | |
| | *NX: Ganglios linfáticos regionales que no pueden ser evaluados |
| | *N0: Sin metástasis en ganglios linfáticos regionales. |
| | *N1: Metástasis en ganglios linfáticos peribronquiales ipsilaterales o hiliares ipsilaterales, y compromiso de ganglios intrapulmonares por extensión directa del tumor primario. |
| | *N2: Metástasis a ganglio(s) linfáticos ipsilaterales mediastinales o subcarinales. |
| | *N3: Metástasis a ganglio(s) linfáticos mediastinales contralaterales, hiliares contralaterales, escalenos ipsilaterales o contralaterales, o supraclaviculares. |
| | |
| | '''Metástasis a distancia (M)''' |
| | |
| | *MX: Presencia de metástasis a distancia que no pueden ser evaluadas. |
| | *M0: Sin metástasis a distancia. |
| | *M1: Metástasis a distancia presentes.<br>a.La mayoría de los derrames pleurales asociados a cáncer de pulmón son debidos al tumor. Sin embargo, en algunos pacientes con múltiples exámenes citopatológicos negativos de derrames pleurales no sanguinolentos, no exudativos o pericárdicos, en los que el juicio clínico dicta que no están relacionados con el tumor, el derrame debería ser excluido como elemento de estadificación de la enfermedad del paciente como T1, T2, o T3.<br>b.Los nódulos tumorales metastásicos alejados del lóbulo tumoral primario del pulmón son clasificados como M1. |
| | |
| | [[Image:Est pulmon.png]] |
| | |
| | <br> |
| | |
| | = Algoritmos = |
| | |
| | [[Image:Algoritmo P.png]] |
| | |
| | [[Image:Algoritmo P1.png]] |
| | |
| | [[Image:Algoritmo P2.png]] |
| | |
| | [[Image:Algoritmo P3.png]] |
| | |
| | [[Image:Algoritmo P4.png]] |
| | |
| | ==== Intervenciones de Oncología Clínica Esquemas de Qumioterapia ==== |
| | |
| | *Esquemas en primera línea de cáncer de pulmón |
| | |
| | #Carboplatino más paclitaxel: paclitaxel 225 mg/m2 infusión de 3 horas más carboplatino AUC 6 mg/ml/min día 1 esquema de 21 días, paclitaxel 175 mg/m2 infusión de 3 horas más carboplatino AUC 6 mg/ml/min día 1 esquema de 21 días |
| | #Carboplatino AUC 2mg/ml/min más paclitaxel 100 mg/m2 semanal |
| | #Cisplatino más etpósido: cisplatino 100mg/m2 día 1 más etpósido 100 mg /m2 días 1 a 3 cada 21 días |
| | #Cisplatino más vinorelbine: cisplatino 100 mg/m2 día1 más vinorelbine 25 mg/ m2 días 1, 8,15, 22 cada 21 días |
| | #Cisplatino más paclitaxel: cisplatino 75 mg/m2 día 1 más paclitaxel 135 mg/m2 día 1 cada 21 días |
| | #Cisplatino más docetaxel: cisplatino 75 mg/m2 más docetaxel 75 mg/m2 cada 21 días |
| | #Carboplatino más docetaxel: carboplatino auc 6 mg/ml/min día 1 más docetaxel 75 mg/m2 cada 21 días |
| | #Cisplatino más gemcitabine: cisplatino 100 mg/m2 día 1 más gemcitabine 1000 mg/m2 días 1, 8, 15, esquema cada 28 días |
| | #Carboplatino más gemcitabine: carboplatino 5 auc mg/ml/min día 1, gemcitabine 1200 mg/m2 días 1 y 8 cada 3 semanas |
| | #Cisplatino más premetrexed: cisplatino 75 mg/m2 día 1 más premetrexed 500 mg/m2 día 1 esquema de 21 días |
| | #Cisplatino más irinotecan: cisplatino 80mg/m2 día 1, irinotecan 60 mg/m2 días 1, 8, 15 cada 4 semanas |
| | #Carboplatino más premetrexed: carboplatino auc 5mg/ml/min día 1 premetrexed 500 mg/m2 cada 21 días (31) |
| | #Carboplatino más vinorelbine: carboplatino auc 4 mg/ml/min día 1 más vinorelbine 25mg/m2 día 1 esquema de 21 días (32)<br> |
| | |
| | <br> |
| | |
| | '''Esquemas con Bevacizumab en primera línea:'''<span style="line-height: 1.5em;"> </span><span style="line-height: 1.5em;">Sólo en pacientes con variedad de adeno</span><span style="line-height: 1.5em;">carcinoma, con el adecuado escala funcional </span><span style="line-height: 1.5em;">(PS), sin historia de hemoptisis, previa presen</span>tación en junta del servicio de oncología): |
| | |
| | #Cisplatino 80 mg /m2 día 1 más gemcitabine 1250 mg/m2 día 1 y 8 más bevacizumab 15 mg /kilo día 1 esquema de 21 días |
| | #Paclitaxel 200 mg /m2 más carbopblatino 6 x auc más bevacizumba 15 mg/kilo día 1 esquema de 21 días |
| | #Esquemas con Cetuximab en primera línea (Sólo en pacientes con variedad de adenocarcinoma, con el adecuado estado general, previa presentación en junta del servicio de oncología) |
| | #Cisplatino 80 mg/m2 día 1 vinorelbine 25 mg/m2/días 1 y 8 cetuximab 400 mg/m2 día 1 seguido de 250 mg/m2 semanal esquemas de 21 días <br> |
| | |
| | <br> |
| | |
| | '''Terapias de Mantenimiento en primera línea: '''sólo en pacientes con variedad de adenocarcinoma, con el adecuado status performance, sin historia de hemoptisis, previa presentación en junta del servicio de oncología |
| | |
| | #Bevacizumab: 15 mg /kilo cada 21 días después de 4-6 ciclos de terapia de combinación quimioterapia, hasta progresión |
| | #Cetuximab: 250 mg/m2 semanal después de 4-6 ciclos de terapia de combinación con quimioterapia, hasta progresión |
| | #Premetrexed: 500 mg/m2 cada 21 días después de 4-6 ciclos de terapia de combinación con derivados de platino, hasta progresión |
| | #Erlotinib: 150 mg día, después de terapia de combinación con bevacizumab solo o asociado a éste (en pacientes con do- cumentación de la mutación de E. G. F. R.)<br> |
| | |
| | <br> |
| | |
| | '''Opciones de tratamiento en pacientes que no puedan recibir platinos''' |
| | |
| | <br> |
| | |
| | #Gemcitabine más docetaxel: gemcitabine 1.000 mg/m2 días 1,8 más docetaxel 85 mg/m2 día 8 cada 3 semanas |
| | #Gemcitabine más paclitaxel: gemcitabine 1.000 mg/m2 días 1,8 más paclitaxel 200 mg/m2 día 1 cada 3 semanas |
| | #Paclitaxel más vinorelbine: paclitaxel 135 mg/m2 día 1, vinorelbine 25 mg/m2 día 1 cada 2 semanas |
| | #Gemcitabine más vinorelbine: gemcitabine 1.000 mg/m2 días 1,8 más vinorelbine 25 mg/m2 días 1,8 cada 3 semanas |
| | #Erlotinib: 150 mg día (pacientes con status performance ECOG 2 o mayor, con comorbilidad que contraindique inicio de platino o con mutaciones de EGFR demostradas<br> |
| | |
| | <br> |
| | |
| | Todo paciente que reciba una tercera línea de tratamiento debe presentarse en junta de Oncología para evaluar el real beneficio de la intervención.<br> |
| | |
| | '''En pacientes ancianos con limitado estado performance:'''<span style="line-height: 1.5em;"> </span><span style="line-height: 1.5em;">Vinorel</span><span style="line-height: 1.5em;">bine monoagente o docetaxel mo</span><span style="line-height: 1.5em;">noagente</span> |
| | |
| | #Vinorelbine 25-30 mg/m2 en días 1 y 8 of cada 21 días |
| | #Docetaxel 60 mg/m2 día 1 esquema de 21 días |
| | #Erlotinib: 150 mg día (pacientes con status performance ECOG 2 o mayor, con comorbilidad que contraindique inicio de platino o con mutaciones de EGFR demostradas<br> |
| | |
| | <br>'''Esquemas de segunda línea de tratamiento.'''<br> |
| | |
| | #Docetaxel monoagente en dosis de 75mg/m2 día 1 esquema de 21 días |
| | #Premetrexed dosis de 500 mg/m2 día 1 esquema de 21 días |
| | #Gemcitabine 1.000-1.250 mg/m2 días 1, 8, 15 o días 1 y 8 en esquema de 28 o 21 días |
| | #Vinorelbine 25-30 mg/m2 en días 1 y 8 de cada 21 días |
| | #Erlotinib 150 mg día (variedades de adenocarcinoma) (evidencia Ib) |
| | #Paclitaxel en dosis de 175 mg/m2 cada 21 días o 80 mg/m2 semanal (tiene evidencia IIa) |
| | #Continuación de esquemas de quimioterapia<br> |
| | |
| | <br> |
| | |
| | '''Esquemas de adyuvancia (-): ''' |
| | |
| | Vinorelbine 30 mg/m2 día semanal por 16 semanas más CDDP 100 mg/m2 día 1, por cuatro ciclos |
| | |
| | #Vinorelbine 25 mg/m2 semanal por 16 semanas más CDDP 50mg/m2 días 1 y 8 cada 4 semanas, por cuatro ciclos |
| | #Vinorelbine 25-30 mg/m2 días 1 y 8 más CDDP 75-80 mg día 1 ciclos de 21 días, por 4 ciclos |
| | #CDDP 100 mg/m2 día 1 más etopósido 100 mg/m2 días 1 a 3 ciclos de 28 días, por 4 ciclos |
| | #CDDP 80 mg/m2 cada 21 días más vinorelbine 4 mg/m2 semanal hasta el día 43, y posteriormente, cada 2 semanas, por 4 ciclos |
| | #El estudio CALGB 9633 no favorece a largo plazo los esquemas de combinación con carboplatino (HR 0,83, 95% CI 0.64-1.08) en términos de beneficios en supervivencia global; la dosis propuesta de paclitaxel en este estudio fue de 200 mg/m2, y la de carboplatino, de 6 por AUC. Debe dejarse como opción para pacientes que no toleren el tratamiento con CDDP <br> |
| | |
| | <br> |
| | |
| | '''Esquemas de quimiorradioterapia concomitante neoadyuvante : '''Quimiorradioterapia concomitante con radioterapia:<br> |
| | |
| | #Cisplatino 50 mg/m2 días 1, 8, 29 y 36 etopósido 50mg/m2 días 1 a 5 y 29 al 33, concomitante con radioterapia (dosis total 61 Gy) |
| | #Cisplatino 100 mg/m2 días 1,29 más vinblastina 5 mg/m2 semanal por 5 semanas, concomitante con la radioterapia 60 Gy |
| | #Cisplatino 100 mg/m2 días 1,29 más vinblastina 5 mg/m2 semanal días 1, 8, 15, 22, 29 más radioterapia con 60Gy |
| | #Paclitaxel 45-50 mg/m2 semanal infusión de 1 hora más carboplatino AUc 2 mg/ml/min semanal más radioterapia 63 Gy<br> |
| | |
| | <br> |
| | |
| | '''Concurrente quimiorradioterapia seguida de radioterapia:''' |
| | |
| | Cisplatino 50 mg/m2 días 1, 8, 29, 36 más etopósido 50 mg/m2 días 1 a 5 y 29 al 33, concomitante con radioterapia dosis de 61Gy, seguido de etopósido 50 mg/ m2 por dos ciclos, o dos ciclos de docetaxel 75 mg/m2 cada 21 días, por 3 dosis iniciados 4 a 6 semanas después de la radioterapia |
| | |
| | #Paclitaxel 45-50 mg/m2 semanal más carboplatino AUC 2 mg/ml/min, más radioterapia concomitante 63 GY, seguido de paclitaxel 200 mg/m2 más carboplatino AUC 6 mg/ml/min, cada 21 días, por 2 ciclos.<br> |
| | |
| | <br> |
| | |
| | '''Intervención-indicaciones de radioterapia'''<br> |
| | |
| | La radioterapia podrá ser utilizada con técnica convencional, conformacional, de intensidad modulada (IMRT) o radioterapia intraoperatoria, según indicación médica del oncólogo radioterapeuta o los protocolos específicos del grupo de Radioterapia.<br> |
| | |
| | = Anexos = |
| | |
| | [http://75.126.65.106/~incancer/instituto//files/libros/archivos/f670452ca9b4cca55eff025b8e8ffe2c_Potocolos%20de%20Manejo%20del%20Paciente%20con%20C%C3%A1ncer.pdf Protocolos de Manejo del Paciente con Cáncer] |
Regresar a Consulta Especializada
Regresar a Procedimiento de evaluación de guías de practica clínica
Identificación
|

|
Nombre
|
Código
|

|
|
Guía de Practica clínica (GPC) Para el Tratamiento Farmacologico y Seguimiento del Paciente con Cancer de Pulmon
|
PGD1E7
|
|
Fecha de Emisión
|
Fecha de Actualización
|
Versión
|
|
2011/09/08
|
2025-10-31
|
4
|
Elaboró: Documento adaptado de las guías de manejo del Instituto Nacional de Cancerología de Colombia y el Ministerio de Protección Social
Revisó y Autorizo Ultima Versión: Comité de tumores 2019/05/11
Objetivo
Servir de apoyo al personal de Oncomedic ltda, para establecer los criterios mínimos indispensables para el adecuado manejo y seguimiento de pacientes con cáncer de pulmon céluas pequeñas, de acuerdo al estadio, que garanticen una atención médica integral, homogénea, con calidad, equidad y eficiencia articulada a los protocolos de manejo del instituto Nacional de Cancerologia.
Alcance
Las recomendaciones generadas en esta guía podrán contribuyen a la toma de decisiones clínicas.
Marco Conceptual
El cáncer de pulmón es la patología maligna mas frecuente en el mundo durante varias décadas, en 2008 se estimaron 1.610.000 casos nuevos, lo que representa el 12,7% del total de casos nuevos de cáncer (sin incluir cáncer de piel) de todo el mundo. En Colombia se estiman 2.697 casos nuevos anuales en hombres, y 1.772 en mujeres, con tasas de incidencia de 16,3 casos nuevos por 100.000 hombres y 8,6 casos nuevos por 100.000 mujeres (1).
El cáncer de pulmón es clasificado clínicamente como de células pequeñas (14%), y de células no pequeñas (85%), para efectos de tratamiento.
El instituto nacional de cancerologia publico la 1 versión del Protocolo de manejo de la paciente con cáncer de cuello del útero en el 2009 y fue actualizado noviembre del 2010 como un aporte para el adecuado manejo de esta entidad patológica.
Acorde a la propuesta del ministerio de protección social y articulada a las características de oncomedic ltda la organización adapta las guías, de modo que aplica sin modificación las recomendaciones que pueden ser seguidas dentro de la organización de acuerdo a los estados clínicos de la enfermedad.
Descripción
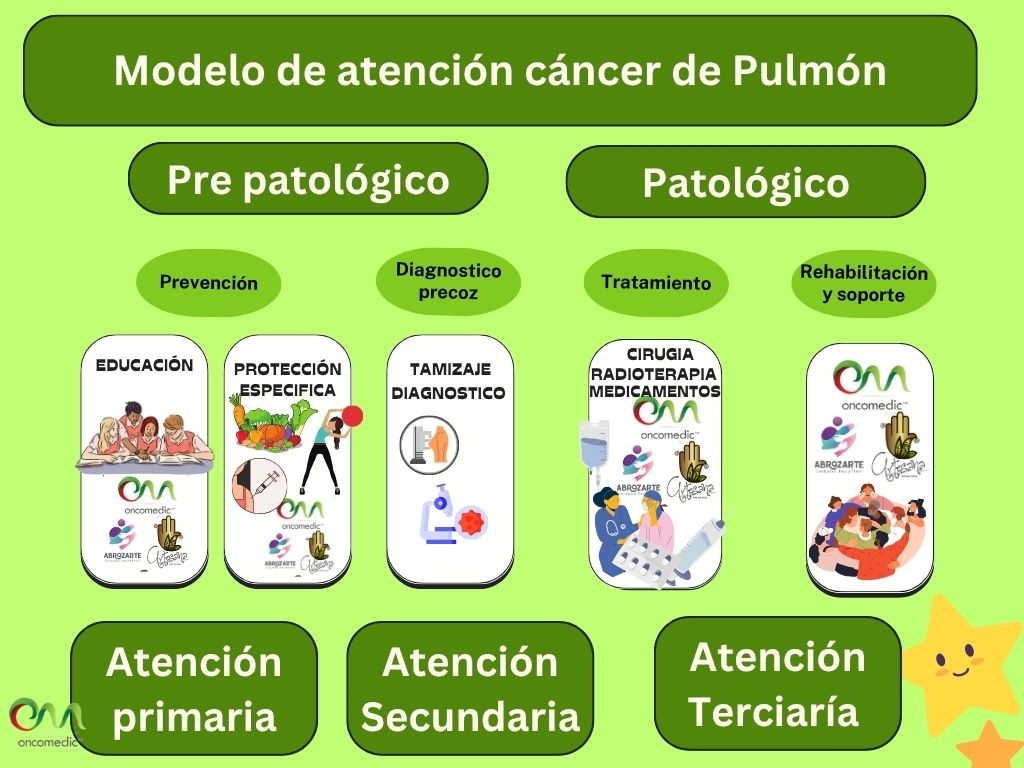 Ruta de atención en cáncer de pulmón
Ruta de atención en cáncer de pulmón
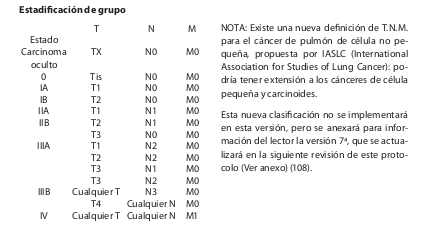
Clasificación TNM
American Joint Committee on Cancer, (6a edición) .
Tumor primario
- T0: No hay evidencia de tumor primario.
- TX: Tumor primario que no puede ser evaluado, o tumor certificado por la presencia de células malignas en el esputo o lavado bronquial, pero no visualizado por imágenes o broncoscopia
- T1: Tumor menor de 3 cm en su diámetro mayor, rodeado por pulmón o pleura visceral, sin evidencia broncoscópica de invasión más proximal del bronquio lobar (no en bronquio principal).
- T2: Tumor con cualquiera de los siguientes características de tamaño o extensión:
- Mas de 3 cm en su diámetro mayor
- Compromiso de bronquio principal, a >2 cm distal de la carina
- Invasión de pleura visceral asociado a atelectasia o neumonitis obstructiva extendida al hilio, pero que no compromete el pulmón entero
- T3: Tumor de cualquier tamaño que invade directamente cualquiera de los siguientes sitios:
- Pared torácica (incluyendo tumores del sulcus superior)
- Diafragma
- Pleura mediastinal
- Pericardio parietal
- Tumor en bronquio principal a mas de 2 cm distal de la carina, pero sin compromiso de ésta o atelectasia asociada, o neumonitis obstructiva del pulmón entero
- T4: Tumor de cualquier tamaño que invade cualquiera de los siguientes estructuras:
- Mediastino
- Corazón
- Grandes vasos
- Tráquea
- Esófago
- Cuerpos vertebrales
- Carina
- Tumor con derrame pleural o pericárdico maligno, o con nódulos(s) tumoral(s) satélite(s) dentro del lóbulo tumoral primario del pulmón.
Ganglios linfáticos regionales (N)
- NX: Ganglios linfáticos regionales que no pueden ser evaluados
- N0: Sin metástasis en ganglios linfáticos regionales.
- N1: Metástasis en ganglios linfáticos peribronquiales ipsilaterales o hiliares ipsilaterales, y compromiso de ganglios intrapulmonares por extensión directa del tumor primario.
- N2: Metástasis a ganglio(s) linfáticos ipsilaterales mediastinales o subcarinales.
- N3: Metástasis a ganglio(s) linfáticos mediastinales contralaterales, hiliares contralaterales, escalenos ipsilaterales o contralaterales, o supraclaviculares.
Metástasis a distancia (M)
- MX: Presencia de metástasis a distancia que no pueden ser evaluadas.
- M0: Sin metástasis a distancia.
- M1: Metástasis a distancia presentes.
a.La mayoría de los derrames pleurales asociados a cáncer de pulmón son debidos al tumor. Sin embargo, en algunos pacientes con múltiples exámenes citopatológicos negativos de derrames pleurales no sanguinolentos, no exudativos o pericárdicos, en los que el juicio clínico dicta que no están relacionados con el tumor, el derrame debería ser excluido como elemento de estadificación de la enfermedad del paciente como T1, T2, o T3.
b.Los nódulos tumorales metastásicos alejados del lóbulo tumoral primario del pulmón son clasificados como M1.
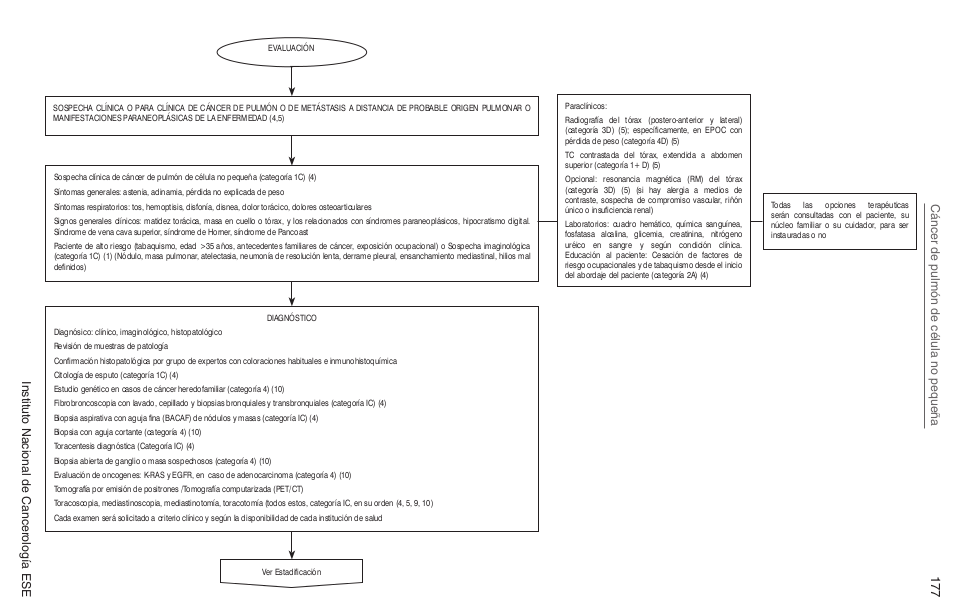
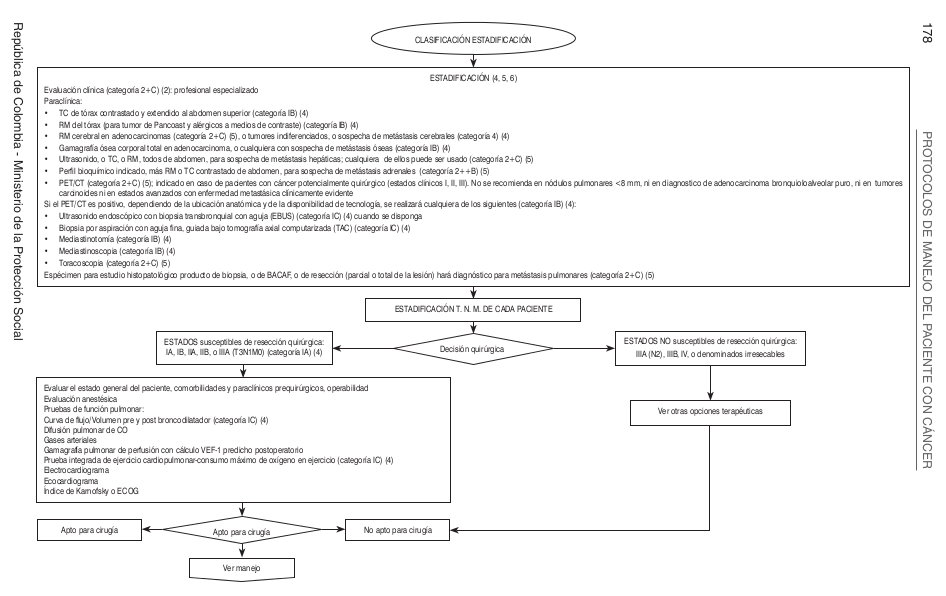
Algoritmos
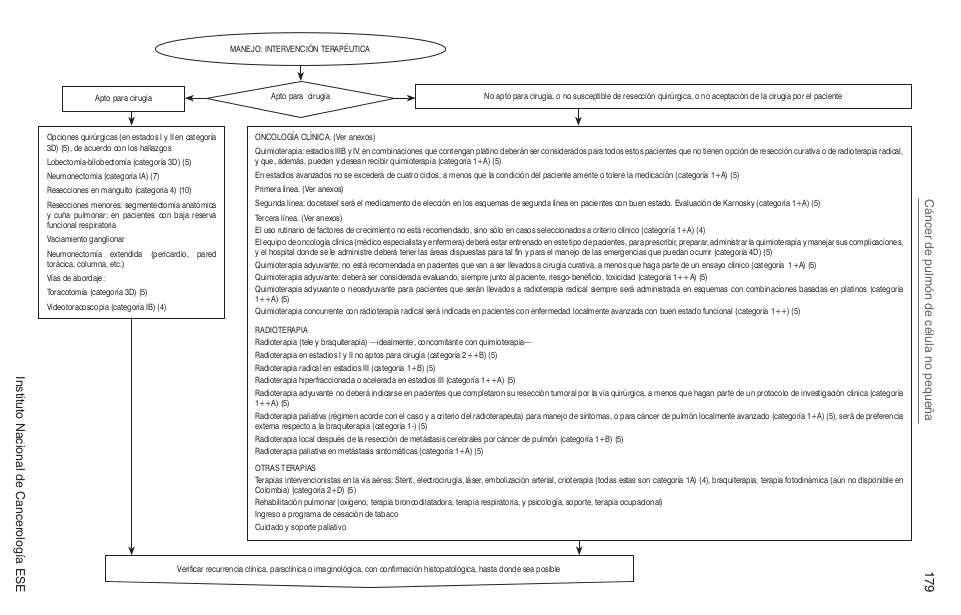
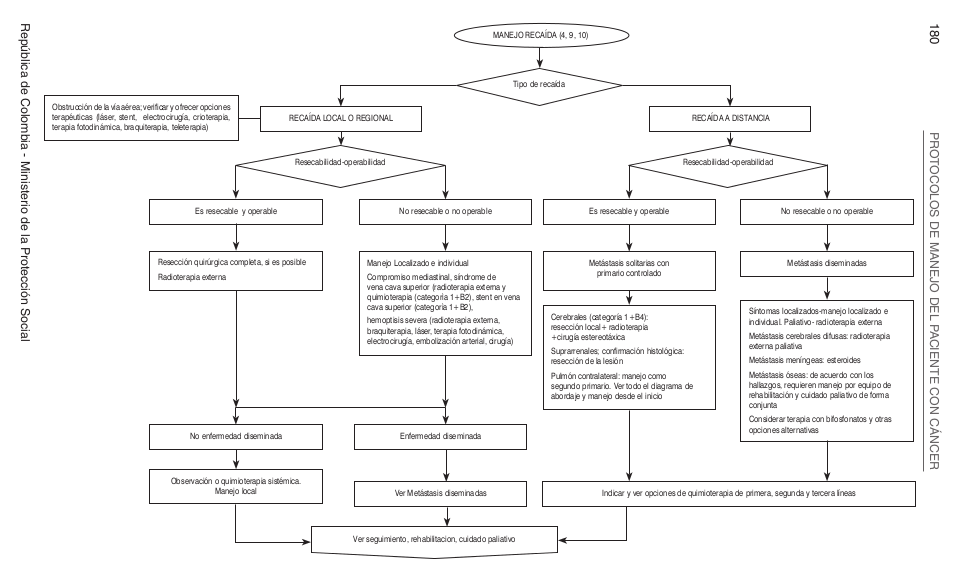
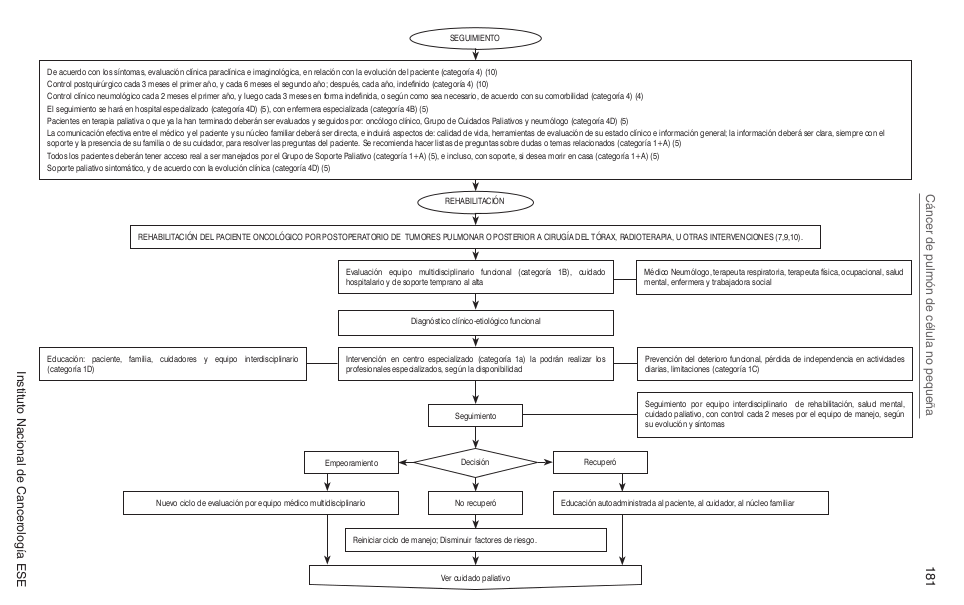
Intervenciones de Oncología Clínica Esquemas de Qumioterapia
- Esquemas en primera línea de cáncer de pulmón
- Carboplatino más paclitaxel: paclitaxel 225 mg/m2 infusión de 3 horas más carboplatino AUC 6 mg/ml/min día 1 esquema de 21 días, paclitaxel 175 mg/m2 infusión de 3 horas más carboplatino AUC 6 mg/ml/min día 1 esquema de 21 días
- Carboplatino AUC 2mg/ml/min más paclitaxel 100 mg/m2 semanal
- Cisplatino más etpósido: cisplatino 100mg/m2 día 1 más etpósido 100 mg /m2 días 1 a 3 cada 21 días
- Cisplatino más vinorelbine: cisplatino 100 mg/m2 día1 más vinorelbine 25 mg/ m2 días 1, 8,15, 22 cada 21 días
- Cisplatino más paclitaxel: cisplatino 75 mg/m2 día 1 más paclitaxel 135 mg/m2 día 1 cada 21 días
- Cisplatino más docetaxel: cisplatino 75 mg/m2 más docetaxel 75 mg/m2 cada 21 días
- Carboplatino más docetaxel: carboplatino auc 6 mg/ml/min día 1 más docetaxel 75 mg/m2 cada 21 días
- Cisplatino más gemcitabine: cisplatino 100 mg/m2 día 1 más gemcitabine 1000 mg/m2 días 1, 8, 15, esquema cada 28 días
- Carboplatino más gemcitabine: carboplatino 5 auc mg/ml/min día 1, gemcitabine 1200 mg/m2 días 1 y 8 cada 3 semanas
- Cisplatino más premetrexed: cisplatino 75 mg/m2 día 1 más premetrexed 500 mg/m2 día 1 esquema de 21 días
- Cisplatino más irinotecan: cisplatino 80mg/m2 día 1, irinotecan 60 mg/m2 días 1, 8, 15 cada 4 semanas
- Carboplatino más premetrexed: carboplatino auc 5mg/ml/min día 1 premetrexed 500 mg/m2 cada 21 días (31)
- Carboplatino más vinorelbine: carboplatino auc 4 mg/ml/min día 1 más vinorelbine 25mg/m2 día 1 esquema de 21 días (32)
Esquemas con Bevacizumab en primera línea: Sólo en pacientes con variedad de adenocarcinoma, con el adecuado escala funcional (PS), sin historia de hemoptisis, previa presentación en junta del servicio de oncología):
- Cisplatino 80 mg /m2 día 1 más gemcitabine 1250 mg/m2 día 1 y 8 más bevacizumab 15 mg /kilo día 1 esquema de 21 días
- Paclitaxel 200 mg /m2 más carbopblatino 6 x auc más bevacizumba 15 mg/kilo día 1 esquema de 21 días
- Esquemas con Cetuximab en primera línea (Sólo en pacientes con variedad de adenocarcinoma, con el adecuado estado general, previa presentación en junta del servicio de oncología)
- Cisplatino 80 mg/m2 día 1 vinorelbine 25 mg/m2/días 1 y 8 cetuximab 400 mg/m2 día 1 seguido de 250 mg/m2 semanal esquemas de 21 días
Terapias de Mantenimiento en primera línea: sólo en pacientes con variedad de adenocarcinoma, con el adecuado status performance, sin historia de hemoptisis, previa presentación en junta del servicio de oncología
- Bevacizumab: 15 mg /kilo cada 21 días después de 4-6 ciclos de terapia de combinación quimioterapia, hasta progresión
- Cetuximab: 250 mg/m2 semanal después de 4-6 ciclos de terapia de combinación con quimioterapia, hasta progresión
- Premetrexed: 500 mg/m2 cada 21 días después de 4-6 ciclos de terapia de combinación con derivados de platino, hasta progresión
- Erlotinib: 150 mg día, después de terapia de combinación con bevacizumab solo o asociado a éste (en pacientes con do- cumentación de la mutación de E. G. F. R.)
Opciones de tratamiento en pacientes que no puedan recibir platinos
- Gemcitabine más docetaxel: gemcitabine 1.000 mg/m2 días 1,8 más docetaxel 85 mg/m2 día 8 cada 3 semanas
- Gemcitabine más paclitaxel: gemcitabine 1.000 mg/m2 días 1,8 más paclitaxel 200 mg/m2 día 1 cada 3 semanas
- Paclitaxel más vinorelbine: paclitaxel 135 mg/m2 día 1, vinorelbine 25 mg/m2 día 1 cada 2 semanas
- Gemcitabine más vinorelbine: gemcitabine 1.000 mg/m2 días 1,8 más vinorelbine 25 mg/m2 días 1,8 cada 3 semanas
- Erlotinib: 150 mg día (pacientes con status performance ECOG 2 o mayor, con comorbilidad que contraindique inicio de platino o con mutaciones de EGFR demostradas
Todo paciente que reciba una tercera línea de tratamiento debe presentarse en junta de Oncología para evaluar el real beneficio de la intervención.
En pacientes ancianos con limitado estado performance: Vinorelbine monoagente o docetaxel monoagente
- Vinorelbine 25-30 mg/m2 en días 1 y 8 of cada 21 días
- Docetaxel 60 mg/m2 día 1 esquema de 21 días
- Erlotinib: 150 mg día (pacientes con status performance ECOG 2 o mayor, con comorbilidad que contraindique inicio de platino o con mutaciones de EGFR demostradas
Esquemas de segunda línea de tratamiento.
- Docetaxel monoagente en dosis de 75mg/m2 día 1 esquema de 21 días
- Premetrexed dosis de 500 mg/m2 día 1 esquema de 21 días
- Gemcitabine 1.000-1.250 mg/m2 días 1, 8, 15 o días 1 y 8 en esquema de 28 o 21 días
- Vinorelbine 25-30 mg/m2 en días 1 y 8 de cada 21 días
- Erlotinib 150 mg día (variedades de adenocarcinoma) (evidencia Ib)
- Paclitaxel en dosis de 175 mg/m2 cada 21 días o 80 mg/m2 semanal (tiene evidencia IIa)
- Continuación de esquemas de quimioterapia
Esquemas de adyuvancia (-):
Vinorelbine 30 mg/m2 día semanal por 16 semanas más CDDP 100 mg/m2 día 1, por cuatro ciclos
- Vinorelbine 25 mg/m2 semanal por 16 semanas más CDDP 50mg/m2 días 1 y 8 cada 4 semanas, por cuatro ciclos
- Vinorelbine 25-30 mg/m2 días 1 y 8 más CDDP 75-80 mg día 1 ciclos de 21 días, por 4 ciclos
- CDDP 100 mg/m2 día 1 más etopósido 100 mg/m2 días 1 a 3 ciclos de 28 días, por 4 ciclos
- CDDP 80 mg/m2 cada 21 días más vinorelbine 4 mg/m2 semanal hasta el día 43, y posteriormente, cada 2 semanas, por 4 ciclos
- El estudio CALGB 9633 no favorece a largo plazo los esquemas de combinación con carboplatino (HR 0,83, 95% CI 0.64-1.08) en términos de beneficios en supervivencia global; la dosis propuesta de paclitaxel en este estudio fue de 200 mg/m2, y la de carboplatino, de 6 por AUC. Debe dejarse como opción para pacientes que no toleren el tratamiento con CDDP
Esquemas de quimiorradioterapia concomitante neoadyuvante : Quimiorradioterapia concomitante con radioterapia:
- Cisplatino 50 mg/m2 días 1, 8, 29 y 36 etopósido 50mg/m2 días 1 a 5 y 29 al 33, concomitante con radioterapia (dosis total 61 Gy)
- Cisplatino 100 mg/m2 días 1,29 más vinblastina 5 mg/m2 semanal por 5 semanas, concomitante con la radioterapia 60 Gy
- Cisplatino 100 mg/m2 días 1,29 más vinblastina 5 mg/m2 semanal días 1, 8, 15, 22, 29 más radioterapia con 60Gy
- Paclitaxel 45-50 mg/m2 semanal infusión de 1 hora más carboplatino AUc 2 mg/ml/min semanal más radioterapia 63 Gy
Concurrente quimiorradioterapia seguida de radioterapia:
Cisplatino 50 mg/m2 días 1, 8, 29, 36 más etopósido 50 mg/m2 días 1 a 5 y 29 al 33, concomitante con radioterapia dosis de 61Gy, seguido de etopósido 50 mg/ m2 por dos ciclos, o dos ciclos de docetaxel 75 mg/m2 cada 21 días, por 3 dosis iniciados 4 a 6 semanas después de la radioterapia
- Paclitaxel 45-50 mg/m2 semanal más carboplatino AUC 2 mg/ml/min, más radioterapia concomitante 63 GY, seguido de paclitaxel 200 mg/m2 más carboplatino AUC 6 mg/ml/min, cada 21 días, por 2 ciclos.
Intervención-indicaciones de radioterapia
La radioterapia podrá ser utilizada con técnica convencional, conformacional, de intensidad modulada (IMRT) o radioterapia intraoperatoria, según indicación médica del oncólogo radioterapeuta o los protocolos específicos del grupo de Radioterapia.
Anexos
Protocolos de Manejo del Paciente con Cáncer
 Ruta de atención en cáncer de pulmón
Ruta de atención en cáncer de pulmón







