|
|
| (No se muestran 25 ediciones intermedias del mismo usuario) |
| Línea 1: |
Línea 1: |
| [[Proceso_de_consulta_especializada|Regresar a Consulta Especializada]] | | [[Proceso de consulta especializada|Regresar a Consulta Especializada]] |
|
| |
|
| <br> <br> <u>'''Protocolo de Manejo Adoptado de las guías de practica clínica del Instituto Nacional de Cancerología de Colombia'''</u><br>
| | [[Procedimiento_de_Evaluaci%C3%B3n_y_Adopci%C3%B3n_de_Guias_de_Practica_Cl%C3%ADnica|Regresar a Procedimiento de evaluación de guías de practica clínica]] |
|
| |
|
| <u</u>
| | <br> |
| | |
| | = Identificación = |
| | |
| | {| width="665" cellspacing="0" cellpadding="4" |
| | |- valign="TOP" |
| | | width="129" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" rowspan="4" | |
| | <br> [[Image:Oncomedic.png]]<br> |
|
| |
|
| = Aspectos Generales = | | | width="327" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" colspan="2" | |
| | '''Nombre''' |
|
| |
|
| <br>El adenocarcinoma de próstata es el cáncer mas frecuente (excluyendo el cáncer de piel) y la segunda causa de mortalidad por cáncer (después del cáncer pulmonar) en hombres, en Estados Unidos. La incidencia de cáncer de próstata en Estados Unidos para 1998 fue de 185,5 x 100.000, con una mortalidad de 39,2 x 100.000. En el Instituto Nacional de Cancerología de Colombia es el tercero mas frecuente en hombres, después de los cánceres de piel y de estómago; en 1988 se registraron 160 casos nuevos.
| | | width="64" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Código''' |
|
| |
|
| = Factores de Riesgo = | | | width="111" style="border: 1px solid #000000; padding: 0.1cm" rowspan="4" | |
| | [[Image:Saludarte.png]] |
|
| |
|
| *'''Raza:''' Los pacientes norteamericanos de raza negra tienen la incidencia más alta en el mundo. Estudios en comunidades afro-americanas jamaiquinas y algunas observaciones de brigadas de salud en comunidades del Chocó, Colombia, confirman una muy alta incidencia en la raza negra. En cada estado clínico los pacientes de raza negra presentan tumores de mayor volumen, menor edad en el momento del diagnóstico, antígeno prostático específico (APE) más elevado y pronóstico más pobre.
| | |- valign="TOP" |
| *'''Historia Familiar:''' El riesgo relativo aumenta en 2 a 3 veces en pacientes con un pariente en primer grado de consanguinidad con cáncer de próstata, y es 5 veces más alto si son dos los parientes afectados. Entre los pacientes menores de 55 años con cáncer de próstata, 43% tienen historia familiar positiva, en comparación con 34% de los diagnosticados antes de los 70 años.
| | | width="327" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" colspan="2" | |
| *'''Dieta:''' La dieta baja en grasas y baja en calcio parece disminuir el riesgo de cáncer de próstata. Estudios recientes sugieren un efecto protector de la vitamina E (alfa tocoferol) y de los licopenos (presentes en el tomate), así como del ejercicio y la actividad física regular.
| | Guía de Practica clínica (GPC) Para el Tratamiento Farmacologico y Seguimiento del Paciente con Cancer de Prostata |
| *'''Historia Natural:''' En estudios de autopsias se encuentra una prevalencia histológica de cáncer de próstata del orden de 30 a 40 % en los varones mayores de 50 años. Sin embargo, de éstos se calcula que sólo 1,5% se hacen clínicamente detectables cada año. El carcinoma de próstata es progresivo y su agresividad biológica está directamente relacionada con el grado de diferenciación (escala de Gleason); 40 a 70% de los pacientes manejados sin intención curativa desarrollan metástasis a los 10-15 años y tienen un riesgo aproximado de 60 80% de morir por la enfermedad.
| |
|
| |
|
| <br> | | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | PGD1E6 |
| | |
| | |- valign="TOP" |
| | | width="156" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Fecha de Emisión''' |
| | |
| | | width="163" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Fecha de Actualización''' |
| | |
| | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Versión''' |
| | |
| | |- valign="TOP" |
| | | width="156" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | 2011/09/08 |
| | |
| | | width="163" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | 2025-07-31 |
| | |
| | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | 4 |
| | |
| | |} |
| | |
| | <br> <u>'''Elaboró'''</u>''': '''Documento adoptado parcialmente de las guías del Ministerio de Protección Social, en lo referente a la falta de actualización por parte del ministerio se acepta referirse a las guías del NCCN<br> |
| | <u>'''Revisó y Autorizo Ultima Versión'''</u>: Comité de tumores |
| | |
| | = Objetivo = |
| | |
| | Servir de apoyo al personal de Oncomedic ltda, para establecer los criterios mínimos indispensables para el adecuado manejo farmacológico y seguimiento de pacientes con cáncer de mama, de acuerdo al estadio, que garanticen una atención médica integral, homogénea, con calidad, equidad y eficiencia articulada a las guías de practica clínica del ministerio de protección social y el instituto nacional de cancerología. |
| | |
| | = Alcance = |
| | |
| | Las recomendaciones generadas en esta guía contribuyen a la toma de decisiones clínicas. |
| | |
| | = Marco Conceptual = |
| | |
| | El Cáncer de prostata es considerada la primera causa de incidencia y la segunda de mortalidad por cáncer en la población masculina, se estiman, entre 6.500 y 8.000 casos nuevos de cáncer de próstata cada año, con una mayor incidencia en hombres mayores de 60 años. En Colombia, el cáncer de próstata muestra incremento de la tasa de incidencia, este comportamiento podría estar explicado por el incremento en la expectativa de vida de la población y el cambio en sus condiciones de vida.<br> Acorde a la propuesta del ministerio de protección social y articulada a las características de oncomedic ltda la organización adapta las guías, de modo que aplica sin modificación las recomendaciones en torno a manejo farmacológico y de seguimiento que aplican a la organización. |
| | |
| | Conforme a la guía del Ministerio las recomendaciones presentadas se dividen por estados clínicos de la enfermedad: carcinoma ductal in situ (DCIS), cáncer temprano y localmente avanzado, cáncer metástasico |
| | |
| | = Descripción = |
| | |
| | '''Ruta de atención en cáncer de Próstata''' |
| | |
| | [[Archivo:Ca prostata.jpg]] |
|
| |
|
| = Clasificación Histopatológica = | | === Clasificación del Cáncer de Próstata TNM === |
|
| |
|
| <br>Se utiliza el sistema de gradación de Gleason que analiza el grado de diferenciación glandular y el patrón de crecimiento tumoral en el estroma prostático (Grados 1 a 5). Dado que la mayoría de los cánceres prostáticos exhibe más de un patrón histológico, se asignan un grado dominante y uno secundario para obtener un puntaje de la sumatoria de los dos (puntaje de 2 a 10). <u>'''Sistema de Gleason'''</u>
| |
|
| |
|
| *Grado I: Muy bien diferenciado
| | === Solapas de Presentación del Texto Original === |
| *Grado II: Bien diferenciado
| |
| *Grado III: Moderadamente diferenciado
| |
| *Grado IV: Moderadamente a pobremente diferenciado
| |
| *Grado V: Indiferenciado (comedocarcinoma, carcinoma anaplásico)
| |
|
| |
|
| <br>
| | [[Image:Sol pros.png]] |
|
| |
|
| '''<u>Puntaje de Gleason</u>'''
| | === Algoritmos<br> === |
|
| |
|
| *2-4 Bien diferenciado
| | [[Image:Algo Pros.png]] |
| *5-6 Moderadamente diferenciado
| |
| *7- Moderadamente a pobremente diferenciado
| |
| *8-10 Pobremente diferenciado
| |
|
| |
|
| <br>
| | [[Image:Algo Pros1.png]] |
|
| |
|
| <u>'''Variante Histopatológica'''</u>
| | [[Image:Algo Pros2.png]] |
|
| |
|
| *Gleason Adenocarcinoma ductal Sin necrosis
| | [[Image:Algo Pros3.png]] |
| *3 endometroide Con necrosis
| |
| *5 Carcinoma indiferenciado de célula pequeña (carcinoma neuroendocrino de alto grado)
| |
| *5 Carcinoma coloide (mucinoso), Carcinoma de células en anillo de sello
| |
| *5 Carcinoma sarcomatoide
| |
| *5 Carcinosarcoma
| |
| *5 Carcinoma adenoide quístico o carcinoma de células basales
| |
| *3-5 Carcinoma de tipo linfoepiteliona
| |
| *5 Carcinoma escamocelular
| |
| *No aplica Carcinoma de células transicionales No aplica
| |
|
| |
|
| CLASIFICACIÓN CLÍNICA Y PATOLÓGICA Revisión de la Clasificación TNM(UICC 1997) Tumor primario, (T) clínico 465 CÁNCER DE PRÓSTATA TX El tumor primario no puede ser evaluado T0 No hay evidencia de tumor primario T1 Tumor primario no es clínicamente aparente (no visible, no palpable) T1a Tumor incidental en 5% o menos del tejido prostático resecado T1b Tumor incidental en más del 5% del tejido prostático resecado T1c Tumor indentificado por biopsia con aguja (por elevación del APE). T2 Tumor primario confinado a la próstata T2a Tumor compromete un lóbulo prostático T2b Tumor compromete ambos lóbulos T3 El tumor se extiende más allá de la cápsula prostática T3a extensión extracapsular uni o bilateral. T3b el tumor compromete vesículas seminales T4 Tumor fijo o que invade estructuras adyacentes diferentes de las vesículas seminales: cuello vesical, esfínter externo, recto, elevadores del ano y/o pared pélvica. Nota: el tumor detectado por biopsia en uno o ambos lóbulos prostáticos, que no es palpable o visible por imagenología, se clasifica como T1c. La invasión del ápex prostático o de la cápsula prostática (pero no más allá de estos) no se clasifica como T3, sino como T2. Tumor primario (pT) patológico pT2 Tumor confinado al órgano. pT2 - Unilateral pT2 - Bilateral pT3 Extensión extraprostática pT3a - Extensión extraprostática uni o bilateral pT3b - Invasión de vesícula seminal pT4 Invasión de recto o vejiga. Nota: no existe clasificación pT1. Ganglios linfáticos regionales (N) Nx Metástasis regionales no evaluables. N0 No hay metástasis regionales. N1 Metástasis en uno o varios Ganglios regionales. Metástasis a distancia (M) Mx Metástasis a distancia no evaluables. M0 No hay metástasis a distancia. M1 Metástasis a distancia M1a A Ganglios linfáticos no regionales M1b A hueso M1c A otro sitio. Nota: cuando hay más de un sitio de metástasis se clasifica como M1c. Control en 1 año APE NORMAL según rangos por edad o < 2,5 en ptes. con factores de riesgo
| | [[Image:Algo Pros4.png]]<br> |
|
| |
|
| Estudios de Extensión positiva APE libre / PSA total APE 2,5 - 10,0 ng/ml APE > 10,m ng/ml APE de control 3 meses negativa ecografía/ biopsias por sextantes APE ELEVADO segun rangos por edad o > 2,5 en ptes. con factores de riesgo APE tacto rectal NORMAL tacto rectal ANORMAL historia clínica examen físico tacto rectal
| | === Tratamiento<br> === |
|
| |
|
| = Diagnóstico =
| | *Para los tratamientos con intención curativa, la evidencia disponible muestra que el uso de terapia hormonal adyuvante en pacientes sometidos a radioterapia con beneficios en mortalidad global y recurrencia, sin un incremento significativo de la mortalidad. |
| | *El uso de terapia hormonal adyuvante a la prostatectomía, no ha mostrado benficios que justifiquen su uso, por el contrario, se asocia con un incremento en eventos adversos. |
| | *El uso de radioterapia adyuvante al tratamiento quirúrgico ha demostrado un efecto en la supervivencia a largo plazo, la tasa de control y el riesgo de recaída bioquímica, sin un incremento significativo de los eventos advesos.<br> |
| | *La mejor evidencia disponible de la adición de antiandrógenos se encuentra disponible para flutamida, otros antiandrógenos que han sido evaluados en ensayos clínicos son la nilutamida y el acetato de ciproterona. Por esta razón, se indican en primera línea del manejo hormonal la castración quirúrgica o médica con análogos de la LHRH. |
| | *Estudios que comparan la castración médica con la castración quirúrgica no encontraron diferencias significativas en su efectividad y balance de efectos adversos. |
| | *En el bloqueo hormonal médico los agonistas de la LHRH que han sido mejor estudiados son leuprolida, goserelina y buserelina. |
| | *Los resultados del estudio muestran que el bloqueo androgénico máximo en cáncer de próstata avanzado puede ser una alternativa costo-efectiva para el país (estudio realizado con flutamida como antiandrógeno de adición) |
| | *Se considera el uso de bloqueo simple (castración con análogos de la LHRH u orquidectomía) en primera línea de manejo hormonal en cáncer avanzado, y la adición de un antiandrógeno se considera alternativa de segunda línea. |
| | *Una revisión de ensayos clínicos muestra que el uso de dietilestilbestrol (DES) podría ser de utilidad en el manejo de las oleadas de calor en el paciente en comparación con otras alternativas. |
| | *La evidencia disponible no permite establecer una recomendación sobre el manejo de la ginecomastia en pacientes con bloqueo hormonal; se recomienda que en caso de requerirse este manejo especializado, se realice en conjunto entre urología, radioterapia y oncología. |
| | *La evidencia clínica de los esquemas de quimioterapia en pacientes con cáncer de próstata hormono refractario indica la utilidad de la combinación de Docetaxel más prednisolonaen términos de mortalidad global, reducción del dolor y calidad de vida (53); esta comparación se realiza contra el esquema mitoxantrona más prednisolona. |
| | *El uso de combinaciones de quimioterapia no demostró un balance riesgo-beneficio favorable que indicara su realización (54), en especial la adición de estramustina no muestra un beneficio importante (55). Las toxicidades en los esquemas con docetaxel fueron superiores. |
| | *En cáncer de próstata hormonorefractario, el tratamiento con docetaxel cada tres semanas más prednisolona es costo-efectivo para Colombia (anexo 11, GPC completa). |
| | *Las combinaciones de quimioterapia mitoxantrona + prednisolona, do-cetaxel + estramustina, docetaxel + estramustina + prednisolona, y prednisolona sola fueron menos costo-efectivas. |
| | *Nuevos medicamentos, como la arabiraterona y el sipuleucel-T, no fueron evaluados y pueden ser considerados acorde con la evidencia disponible en actualizaciones posteriores de la presente guía. |
| | *Los bifosfonatos en tratamiento de cáncer avanzado con metástasis óseas |
|
| |
|
| Exámenes de laboratorio Antígeno Prostático Especifico (APE) Es una proteína serina-proteasa de 33 Kd, cuya función es la lisis del coágulo seminal. Se encuentra en el fluido prostático en concentraciones de 1.000.000 ng/ml, y en el suero en concentraciones usualmente <4 ng/ml. Es la mejor herramienta de tamizaje y de seguimiento en pacientes con cáncer de próstata. La elevación aguda de sus niveles séricos se debe a: - Prostatitis aguda - Biopsia con aguja - Retención urinaria aguda La elevación puede ser transitoria, por lo cual debe evitarse su determinación inmediatamente después de: - Masaje prostático vigoroso - Cateterismo uretral - Cistoscopia - Eyaculación Sus niveles séricos se reducen en 50% en pacientes con 6 o más meses de tratamiento con Inhibidor de 5 alfa reductasa 5 mg/día, de manera que el valor real para estos pacientes debe estimarse en el doble del obtenido para fines de diagnóstico. En pacientes asintomáticos sin factores de riesgo, la determinación de los niveles de APE y su interpretación según rangos de edad (Tabla 1) puede disminuir el número de biopsias innecesarias. En pacientes con factores de riesgo (por ej, raza negra o historia familiar), el nivel recomendado es mayor de 2,5 ng/ml, independiente de la edad. Tabla 1 Rango de edad APE total ng/ml 40 49 0 2,5 50 59 0 3,5 60 69 0 4,5 70 79 0 6,5 APE libre La medición del índice APE libre/APE total es útil en niveles de APE total de 2,5 a 10,0 ng/ml, para mejorar la especificidad del antígeno en el diagnóstico de cáncer prostático. Con índices de 0,07 o menos, la probabilidad de cáncer se acerca a 90%. El índice límite no está definido, pero se recomienda 0,25 para tomar conducta sobre biopsia o seguimiento. La densidad de APE (APE total sobre volumen de la próstata expresado en cc y determinado por ecografía >1,5 ng/ml/cc y la velocidad de APE >0,75 ng/ml/año de edad sugieren la presencia de cáncer. Estos parámetros pueden usarse como medidas auxiliares, a pesar de sus limitaciones prácticas y técnicas. La fosfatasa ácida prostática (PAP) no aporta información adicional al APE. No debe usarse. Biopsias Técnica estándar: Biopsias dirigidas por ecografía mediante ultrasonografía transrectal de lesiones hipoecoicas visibles y por sextantes, de la zona periférica de la glándula (ápex, parte medio y no se recomienda y base de cada lóbulo prostático). Las biopsias de la zona transicional están indicadas en pacientes con biopsias negativas previas y persistencia de APE elevado. Estudios radiográficos La tomografía axial computarizada (TAC) tiene poca utilidad en el diagnóstico de metástasis regionales a ganglios linfáticos, con tasas detección de 1,5% en pacientes con APE superior a 20 ng/ml. La mayoría de los pacientes con ganglios positivos sin metástasis a distancia se presentan con enfermedad microscopica no detectable por imágenes y la linfadenectomía pélvica es el procedimiento de elección para estadificación. La TAC no tiene un costo beneficio aceptable y debería reservarse para casos seleccionados: APE muy superior a 20 ng/ml. · Pacientes que acepten biopsia por aspiración percutánea. · Pacientes que probablemente no se someterán a estadificación quirúrgica La resonancia magnética endorectal es un procedimiento costoso, que no da mejor información que el ultrasonido. No se recomienda su uso de rutina. La Ultrasonografía transrectal de la próstata no se justifica si no se van a practicar biopsias ecodirigidas, en el paciente con sospecha de cáncer de próstata. Medicina nuclear La gamagrafía ósea es estudio obligatorio inicial en pacientes con APE >10 ng/ml. La probabilidad de una gamagrafía positiva en pacientes con niveles de APE inferiores a 10 es menor del 1%.
| | = Anexos = |
|
| |
|
| <br>
| | [http://gpc.minsalud.gov.co/Documents/Guias-PDF-Recursos/Prostata/(GPC)%20Ca%CC%81ncer%20de%20pro%CC%81stata_final_Prof.Salud%20final%20(Web).pdf Guía de Práctica clínica (GPC) Para la Detección Temprana, Diagnóstico, Tratamiento, Seguimiento y Rehabilitación del Cáncer de Próstata] |
|
| |
|
| = Tratamiento =
| | [http://gpc.minsalud.gov.co/Documents/Guias-PDF-Recursos/Prostata/GPC_Comple_Prostata.pdf Guía de Práctica clínica (GPC) Para la Detección Temprana, Diagnóstico, Tratamiento, Seguimiento y Rehabilitación del Cáncer de Próstata(Completa)] |
|
| |
|
| <br>El tratamiento depende del estado del tumor en el momento del diagnóstico. Se emplean cuatro modalidades terapéuticas principales: 1. Tratamiento quirúrgico 2. Radioterapia 2. Terapia hormonal 3. Observación Tratamiento Quirúrgico Carcinoma de próstata localizado < cT2b Nx Mo - Prostatectomía radical retropúbica, con linfadenectomía pélvica bilateral. - Prostatectomía radical perineal, sin linfadenectomía pélvica en pacientes con: - APE menor de 10 ng/ml. - Puntaje de Gleason <7 en las biopsias. - Con linfadenectomía pélvica previa negativa (por vía abierta o laparoscópica) Tratamiento quirúrgico recomendado en pacientes con: · Expectativa de vida mayor de 10 años, idealmente mayor de 15 (en nuestro medio, en general, pacientes menores de 70). · Historia familiar de longevidad importante. · APE menor de 20 ng/ml. Como herramienta predictiva del estado patológico final se recomienda uso de las Tablas de Partin. La opción de técnica preservadora de nervios en pacientes sin disfunción eréctil, se hace de acuerdo a la evaluación intraoperatoria y el nomograma de Partin. 469 CÁNCER DE PRÓSTATA En cerca de 90% de los pacientes con estados T1a se encuentra adenocarcinoma residual después de prostatectomía radical, en su mayoría con volúmenes inferiores a 1 cc. Aquellos con APE post resección transuretral menor o igual a 1,0 ng/ml tienen menor riesgo de progresión y son buenos candidatos para observación. RADIOTERAPIA - Radioterapia externa (teleterapia) Con tratamiento hormonal neoadyuvante por un mínimo de 3 meses · Pacientes con expectativa de vida >7 años. · Cualquier puntaje de Gleason. · Linfadenectomía pélvica negativa y cualquier APE. · Sin linfadenectomía, en pacientes con puntaje de Gleason <7 y APE < 10 ng/ml. - Braquiterapia Con Tratamiento Hormonal neoadyuvante por un mínimo de 3 meses, para glándulas > 70 cc por ecografía. · Pacientes con expectativa de vida > de 7 años. · APE menor de 10 ng/ml. · Puntaje de Gleason menor de 7. · No es recomendada en pacientes con historia de resección transuretral de próstata. SEGUIMIENTO APE y examen físico cada 3 - 4 meses durante los primeros 2 años, luego cada 6 meses. TRATAMIENTO HORMONAL Orquidectomía quirúrgica o médica (ej: con agonista de LHRH) Tratamiento hormonal intermitente Tratamiento hormonal con preservación de la potencia Monoterapia con antiandrógeno no esteroide, con o sin agente inhibidor de 5 alfa - reductasa. OBSERVACIÓN En pacientes de edad avanzada o con co-morbilidad importante y puntajes de Gleason <8. 470 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) Pacientes que rechazan tratamiento. Seguimiento clínico y bioquímico para prevención de complicaciones debido a progresión de la enfermedad. Carcinoma de próstata localmente avanzado cT3 a-b Nx Mo Radioterapia Teleterapia con tratamiento hormonal neoadyuvante por un mínimo de tres meses, con o sin linfadenectomía previa negativa. La braquiterapia no está indicada en enfermedad localmente avanzada como monoterapia, pero sí en combinacion con teleterapia. Tratamiento hormonal Orquidectomía quirúrgica o médica. Tratamiento hormonal intermitente Tratamiento hormonal con preservación de la potencia Monoterapia con antiandrógeno no esteroide, con o sin agente inhibidor de 5 alfa - reductasa. Prostatectomía radical retropúbica con linfadenectomía pélvica bilateral. Pacientes jóvenes seleccionados, con cT3a y Gleason <7 y APE menor de 20 ng/ml, pueden considerarse para esta cirugia, pues hasta un 25% pueden estar sobreestadificados y ser pT2. Observación En pacientes de edad avanzada y comorbilidad importante y puntajes de Gleason <8, y en aquellos que rechazan otros tratamientos. Seguimiento clínico y bioquímico para prevención de complicaciones cuando ocurre progresión de la enfermedad. Seguimiento APE y examen físico cada 3 - 4 meses. Carcinoma de próstata con extensión regional, cualquier T N1 M0 Tratamiento hormonal Orquidectomía quirúrgica o médica. 471 CÁNCER DE PRÓSTATA Tratamiento hormonal intermitente Hormonoterapia con preservación de la potencia Monoterapia con antiandrógeno no esteroide, con o sin agente inhibidor de 5 alfa reductasa. Observación En pacientes de edad avanzada o con co-morbilidad importante y en aquellos que rechazan tratamiento. Seguimiento clínico y bioquímico para prevención de complicaciones cuando ocurre progresión de la enfermedad. Carcinoma de próstata metastásico, cualquier T cualquier N M1a-c. Tratamiento hormonal Orquidectomía quirúrgica o médica. Tratamiento hormonal Intermitente Hormonoterapia con preservación de la potencia Monoterapia con antiandrógeno no esteroideo, con o sin agente inhibidor de alfa reductora. Observación En pacientes de edad avanzada o con co-morbilidad importante. En aquellos que rechazan tratamiento. Seguimiento clínico y bioquímico, para prevención de complicaciones cuando ocurre progresión de la enfermedad. Carcinoma de próstata metastásico hormonoindependiente Supresión del antiandrógeno En pacientes en tratamiento hormonal combinado, se puede observar respuesta clínica con disminución del APE por periodos de 2-10 meses. * Siempre requiere bloqueo en el momento de máximo estímulo ( flare), con administración previa de antiandrógeno no esteroideo por 2 semanas. 472 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) Terapia de 2ª línea (una de las siguientes) Dietilestilbestrol (DES), 1 mg/día. Ketoconazol, 200 mg c/8h. Prednisona, 10 mg/día. Bicalutamida, 150 mg/día. Radioterapia externa paliativa En dosis total de 3000 a 3500 cGy, con fracciones de 300 cGy, 5 veces a la semana sobre sitios de metástasis específicos. Se obtienen 75-80% de respuestas, con control efectivo del dolor, con una duración media de 6 meses. Radiofármacos En pacientes con enfermedad metastásica extensa se recomiendan radiofármacos de acción sistémica como el estroncio189 o el samario153. No deben usarse en pacientes candidatos a quimioterapia paliativa, por su toxicidad sobre la medula ósea. Quimioterapia paliativa Cinco esquemas se sugieren en las Guías de Manejo del NCCN (National Comprehensive Cancer Network): Ketoconazol Etopósido Mitoxantrona Estramustina Doxorubicina Prednisona Vinblastina Estramustina Paclitaxel Estramustina Terapia de soporte Prednisona 7,5 mg, VO día. Dexametasona- 0,75 mg c/12 h. Guías para el manejo de la recurrencia bioquímica (APE ) después de prostatectomía radical El riesgo de recurrencia bioquímica se relaciona directamente con - el APE preoperatorio - el puntaje de Gleason - el pT o T patológico Los Niveles de Detección de Cáncer Residual (NDCR) se definen como el APE en suero que predicen progresión bioquímica subsiguiente. Estos varían entre 0,1 y 0,6, ng/ml, según la literatura. 473 CÁNCER DE PRÓSTATA Radioterapia de rescate Radioterapia externa (RT) 64 Gy La RT produce APE no detectable en aproximadamente la mitad de los pacientes con recurrencia bioquímica entre 3 y 5 años de seguimiento. Se considera candidato ideal para rescate el paciente con: - Tumor menor de pT3b. - Puntaje de Gleason del espécimen <7. - Recurrencia bioquímica después de 1 año postoperatorio. - Tiempo de duplicación de APE >6 meses. - Paciente continente. 1. Tratamiento hormonal temprano Se considera una opción viable en pacientes con alto riesgo de progresión (recurrencia temprana, doblaje de APE en menos de seis meses, Gleason alto y T alto), aunque no se cuenta actualmente con evidencia de que el bloqueo temprano de Andrógenos signifique beneficio en cuanto a supervivencia, tasa de progresión o calidad de vida en pacientes con recurrencia puramente bioquímica. Observación Guías para el manejo de la recurrencia después de radioterapia curativa Tratamiento hormonal La recurrencia local puede preceder el desarrollo de metástasis hasta por 6 años. No hay evidencia de beneficio con el inicio temprano del tratamiento hormonal. Se recomienda en pacientes con alto riesgo de progresión o de enfermedad metastásica oculta. Cirugía radical de rescate ( prostatectomía / cistoprostatectomía) El procedimiento se asocia con morbilidad quirúrgica importante y tasas de incontinencia cercanas al 50%. Puede ser considerado en pacientes con: - APE pre radioterapia y pre-quirúrgico menor de 20 ng/ml. - Nadir de APE <1,0 ng/ml. - Tiempo de duplicación de APE después de 6 meses - Recurrencia comprobada por biopsia, más de un año después de la RT. - Estado clínico inicial T3NoMo - Expectativa de vida mayor de 10 años, buena condición general. - Sin evidencia de proctitis o cistitis post RT, persistente. - Gammagrafía ósea negativa. - Posibilidad de acceso a esfínter artificial. 474 INSTITUTO NACIONAL DE CANCEROLOGÍA (Adoptado por ONCOMEDIC Ltda) LECTURAS RECOMENDADAS 1. ARCANGELI CG, HUMPHREY PA, SMITH DS, ET AL. Percentage of free serum prostate-specific antigen as a predictor of pathologic features of prostate cancer in a screening population. Urology 51:558, 1998. 2. BOSTWICK DG. Grading prostate cancer. Am J Clin Pathol 102 (Suppl 4): 38, 1994. 3. KAMRADT JM, SMITH DC, PIENTA KJ. Hormone refractory prostate cancer: National Comprehensive Cancer Network Guidelines. Adv Oncol 14:14, 1998. 4. LABRIE F, CUSAN L, GOMEZ JL, ET AL. Neoadjuvant<br> hormonal therapy: the Canadian experience. Urology 49:56, 1997. 5. LATIFF A. Diagnóstico y manejo tempranos del cáncer de la próstata. Trib Médica 81:284, 1990. 6. LATIFF A. Preservation of bladder neck fibers in radical prostatecmy. Urology 41:566, 1993. 7. LOWE BA. Management of stage T1a prostate cancer. Sem Urologic Oncol 14:178, 1996. 8. MORRIS MM, DALLOW KC, ZIETMAN AL, ET AL. Adjuvant and salvage irradiation following radical prostatectomy for prostate cancer. Int J Radiol Oncol Biophys 38:731, 1997. 9. PANNEK J, RITTENHOUSE HG, CHAN DW, ET AL. The use of percent free prostatic specific antigen for staging clinically localized prostate cancer. J Urol 159:1238, 1998. 10. PARTIN AW, YOO J, CARTER B, ET AL. The use of prostate specific antigen, clinical stage and Gleason score to predict pathologic stage in men with localized prostate cancer. J Urol 150:110, 1993. 11. PARTIN AW, FENELEY MR. Radical retropubic prostatectomy: limitations in high-risk disease. En: American Society of Clinical Obncology 2000 Educational Book. MC Perry (editor). American Society of Clinical Oncology. Alexandria, VA, 2000. 12. PETTAWAY CA, MANOLA J, ROTH BJ, ET AL. Neoadjuvant chemotherapy and hormonal therapy followed by radical prostatectomy: feasibility and preliminary results. J Clin Oncol 18:1050, 2000. 13. TIGUERT R, FORMAN JD, HUSSAIN M, ET AL. Radiation therapy for a rising PSA level after radical prostatectomy. Semin Urol Oncol 17:141, 1999. 14. UICC. Union Internationale Contra el Cancer. Atlas TNM. Guía ilustrada de la clasificación TNM/ pTNM de los tumors malignos. 4a Edición. Editado por P Hermanek, RVP Hutter, LH Sobin, G Wagner, Ch Wittekind. Springer-Verlag Ibérica SA. Barcelona, 1998. 475 <br><br>
| | [http://gpc.minsalud.gov.co/Documents/Guias-PDF-Recursos/Prostata/(GPC)%20Ca%CC%81ncer%20de%20pro%CC%81stata_final_pacientes%20final(web).pdf Guía de Práctica clínica (GPC) Para la Detección Temprana, Diagnóstico, Tratamiento, Seguimiento y Rehabilitación del Cáncer de Próstata(Pacientes y Cuidadores)] |
Regresar a Consulta Especializada
Regresar a Procedimiento de evaluación de guías de practica clínica
Identificación
|

|
Nombre
|
Código
|

|
|
Guía de Practica clínica (GPC) Para el Tratamiento Farmacologico y Seguimiento del Paciente con Cancer de Prostata
|
PGD1E6
|
|
Fecha de Emisión
|
Fecha de Actualización
|
Versión
|
|
2011/09/08
|
2025-07-31
|
4
|
Elaboró: Documento adoptado parcialmente de las guías del Ministerio de Protección Social, en lo referente a la falta de actualización por parte del ministerio se acepta referirse a las guías del NCCN
Revisó y Autorizo Ultima Versión: Comité de tumores
Objetivo
Servir de apoyo al personal de Oncomedic ltda, para establecer los criterios mínimos indispensables para el adecuado manejo farmacológico y seguimiento de pacientes con cáncer de mama, de acuerdo al estadio, que garanticen una atención médica integral, homogénea, con calidad, equidad y eficiencia articulada a las guías de practica clínica del ministerio de protección social y el instituto nacional de cancerología.
Alcance
Las recomendaciones generadas en esta guía contribuyen a la toma de decisiones clínicas.
Marco Conceptual
El Cáncer de prostata es considerada la primera causa de incidencia y la segunda de mortalidad por cáncer en la población masculina, se estiman, entre 6.500 y 8.000 casos nuevos de cáncer de próstata cada año, con una mayor incidencia en hombres mayores de 60 años. En Colombia, el cáncer de próstata muestra incremento de la tasa de incidencia, este comportamiento podría estar explicado por el incremento en la expectativa de vida de la población y el cambio en sus condiciones de vida.
Acorde a la propuesta del ministerio de protección social y articulada a las características de oncomedic ltda la organización adapta las guías, de modo que aplica sin modificación las recomendaciones en torno a manejo farmacológico y de seguimiento que aplican a la organización.
Conforme a la guía del Ministerio las recomendaciones presentadas se dividen por estados clínicos de la enfermedad: carcinoma ductal in situ (DCIS), cáncer temprano y localmente avanzado, cáncer metástasico
Descripción
Ruta de atención en cáncer de Próstata
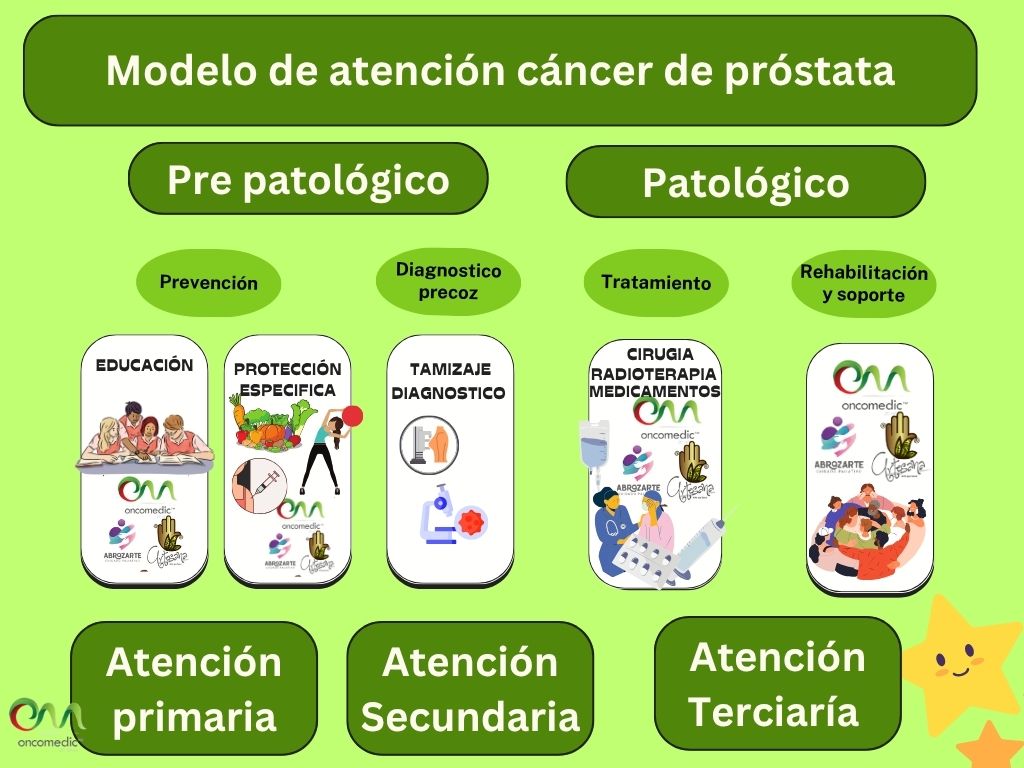
Clasificación del Cáncer de Próstata TNM
Solapas de Presentación del Texto Original

Algoritmos
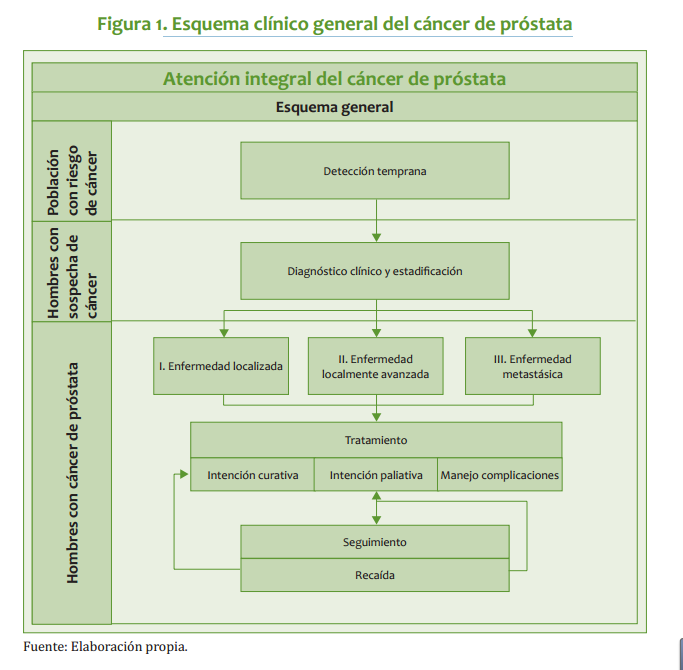
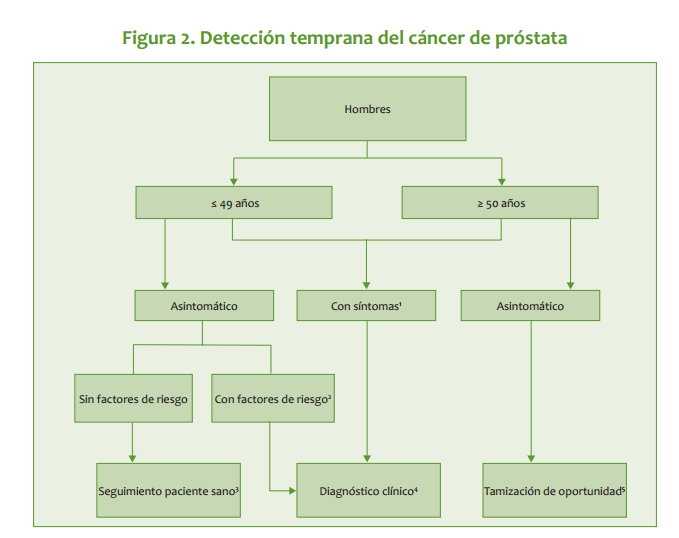
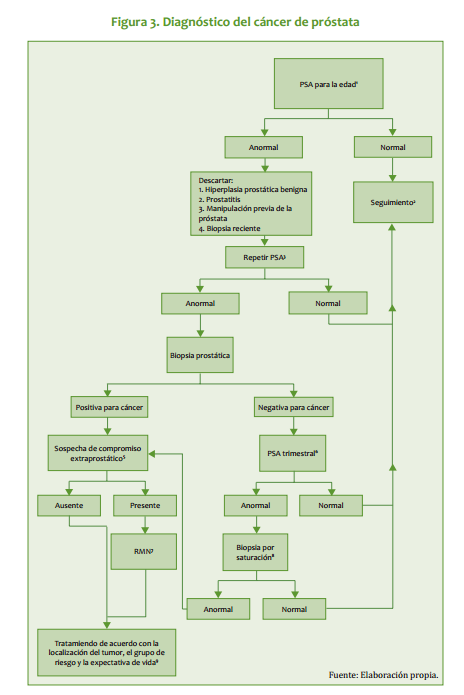
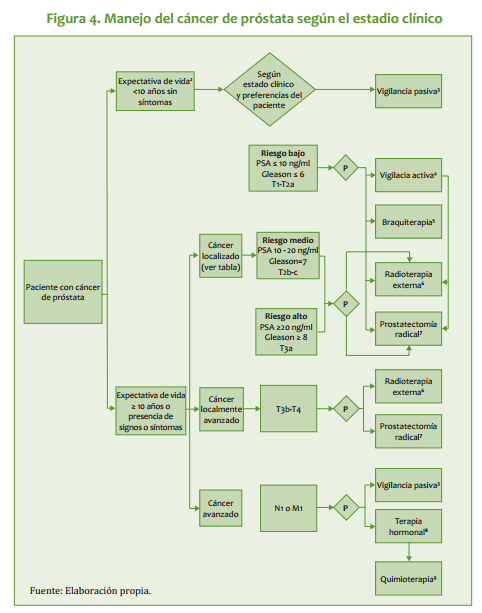
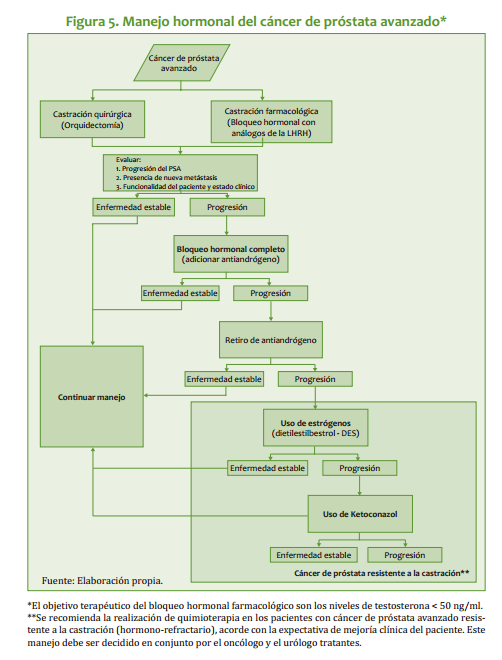
Tratamiento
- Para los tratamientos con intención curativa, la evidencia disponible muestra que el uso de terapia hormonal adyuvante en pacientes sometidos a radioterapia con beneficios en mortalidad global y recurrencia, sin un incremento significativo de la mortalidad.
- El uso de terapia hormonal adyuvante a la prostatectomía, no ha mostrado benficios que justifiquen su uso, por el contrario, se asocia con un incremento en eventos adversos.
- El uso de radioterapia adyuvante al tratamiento quirúrgico ha demostrado un efecto en la supervivencia a largo plazo, la tasa de control y el riesgo de recaída bioquímica, sin un incremento significativo de los eventos advesos.
- La mejor evidencia disponible de la adición de antiandrógenos se encuentra disponible para flutamida, otros antiandrógenos que han sido evaluados en ensayos clínicos son la nilutamida y el acetato de ciproterona. Por esta razón, se indican en primera línea del manejo hormonal la castración quirúrgica o médica con análogos de la LHRH.
- Estudios que comparan la castración médica con la castración quirúrgica no encontraron diferencias significativas en su efectividad y balance de efectos adversos.
- En el bloqueo hormonal médico los agonistas de la LHRH que han sido mejor estudiados son leuprolida, goserelina y buserelina.
- Los resultados del estudio muestran que el bloqueo androgénico máximo en cáncer de próstata avanzado puede ser una alternativa costo-efectiva para el país (estudio realizado con flutamida como antiandrógeno de adición)
- Se considera el uso de bloqueo simple (castración con análogos de la LHRH u orquidectomía) en primera línea de manejo hormonal en cáncer avanzado, y la adición de un antiandrógeno se considera alternativa de segunda línea.
- Una revisión de ensayos clínicos muestra que el uso de dietilestilbestrol (DES) podría ser de utilidad en el manejo de las oleadas de calor en el paciente en comparación con otras alternativas.
- La evidencia disponible no permite establecer una recomendación sobre el manejo de la ginecomastia en pacientes con bloqueo hormonal; se recomienda que en caso de requerirse este manejo especializado, se realice en conjunto entre urología, radioterapia y oncología.
- La evidencia clínica de los esquemas de quimioterapia en pacientes con cáncer de próstata hormono refractario indica la utilidad de la combinación de Docetaxel más prednisolonaen términos de mortalidad global, reducción del dolor y calidad de vida (53); esta comparación se realiza contra el esquema mitoxantrona más prednisolona.
- El uso de combinaciones de quimioterapia no demostró un balance riesgo-beneficio favorable que indicara su realización (54), en especial la adición de estramustina no muestra un beneficio importante (55). Las toxicidades en los esquemas con docetaxel fueron superiores.
- En cáncer de próstata hormonorefractario, el tratamiento con docetaxel cada tres semanas más prednisolona es costo-efectivo para Colombia (anexo 11, GPC completa).
- Las combinaciones de quimioterapia mitoxantrona + prednisolona, do-cetaxel + estramustina, docetaxel + estramustina + prednisolona, y prednisolona sola fueron menos costo-efectivas.
- Nuevos medicamentos, como la arabiraterona y el sipuleucel-T, no fueron evaluados y pueden ser considerados acorde con la evidencia disponible en actualizaciones posteriores de la presente guía.
- Los bifosfonatos en tratamiento de cáncer avanzado con metástasis óseas
Anexos
Guía de Práctica clínica (GPC) Para la Detección Temprana, Diagnóstico, Tratamiento, Seguimiento y Rehabilitación del Cáncer de Próstata
Guía de Práctica clínica (GPC) Para la Detección Temprana, Diagnóstico, Tratamiento, Seguimiento y Rehabilitación del Cáncer de Próstata(Completa)
Guía de Práctica clínica (GPC) Para la Detección Temprana, Diagnóstico, Tratamiento, Seguimiento y Rehabilitación del Cáncer de Próstata(Pacientes y Cuidadores)








