|
|
| (No se muestran 313 ediciones intermedias de 10 usuarios) |
| Línea 1: |
Línea 1: |
| = Identificación =
| | [[Página_principal|Regresar a la Página principal ]] |
|
| |
|
| == Elaboró: ==
| |
|
| |
| == Revisó: ==
| |
|
| |
| == Autorizó: ==
| |
|
| |
| = Introducción<br> =
| |
|
| |
| ONCOMEDIC LTDA. Consciente de la necesidad que afronta el municipio de Ibague y la zona en general, respecto a la carencia de centrales de mezclas intravenosas en sus instituciones de salud, realiza la presente propuesta para el suministro de medicamentos en Dosis Unitaria (SDMDU), que debe ser implementado en las instituciones hospitalarias de segundo nivel de complejidad en adelante como alternativa de alta eficiencia que permite el cumplimiento de la reglamentación vigente y dicionalmente múltiples beneficios en los diferentes sectores; en primera instancia beneficios sociales dados como resultado de la mejor calidad de vida lograda en los usuarios ante los tratamientos más seguros y modernos que se desarrollan. Al mismo tiempo permite el ahorro en infraestructura, recursos técnicos, humanos y administrativos, que se traducen en beneficios económicos tanto institucionales como generales, permitiendo continuar con el proceso de liderazgo institucional, generando mayor confianza dentro de las instituciones del sector y mayor productividad en términos sociales y económicos.
| |
| <br>
| |
| <br>
| |
|
| |
| = <br>Objetivo.<br> =
| |
|
| |
| == Objetivo General ==
| |
|
| |
| Implementar una central de mezclas para la preparación de medicamentos inyectables en dosis unitarias como apoyo a los servicio farmacéuticos de las IPS de la ciudad de Ibague y el departamento del Tolima.<br>
| |
|
| |
| == Objetivos específicos ==
| |
|
| |
| <br>Racionalización de distribución y administración de los medicamentos.<br>Incrementar el Control en la formulación, preparación y administración de medicamentos (Dosis correctas, interacción de medicamentos, duración del tratamiento, efectos secundarios, etc.).<br>Ahorrar los costos de los medicamentos.<br>Incrementar la seguridad para los pacientes.<br>Implementar y reforzar los programas de farmacovigilancia en las instituciones a las que se les presta el servicio
| |
|
| |
| = Marco conceptual<br> =
| |
|
| |
| De acuerdo a lo estipulado en el Decreto 2200 de 2005 Articulo 7, funciones del servicio farmacéutico, Numeral 4 (Realizar preparaciones, mezclas, adecuación y ajuste de concentraciones de dosis de medicamentos, sujeto al cumplimiento de las Buenas Prácticas de Manufactura exigidas para tal fin), la Resolución 1043 de 2006, que establece las condiciones que deben cumplir los prestadores de servicios de salud para habilitar sus servicios e implementar el componente de auditoria para el mejoramiento de la calidad de la atención, el artículo 27 de la resolución 1403 de 2007 expedida por el Ministerio de Protección Social y la resolución 2955 de 2007 en donde se manifiesta que será obligatorio a partir del 1 de enero de 2009 emplear el Sistema de Distribución de Medicamentos en Dosis Unitaria , para toda persona que realice una o más actividades y/o procesos del servicio farmacéutico donde se almacenen, comercialicen, distribuyan o dispensen medicamentos y dispositivos médicos o se realice cualquier otra actividad y/o proceso del servicio farmacéutico.
| |
|
| |
| Los sistemas tradicionales de distribución de medicamentos en los hospitales fomentan la incidencia de errores entre un 20 a 30% del total de prescripciones, esta situacion motivo que desde los años sesenta se empezaran a desarrollar sistemas más racionales de distribución de medicamentos en los hospitales.
| |
|
| |
| <br>El sistema de dosis unitaria o Uni-Dosis fundamentado en tres principios básicos (Seguridad, Rapidez y Control) fue el que demostró mayor eficacia1. Representado un gran beneficio tanto económico como laboral para las entidades de salud pues disminuye notoriamente la necesidad de inventarios, además permitir un mayor control de los mismos evitando las pérdidas y minimizando los desperdicios y sobrantes no utilizados.
| |
|
| |
| = Requisitos =
| |
|
| |
| == Recurso Humano ==
| |
|
| |
| Gerente General<br>Director Técnico (Qco. Farmacéutico),<br>Según las necesidades mas Químicos Farmacéuticos<br>Auxiliares Técnicos (A razón de hasta dos auxiliares por cada QF, según la Organización Panamericana de la Salud) <br>
| |
|
| |
|
| | = Identificación = |
| | <div> |
| <br> | | <br> |
|
| |
|
| == Programa de Farmacovigilancia<br> == | | {| width="665" cellspacing="0" cellpadding="4" |
| | |- valign="TOP" |
| | | width="129" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" rowspan="4" | |
| | <br> [[Image:Oncomedic.png]]<br> |
|
| |
|
| === Mecanismo Para la Verificacion de Ordenes Medicas<br> === | | | width="327" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" colspan="2" | |
| | '''Nombre''' |
|
| |
|
| === Protocolo de los procesos propios del servicio farmacéutico <br> === | | | width="64" style="border-top: 1px solid #000000; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0.1cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Código''' |
|
| |
|
| === Protocolo de Mecanismos para suplir las ausencias del personal principal === | | | width="111" style="border: 1px solid #000000; padding: 0.1cm" rowspan="4" | |
| | [[Image:Saludarte.png]] |
|
| |
|
| === Procedimiento de ingreso a las areas === | | |- valign="TOP" |
| | | width="327" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" colspan="2" | |
| | '''Manual de Procesos Farmacéuticos<br>''' |
|
| |
|
| === === | | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| <br>
| | '''MPF''' |
| === <br>Manual de bioseguridad ===
| |
|
| |
|
| === <br>Circulación para el ingreso y egreso de los vestieres === | | |- valign="TOP" |
| | | width="156" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Fecha de Emisión''' |
|
| |
|
| === <br>Instrucciones escritas y/o gráficas visibles para la correcta colocación de la vestimenta, en las áreas donde se requiere<br>Restringir el uso de uniformes a las áreas de trabajo === | | | width="163" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Fecha de Actualización''' |
|
| |
|
| === <br><br>Documentar procedimientos lavado (y esterilización si aplica) de uniformes de acuerdo a cada una de las áreas y/o la actividad que se realiza === | | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''Versión''' |
|
| |
|
| === <br>Se aplican los procedimientos y se supervisa su cumplimiento procedimientos para el uso, limpieza, desinfección, mantenimiento y calibración de equipos === | | |- valign="TOP" |
| | | width="156" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''2010/03/15''' |
|
| |
|
| === Realizar carteles alusivos al lavado de manos antes de ingresar a las áreas de elaboración === | | | width="163" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''2021/06/29''' |
|
| |
|
| === <br>Crear una lista de chequeo de los materiales de aseo, se debe estimar tiempos de cambio tentativos y documentar los procedimientos. === | | | width="64" style="border-top: none; border-bottom: 1px solid #000000; border-left: 1px solid #000000; border-right: none; padding-top: 0cm; padding-bottom: 0.1cm; padding-left: 0.1cm; padding-right: 0cm" | |
| | '''4''' |
|
| |
|
| === <br>Procedimientos escritos y registros de saneamiento y control de plagas ===
| | |} |
| | </div> |
| | '''<u><br></u>'''<br> |
|
| |
|
| === <br>Documentacion de la rotación de sanitizantes ===
| | '''Elaboró:''' Servicio farmacéutico. |
|
| |
|
| === <br>Fichas técnica de los diferentes sanitizantes ===
| | '''Reviso y Autorizó Ultima Versión: '''Comité de Farmacia y Terapéutica |
|
| |
|
| === <br>Manual de manejo de residuos<br><br>Contrato con el Horno incinerador documentar los dias de recoleccion y los procedimientos === | | = Introducción = |
|
| |
|
| === <br>Documentar la supervicion de la disposición final de residuos y desechos que requieren tratamiento especial mediante acta de incineracion ===
| | Oncomedic cuenta con un servicio farmacéutico encargado de la gestión de medicamentos, dispositivos médicos e insumos, liderado por personal calificado en los procedimientos de adquisición, almacenamiento, distribución y control de calidad, en alianza con un proveedor externo en para producción, dispensación y aseguramiento de la calidad de unidosis oncológicas y no oncológicas, requeridas en el funcionamiento organizacional.<br> |
|
| |
|
| === <br>Establecer y corroborar las normas de cumplimiento en las áreas ===
| | Otro de los importantes aportes del servicio farmacéutico de Oncomedic ltda lo constituyen los programas especiales de atención farmacéutica como farmacovigilancia, tecnovigilancia, seguimiento farmacoterapéutico orientados a la educación del paciente y del personal de la IPS con el fin de promover el uso racional y seguro de los medicamentos, prevenir reacciones adversas y posibles fallos terapeuticos, permitiendo no solo el cumplimiento de la reglamentación vigente, si no también optimizar los recursos técnicos y humanos, mejorar la calidad de vida en los usuarios ante tratamientos más seguros y eficaces.<br> |
|
| |
|
| === <br>Manual de mantenimiento de equipos, === | | = Objetivo<br> = |
|
| |
|
| === <br>Programas y procedimientos para el mantenimiento y reparaciones de las instalaciones, === | | == Objetivo General == |
|
| |
|
| === <br>Hoja de vida de los equipos,donde se registren los datos de su compra, proveedor, especificaciones técnicas, cuidados especiales,<br><br>Registros de uso de los equipos críticos ===
| | Establecer los lineamientos procedimentales del servicio farmacéutico de Oncomedic limitada, bajo un enfoque integral de gestión de medicamentos, dispositivos médicos e insumos que incluye los componentes científico, logístico administrativo, técnico y de gestión de la calidad como base fundamental en la prestación de servicios seguros y efectivos para la institución, las demás IPS y en general los pacientes que lo requieran en la ciudad de Ibagué, el departamento del Tolima y la zona en general.<br> |
|
| |
|
| === <br>Cronograma de calibración de equipos e instrumentos mantenimientos preventivos === | | == Objetivos específicos == |
|
| |
|
| Formatos
| | *Garantizar una oportuna gestión de medicamentos, insumos y dispositivos médicos. |
| | *Proveer un suministro seguro y eficaz de medicamentos dispositivos médicos e insumos. |
| | *Racionalizar la dispensación y administración de los medicamentos. |
| | *Promover, divulgar y gestionar los programas especiales de atención farmacéutica. |
| | *Optimizar los recursos aportando a la rentabilidad institucional.<br> |
| | *Verificar las condiciones de calidad y seguridad de los proveedores. |
| | *Cumplir con la normatividad vigente.<br><br> |
|
| |
|
| === Formatos de verificación de mantenimiento preventivo y reparaciones <br> === | | = Marco Conceptual<br> = |
|
| |
|
| BUENAS PRÁCTICAS DEL SERVICIO FARMACÉUTICO. <br>PROTOCOLOS PARA LAS PREPARACIONES MAGISTRALES Y OTRAS ACTIVIDADES DEL SERVICIO FAMACÉUTICO. <br>1.Interpretación de la orden médica y cálculo de cantidades. <br>2.Limpieza y desinfección de áreas. <br>3.Desinfección personal. <br>4.Ingreso a las áreas.<br>5.Estabilidad de los medicamentos sometidos a adecuación y mezcla. <br>6.Elaboración de preparaciones magistrales.<br>7.Contaminación accidental. <br>8.Control físico-químico y microbiano.<br>9.Uso, calibración, desinfección y mantenimiento de equipos.<br>10.Recepción y almacenamiento, reempaque, distribución de materias primas y material de acondicionamiento.<br>11.Manejo de residuos.
| | == Marco Legal == |
|
| |
|
| PROTOCOLO PARA LA DISTRIBUCIÓN DE MEDICAMENTOS MEDIANTE EL SISTEMA DE DOSIS UNITARIA.<br>El protocolo que contenga el procedimiento dentro del Sistema de Distribución de Medicamentos en Dosis Unitaria, contendrá básicamente los siguientes aspectos: <br>recepción de la orden médica; <br>elaboración del perfil farmacoterapéutico<br>detección, identificación y resolución de problemas relacionados con medicamentos -<br>PRM; <br>preparación, transporte de la medicación y devoluciones.<br> <br>PROTOCOLO PARA EL REEMPAQUE Y REENVASE DE MEDICAMENTOS A TRAVÉS DEL SISTEMA DE DOSIS UNITARiA.<br>Actividades previas.<br>Actividades propias del reempaque y reenvase<br>Actividades posteriores. <br> <br>MECANISMOS DE AJUSTE DEL SERVICIO FARMACÉUTICO. <br>SISTEMA DE INFORMACIÓN INSTITUCIONAL SOBRE MEDICAMENTOS Y DISPOSITIVOS MÉDICOS. Las instituciones prestadoras de servicios de salud, construirán e implementarán el Sistema Institucional de Información, en lo posible computarizado, sobre medicamentos y dispositivos médicos, integrado al Sistema Institucional de Salud, Sistema Integral de Información en Salud y Sistema General de Información Administrativa.
| | *Decreto 2200 de 2005 “Por el cual se reglamenta el servicio farmacéutico y se dictan otras disposiciones”<br> |
| | *Resolución 3100 de 2019 del Ministerio de Salud “Por la cual se definen los procedimientos y condiciones de inscripción de los Prestadores de Servicios de Salud y de habilitación de servicios de salud”.<br> |
| | *Resolución 1403 de 2007 “Por la cual se determina el Modelo de Gestión del Servicio Farmacéutico, se adopta el Manual de Condiciones Esenciales y Procedimientos y se dictan otras disposiciones” |
| | *RESOLUCION 001043 DE 2006 Por la cual se establecen las condiciones que deben cumplir los Prestadores de Servicios de Salud para habilitar sus servicios e implementar el componente de auditoría para el mejoramiento de la calidad de la atención y se dictan otras disposiciones. |
|
| |
|
| CONTENIDO DEL SISTEMA INSTITUCIONAL DE INFORMACIÓN SOBRE MEDICAMENTOS Y DISPOSITIVOS MÉDICOS. Este Sistema contendrá datos sobre los aspectos siguientes:
| | == Marco Referencial == |
|
| |
|
| Capacitacion
| | El servicio farmacéutico de Oncomedic ltda cuenta con un sistema de gestión de la calidad y la información que le ha permitido estar a la vanguardia jalonando el desarrollo organizacional, luego de decidir la tercerización de elaboración de las dosis unitarias nos comprometemos a mantener la calidad y seguridad de la atención mediante un trabajo articulado con los proveedores, y un modelo de atención farmacéutica mediante el desarrollo de actividades educativas y de acompañamiento continuo a los pacientes, lo que es de vital importancia ya que genera un impacto positivo en el uso seguro de medicamentos, buenas practicas de almacenamiento en casa, adherencia farmacológica, prevención de incidentes o eventos adversos relacionados con la utilización de medicamentos y dispositivos médicos, de igual manera un impacto económico por medio de la conciliación farmacológica y análisis de pertinencia. <br> |
|
| |
|
| Reunion semestral para realizar un programa de capacitación ordinario con sus respectivas actas de la reunion programación y ejecución<br>Socializacion de manuales y funciones con actas tanto al ingreso como anualmente o cuando se presenten cambios<br>BUENAS PRACTICAS DE ELABORACION<br>HIGIENE Y SALUD OCUPACIONAL<br>EVALUACION DE LAS BPE, REALIZAR FORMATO E INSTRUCTIVOS<br>BIOSEGURIDAD<br>MANEJO DE NORMAS DE BISEGURIDAD PARA PERSONAL AGENO AL SERVICIO
| | En respuesta a los continuos cambios se ha generado una reorganización empresarial y una nueva planificación de las estructuras existentes en consonancia con estas actividades, de tal manera que el servicio farmacéutico realiza un aporte significativo a los procesos misionales de la institución aportando al progreso de la organización y el sector articulado a los principios de seguridad, eficiencia y efectividad generando beneficio tanto económico como social evitando las pérdidas y minimizando la generación de residuos de medicamentos siendo de este modo también mas amigable con el entorno. |
|
| |
|
| 5.Salud ocupacional
| | <br> |
| | |
| Comité de Salud Ocupacional o Vigía de la Salud<br>Mapa de Riesgos<br>Planes de contingencia para los riesgos calificados como críticos con base en el Mapa de Riesgos<br>Programa de seguridad Industrial<br>Equipos para control y prevención de incendios, los extinguidores deben tener accesos libres y delimitados estar vigentes, formatos y procedimientos de verificación del correcto funcionamiento delos mismos <br>Planos y señales de evacuación<br>Simulacros de evacuación y actas de los mismos<br>Cumplir con las normas vigentes sobre control y prevención de incendios, acorde con la legislación nacional vigente<br>procedimientos para el manejo de eventualidades (derrames, roturas,etc.
| |
| | |
| <br>6. INFRAESTRUCTURA FISICA<br>Pisos. Los pisos deben ser de material impermeable, resistente y contar con sistema de drenaje que permita su fácil limpieza y sanitización.<br>Paredes. Las paredes y muros deben ser impermeables, sólidos, de fácil limpieza y resistentes a factores ambientales como humedad y temperatura.<br>Techos. Los techos y cielo rasos deben ser resistentes, uniformes y de fácil limpieza y sanitización.<br>Áreas de almacenamiento. Las áreas para el almacenamiento de medicamentos y dispositivos médicos deben ser independientes, diferenciadas y señalizadas, con condiciones ambientales, temperatura y humedad relativa controladas.<br>Iluminación. Debe poseer un sistema de iluminación natural y/o artificial que permita la conservación adecuada e identificación de los medicamentos y dispositivos médicos y un buen manejo de la documentación.<br>Instalaciones eléctricas. Plafones en buen estado, tomas, interruptores y cableado protegido.<br>Ventilación. Debe tener un sistema de ventilación natural y/o artificial que garantice la conservación adecuada de los medicamentos y dispositivos médicos. No debe entenderse por ventilación natural las ventanas y/o puertas abiertas que podrían permitir la contaminación de los medicamentos y dispositivos médicos con polvo y suciedad del exterior. <br>Condiciones de temperatura y humedad. Los sitios donde se almacenen medicamentos deben contar con mecanismos que garanticen las condiciones de temperatura y humedad relativa recomendadas por el fabricante y los registros permanentes de estas variables, utilizando para ello termómetros, higrómetros u otros instrumentos que cumplan con dichas funciones.<br>Criterios de almacenamiento. Los dispositivos médicos y los medicamentos se almacenarán de acuerdo con la clasificación farmacológica (medicamentos) en orden alfabético o cualquier otro método de clasificación, siempre y cuando se garantice el orden, se minimicen los eventos de confusión, pérdida y vencimiento durante su almacenamiento. El sistema de segregación de los dispositivos médicos y medicamentos debe garantizar que el lote más próximo a vencerse sea lo primero en dispensarse.<br>.2 Áreas
| |
| | |
| 1.2.1 Servicio farmacéutico hospitalario de baja complejidad
| |
| | |
| a)Área administrativa, debidamente delimitada<br>b)Área de recepción de medicamentos y dispositivos médicos.<br>c)Área de cuarentena de medicamentos.<br>d)Área adecuada para almacenamiento, teniendo en cuenta los tipos de productos que se van a distribuir y/o dispensar.<br>e)Área independiente y segura para el almacenamiento de medicamentos de control especial.<br>f)Área para la dispensación de medicamentos y entrega de dispositivos médicos.<br>g)Área debidamente identificada para el almacenamiento de medicamentos que deben ser destruidos o desnaturalizados, por vencimiento o deterioro. <br>h)Área destinada para el almacenamiento de productos rechazados, devueltos y retirados del mercado.<br>i)Área para manejo y disposición de residuos, de acuerdo con la reglamentación vigente<br>j)Área independiente y diferenciada para la elaboración de una o varias de las preparaciones magistrales siguientes: mezcla de nutrición parenteral; mezcla y/o adecuación y ajuste de concentraciones de medicamentos oncológicos; preparaciones estériles; adecuación y ajuste de concentraciones de otros medicamentos para cumplir con la dosis prescrita y radiofármacos. <br>k)Areas de cuarentena
| |
| | |
| Varias preparaciones magistrales pueden elaborarse en una misma área, siempre que tengan similar naturaleza y se cuente con la dotación necesaria.<br>La elaboración y/o adecuación de productos estériles requiere de área exclusiva. Sin embargo, la elaboración, mezcla y manipulación de productos oncológicos deberán realizarse en área separada de los demás productos estériles.
| |
| | |
| Separadas y claramente identificadas, o mecanismo para sustituirlas de manera segura<br>Areas separadas para almacenamiento de materiales o productos rechazados, vencidos o devueltos <br>Identificados los materiales de partida, insumos y productos<br>Almacenar los envases, etiquetas y otros materiales impresos en sitio(s) adecuado(s) y seguro(s) documentar
| |
| | |
| Areas accesorias (de servicio al personal)<br>Servicios Sanitarios<br>Ubicados en sitios convenientes y separados para personal femenino y masculino (no es obligatorio) suficientes de acuerdo al número de personas y adecuadamente aseados y ventilados<br>Cuentan con la dotación necesaria. separados de las áreas de elaboración y/o almacenamiento<br>Vestieres<br>vestieres separados para personal femenino y masculino, separados de los sanitarios en adecuadas condiciones de limpieza, orden y ventilacion<br>Lockeer para guardar los objetos personales,<br>Areas separadas para ropa de calle y de trabajo
| |
| | |
| DOTACIÓN DEL SERVICIO FARMACÉUTICO HOSPITALARIO
| |
| | |
| El servicio farmacéutico hospitalario, de acuerdo con su grado de complejidad, estará dotado de los equipos; instrumentos; materiales; literatura científica disponible aceptada internacionalmente; soporte bibliográfico actualizado sobre estabilidad y compatibilidad; y la farmacopea de base oficialmente adoptada en Colombia, necesarios para el cumplimiento de los objetivos de las actividades y/o procesos que realiza.<br>Identificar los equipos según el estado de uso o limpieza en que se encuentran<br>Identificar los equipos fuera de uso se encuentran identificados<br>Rotular los instrumentos y equipos, indicando la vigencia de la calibración?<br>Termometro para los equipos de cadena de frío
| |
| | |
| COMITÉ DE FARMACIA Y TERAPÉUTICA <br>Actividades de promoción y prevención
| |
| | |
| <br>
| |
| | |
| <br>12. CONTRATOS<br>Contratos escritos que estipulen claramente las obligaciones de cada una de las partes y abarca todos los procesos y gestión técnica relacionada con los mismos?<br>Incluye auditorías periódicas por parte del contratante a las instalaciones del contratista para verificar las condiciones del trabajo que debe realizarse para el cumplimiento del objeto del contrato<br>Establecer en el contrato la verificación del cumplimiento de las obligaciones estipuladas<br>En el contrato se establece la responsabilidad solidaria entre contratante y contratista por la prestación del servicio o la realización de la labor<br>El contrato define la posibilidad de ceder total o parcialmente el mismo por parte del contratista
| |
| | |
| 13. AUDITORIAS INTERNAS<br>Implementado un programa y su procedimiento para la auditoría interna, de acuerdo a un cronograma definido<br>Crear formatos y reportar actividades<br>Documentar la definicion responsables y se realiza seguimiento y cierre a las acciones planteadas
| |
| | |
| 14. SISTEMA DE INFORMACION – FARMACOVIGILANCIA<br>Sistema de información sobre medicamentos y dispositivos médicos<br>fuentes de donde es obtenida la información<br>Comunicación con los otros servicios de la Institución Prestadora de Servicios de Salud<br>Establecer un procedimiento escrito para que los usuarios soliciten información<br>Establecer un procedimiento para dar la información solicitada<br>Nombrar un responsable de dar la información<br>El sistema debe contener los datos enumerados en el artículo 21 de la Resolución 1403 de 2007<br>Solicitar reporte de los eventos adversos relacionados con medicamentos<br>Programa de farmacovigilancia<br>Estandarizar procedimientos para la notificación, registro y procesamiento de eventos adversos<br>Análisis clínico de la información reportada del evento adverso<br>Estandarizar un procedimiento para el envío de reportes a la entidad reguladora correspondiente<br>El establecimiento farmacéutico y/o servicio farmacéutico adopto el formato de reporte de eventos adversos que posee el Invima?
| |
| | |
| 14.2.6.1 ¿El formato o formulario de notificación de eventos adversos contiene la información<br>básica siguiente?<br>a) Identificación del paciente, incluyendo género y/o edad.<br>b) Medicamento sospechoso y medicación concomitante. Para cada medicamento: indicación,<br>fecha de inicio, dosis, vía, frecuencia de administración y momento en que se suspendió su<br>utilización.<br>c) Información sobre el evento: inicio, evolución y desenlace.<br>d) Diagnóstico y enfermedades concomitantes, incluyendo para-clínicos pertinentes.<br>e) Identificación del notificador, profesión y contacto.<br>Mayor<br>Programa de capacitación continuo a los profesionales y grupo de trabajo que incluya el perfil de seguridad de los medicamentos utilizados en el establecimiento farmacéutico y/o servicio farmacéutico?<br>Posee el establecimiento farmacéutico y/o servicio farmacéutico un grupo de profesionales que analice los eventos adversos<br>Participa el establecimiento farmacéutico y/o servicio farmacéutico en el programa nacional de farmacovigilancia<br>Tiene establecido un procedimiento escrito para participar?<br>Tiene establecido un procedimiento para el envío de los reportes al Invima y a la entidad territorial de salud
| |
| | |
| SISTEMA DE TRATAMIENTO DE AGUAS<br>Sí No Criterio<br>sistema de tratamiento para la obtención de agua purificada a emplear en la elaboración de preparaciones magistrales<br>Se realiza mantenimiento periódicamente con registro, controles de calidad al agua obtenida periodicidad se realizan estos controles registro
| |
| | |
| REQUISITOS ESPECIFICOS<br>16. REEMPAQUE Y REENVASE DE MEDICAMENTOS – SISTEMA DE DISTRIBUCION DE<br>MEDICAMENTOS EN DOSIS UNITARIA<br>Dotación para las preparaciones magistrales <br>a)Un soporte horizontal que evite en lo posible las vibraciones, con espacio suficiente para la(s) balanza(s) y que garantice una correcta pesada.<br>b)Armarios y estanterías impermeables, de fácil limpieza, con suficiente capacidad para colocar los materiales, protegidos del polvo y de la luz, si procediere.<br>c)Un frigorífico dotado de termómetro de temperatura máxima y mínima para almacenar los productos termolábiles: materias primas, productos a granel o producto terminado, e instrumentos para controlar la temperatura y humedad relativa, en casos que se requiera.<br>d)Los elementos, instrumentos y equipos necesarios para cada preparación en particular.<br>Cabina de flujo laminar calificada operacionalmente con una frecuencia mínima anual, la variedad de ésta será determinada por la organización, de acuerdo con la cantidad y complejidad de las preparaciones. <br>Mezclador automático, si se requiere.<br>Medidor de diferencial de presiones debidamente calibrado, en aquellas áreas que se requieran.<br>Termo-selladora, si se requiere.<br>Termo-higrómetro. <br>Vestuario para el personal que ingrese allí: vestido estéril, incluyendo polainas, gorro, tapabocas y guantes estériles. <br>Recipientes para el depósito de desechos de acuerdo con su clasificación.<br>Lavamanos y vestier.<br>Dispositivos médicos estériles para transferencia y medición de los constituyentes de la nutrición.
| |
| | |
| Procedimiento <br>a) Actividades previas.<br>b) Actividades de elaboración. <br>c) Actividades posteriores. <br>3.4 Controles en la elaboración de mezclas de nutrición parenteral<br> 3.5 Documentación<br>Los que contengan los protocolos a que se refieren los artículo 10º y 11° de la presente resolución, que se apliquen a las preparaciones magistrales.<br>Los que contengan la capacitación del personal.<br>Los que contengan los controles en proceso e inspección final.<br>Los de manejo de desviaciones<br>Los de despacho y devoluciones. <br> Los de quejas y reclamos.
| |
| | |
| Protocolos y procedimientos de Adecuación y ajuste de concentraciones de dosis de medicamentos de administración parenteral<br>Protocolos y procedimientos de MEZCLAS DE MEDICAMENTOS ONCÓLOGICOS <br>Farmacovigilancia<br>Reportes<br>TRANSPORTE DE MEDICAMENTOS Y DISPOSITIVOS MÉDICOS<br>Transporte de materias primas y/o medicamentos de control especial<br>Embalaje de medicamentos <br>Entrega y recepción <br>Condiciones del transporte<br> Responsabilidad del transportador<br><br>
| |
| | |
| <br> Requisitos externos:
| |
| | |
| Inventario adecuado de los medicamentos utilizados y de los materiales utilizados.
| |
| | |
| Contar con el servicio de proveedores de medicamentos y de materiales adecuados.<br> Buenos productos, servicios y tecnología que tiene que adquirirse fuera de la Institución.
| |
| | |
| Requisitos de Recursos (Central Externa)
| |
| | |
| Requisitos tecnológicos:
| |
| | |
| Area Física adecuada (Espacio, sellado, revestimientos, etc.)<br>Cámara(s) de flujo laminar.<br>Equipo automatizado para preparación de mezclas parenterales con doble control de volumen y peso mediante balanza de alta precisión que cuente con los programas adecuados de cálculo y operación.<br>Computador (es) para facturación, cálculos, estadística y con un programa para manejo de pacientes y medicamentos (IV)2.<br>Impresora(s) y Fax(es).<br>Estanterías y Nevera (Pre y Post).
| |
| | |
| Requisitos de personal:
| |
| | |
| Se requieren, un Gerente General, un Director Técnico (Qco. Farmacéutico), Químico Farmacéutico. Según las necesidades Químicos Farmacéuticos y Auxiliares Técnicos (A razón de dos auxiliares por cada QF, según la Organización Panamericana de la Salud).<br> Personal de distribución.<br> Personal de ventas con conocimientos del sistema.
| |
| | |
| Requisitos de otros recursos:
| |
| | |
| Distribución:
| |
| | |
| Medios de Comunicación (Fax o módem necesarios)
| |
| | |
| Medos de transporte rápidos.
| |
| | |
| Medios de almacenamiento (Pre y Post).
| |
| | |
| Material de promoción.
| |
| | |
| <br>BIBLIOGRAFÍA <br>1. Bonal de Falgás J. Bases para el desarrollo y aprovechamiento sanitario de la farmacia hospitalaria. Organización Panamericana de la Salud. 1987.
| |
| | |
| 2. American Society of Hospital Pharmacist. Draft guidelines on quality assurance for pharmacy prepared sterile products. Am J Hosp Pharm. 1992:407-17.
| |
| | |
| 3. American Society of Hospital Pharmacist. ASHP technical assistance bulletin on quality assurance for pharmacy-prepared sterile products. AM J Hops Pharm. 1993;50-2386-98.
| |
| | |
| 4. American Society of Hospital Pharmacist. ASHP statement on unit dose drug distribution. Am J Hosp Pharm. 1989;46:2346.
| |
| | |
| 5. American Society of Hospital Pharmacist. ASHP guidelines: minimum standard for pharmacies in institutions. Am J Hosp Pharm. 1985; 42:372-5.
| |
|
| |
|
| 6. American Society of Health-System Pharmacists. National survey of pharmacy practice in hospital settings, 2002. Am J Health-Syst Pharm. Vol. 60. No. 1. Enero, 2003. Pág. 52-69.
| | = Descripción del Proceso del Servicio Farmacéutico: = |
|
| |
|
| 7. Lee LW, Wellman GS, Birdwell SW et al. Use of an automated medication storage and distribution system. Am J Hosp Pharm. 1992; 49:851-5.
| | El servicio farmaceutico cuenta con multiples procesos y procedimientos fundamentales que requieren de gran precisión y control, con objetivos procedimentales se establecieron los componentes de acción del servicio farmaceutico asi: |
|
| |
|
| 8. Ray MD, Aldrich LT, Lew PJ. Experience with an automated point-of-use drug distribution system. Hosp Pharm. 1995; 30:18,20-3,27-30.
| | == Componente Científico == |
|
| |
|
| 9. Schwarz HO, Brodowy BA. Implementation and evaluation of an automated dispensing system. Am J Health-Syst Pharm. 1995; 52:823-8.
| |
|
| |
|
| 10. Borel JM, Rascati KL. Effect of an automated, nursing unit-based drug-dispensing device on medication errors. Am J Health-Syst Pharm. 1995; 52:1875-9.
| | *[[Selección de medicamentos|Selección de Medicamentos e Inclusión en el Listado de Medicamentos de Oncomedic]] |
| | *[[Atención farmacéutica|Atención Farmacéutica]] |
| | *[[Farmacovigilancia|Programa de Farmaco-vigilancia]] |
| | *[[Programa de Tecnovigilancia|Programa de Tecno-vigilancia]]<br> |
| | *[[Procedimiento de Informacion de Medicamentos|Información de Medicamentos]] |
| | *[[Recepcion de Medicamentos y Dispositivos medicos|Procedimiento Recepción de Medicamentos y Dispositivos Médicos]]. |
|
| |
|
| 11. Perini VJ, Vermeulen LC Jr. Comparison of automated medication-management systems. Am J Hosp Pharm. 1994; 51:1883-91.
| | == Componente Administrativo y Logístico == |
| | |
| | *[[Contratacion|Procedimiento de Contratación de Proveedores Para la Adquisición de Medicamentos y Dispositivos Médicos]]. <br> |
| | *[[Adquisicion de Medicamentos y Dispositivos Medicos|Procedimiento Adquisición de Medicamentos y Dispositivos Médicos]]. |
| | *[[Recepcion de Medicamentos y Dispositivos medicos|Procedimiento Recepción de Medicamentos y Dispositivos Médicos]]. |
| | *[[Almacenamiento de Medicamentos y Dispositivos Medicos|Procedimiento de Almacenamiento de Medicamentos y Dispositivos Médicos]]. |
| | *[[Distribucion de Medicamentos y Dispositivos medicos#Componente_Cient.C3.ADfico|Distribución de Medicamentos y Dispositivos Médicos]]. |
| | *[[Manual_Farmacotecnia_Elaboraci%C3%B3n_de_Productos#Protocolo_de_Elaboraci.C3.B3n_de_Unidosis_Oncol.C3.B3gicas|Manual Farmacotecnia Elaboración de Productos]] |
| | *[[Procedimiento de Devolución de Medicamentos y Dispositivos Medicos|Procedimiento de Devolución de Medicamentos y Dispositivos Médicos]]. |
| | *[[Manual de Disposición Final de Medicamentos y Dispositivos Medicos|Procedimiento de Disposición final de Medicamentos y Dispositivos Médicos]]. |
|
| |
|
| 12. Talley CR. Whither unit dose distribution? Am J Hosp Pharm. 1994; 51:1879. Editorial.
| | == Componente de Gestión de la Calidad y de Apoyo == |
|
| |
|
| 13. Summerfield MR. Dangers of compromising drug distribution. Am J Health-Syst Pharm. 1995; 52:752-3. Commentary.
| | *[[Proceso de Gestion de Calidad|Proceso de Gestión de Calidad]] |
| | *[[Programa de Calidad del Servicio Farmacéutico]] |
| | *[[Programa Sistema de Gestión de la Seguridad y Salud en el Trabajo|Programa del Sistema de Gestión de la Seguridad y Salud en el Trabajo]] |
| | *[[Subprograma de Orden Aseo y Bioseguridad|Subprograma de Orden Aseo y Bioseguridad]] |
|
| |
|
| 14. National Coordinating Committee on large Volume Parenterals. Recommended guidelines for quality assurance in hospital centralized intravenous admixture service. Am J Hospital Pharm 1980; 37:645-55.
| | = Cuadro de Procesos = |
|
| |
|
| 15. Buchanan C Mckinnon B, Scheckelhoff D, Schneider, P Principles of sterile Product Preparation 1ª edición. Bethesda: American Society of Health-System Pharmacist, 1995 Hunt M, Tomo V ed. Training Manual for Intravenous Admixture Personnel. 5ª edición.
| | {| cellspacing="1" cellpadding="1" border="1" style="width: 1000px; height: 1257px;" |
| | |- |
| | | Nombre del proceso |
| | | Procesos del Servicio Farmacéutico. |
| | |- |
| | | Coordinador del proceso |
| | | Dirección Técnica. |
| | |- |
| | | Producto |
| | | Adecuada gestión de medicamentos y dispositivos médicos. |
| | |- |
| | | Entrada |
| | | |
| | Solicitud de servicios de uso racional de medicamentos y dispositivos médicos. |
| | *Selección de medicamentos. |
| | *Adquisición y/o recepción de medicamentos y dispositivos. |
| | *Ordenes medicas. |
| | *Autorizaciones. |
| | *Solicitud de adecuación de unidosis por proveedor. |
| | |- |
| | | Salidas |
| | | |
| | *Recepción y administración de unidosis. |
| | *Medicamentos/tratamientos. |
| | *Devoluciones. |
| | *Residuos. |
| | *Atención farmacéutica. |
| | *Reportes. |
| | |- |
| | | Procedimientos |
| | | '''Componente Científico.''' |
| | *Selección de Medicamentos. |
| | *Atención Farmacéutica. |
| | *Fármaco-Vigilancia. |
| | *Información de Medicamentos. |
| | '''Componente Administrativo y Logístico.''' |
| | *Procedimiento de Contratación de Proveedores Para la Adquisición de Medicamentos y Dispositivos Médicos. |
| | *Procedimiento de Adquisición y Recepción de Medicamentos y Dispositivos médicos. |
| | *Procedimiento de Almacenamiento de Medicamentos y Dispositivos Médicos. |
| | *Distribución de Medicamentos y Dispositivos Médicos. |
| | *Procedimiento de Devolución de Medicamentos y Dispositivos Médicos. |
| | *Manual Para Ajuste de Dosis y Concentración de Medicamentos Con Proveedor Externo. |
| | '''Componente de Gestión de la Calidad y de Apoyo.''' |
| | *Programa de Calidad del Servicio Farmacéutico. |
| | |} |
|
| |
|
| 16. ASHP Guidelines on outsourcing pharmaceutical services. 1999. Am J Health-Syst Pharm. <br>17. Kastango, E. S. Sterile-Product preparations: Mix or Buy? International Journal of Pharmaceutical Compounding. Vol. 5 No. 1. Enero-Febrero, 2001. Pág. 59-63.
| |
|
| |
|
| 18. Galatowitsch, S. Hospital pharmacy staff may risk significant exposure to cytotoxics. Journal of the American Society of Health-System Pharmacists. Vol. 13. No. 10. Octubre, 1999. <br>
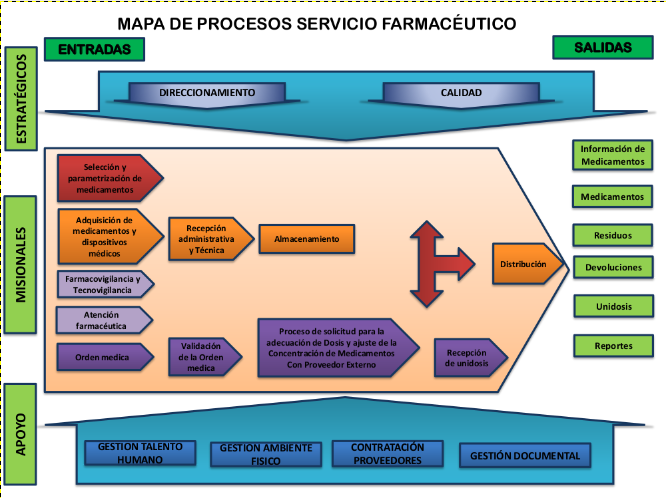
| | [[Image:Mapa procesos Farmacia.png]] |